Wetenschap
Complexe patronen:een brug bouwen van het grote naar het kleine
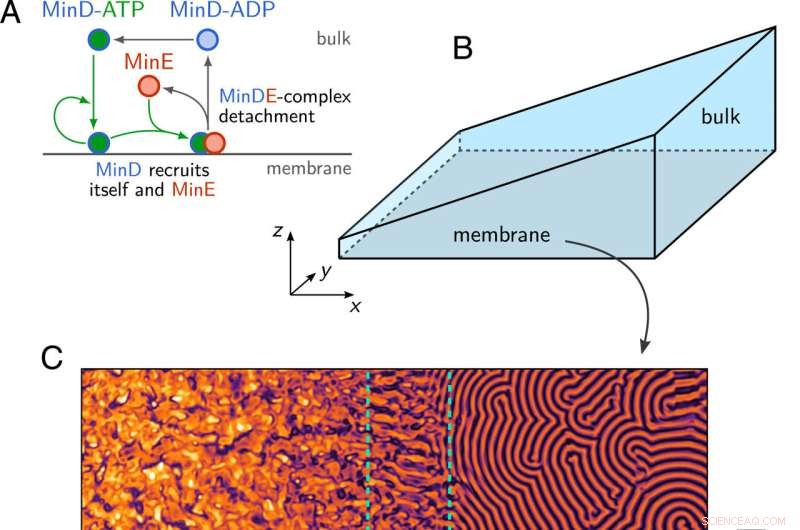
(A) Schematische illustratie van het Min-eiwitreactienetwerk. (B) Wiggeometrie met een membraanoppervlak op het bodemvlak (z =0) en bulkhoogte H (x) lineair toenemend langs de x-richting. (C) Momentopname van de membraandichtheid van MinD, verkregen door de Min-dynamiekvergelijkingen numeriek te simuleren. 1-3 in de geometrie getoond in B. Men observeert regio's met chaotische patronen, staande golven (SW, gestreepte groene omtreklijn) en lopende golven (TW) langs het membraan en op verschillende bulkhoogten. Credit:Procedures van de National Academy of Sciences (2022). DOI:10.1073/pnas.2206888119
Voor veel levensbelangrijke processen zoals celdeling, celmigratie en de ontwikkeling van organen is de ruimtelijk en temporeel correcte vorming van biologische patronen essentieel. Om deze processen te begrijpen, bestaat de belangrijkste taak niet uit het uitleggen hoe patronen ontstaan uit een homogene begintoestand, maar uit het uitleggen hoe eenvoudige patronen veranderen in steeds complexere. Het belichten van de mechanismen van deze complexe zelforganisatie op verschillende ruimtelijke en temporele schalen is een belangrijke uitdaging voor de wetenschap.
Met zogenaamde "grofkorrelige" technieken kunnen dergelijke meerschalige systemen worden vereenvoudigd, zodat ze met een gereduceerd model op grote lengte- en tijdschalen kunnen worden beschreven. "De prijs die je betaalt voor grofkorreligheid is echter dat belangrijke informatie over de patronen op kleine schaal - zoals het patroontype - verloren gaat. Maar het punt is dat deze patronen een beslissende rol spelen in biologische systemen. Om een voorbeeld te geven , ze controleren belangrijke cellulaire processen", legt Laeschkir Würthner uit, lid van het team onder leiding van LMU-natuurkundige prof. Erwin Frey en hoofdauteur van een nieuwe studie gepubliceerd in de Proceedings of the National Academy of Sciences dat dit probleem oplost.
In samenwerking met de onderzoeksgroep van prof.dr. Cees Dekker (TU Delft) heeft het team van Frey een nieuwe grofkorrelige benadering ontwikkeld voor zogenaamde massabesparende reactie-diffusiesystemen, waarbij de grootschalige analyse van de totale dichtheden van de betrokken deeltjes maken de voorspelling van patronen op kleine schaal mogelijk.
De wetenschappers illustreerden het potentieel van hun aanpak met het Min-eiwitsysteem, een paradigmatisch model voor biologische patroonvorming. De bacterie E. coli gebruikt verschillende Min-eiwitten die in een cel circuleren om te bepalen op welke locatie celdeling plaatsvindt. Doorslaggevend hierbij is dat de betrokken eiwitten met verschillende frequenties voorkomen, afhankelijk van hun locatie in de cel en de chemische toestand, dat wil zeggen dat ze verschillende dichtheden hebben.
"We zijn er nu in geslaagd om de complexiteit van dit systeem te verminderen door een theorie te ontwikkelen die uitsluitend gebaseerd is op de totale dichtheden van de eiwitten, zodat we de dynamiek van patroonvorming volledig kunnen spiegelen", zegt Frey. "Dit is een enorme reductie. De numerieke berekeningen worden nu in enkele minuten uitgevoerd in plaats van maanden."
De onderzoekers konden de theoretische voorspellingen van het model experimenteel bevestigen, volgens welke de verdeling van de eiwitten afhangt van de geometrie van de omgeving. Dit deden ze door het Min-eiwitsysteem te reconstrueren in een in vitro flowcel, waarbij de resultaten dezelfde eiwitpatronen lieten zien als in de simulatie.
"Een dergelijke reconstructie van informatie op kleine schaal van verminderde dynamiek op macroscopisch niveau opent nieuwe wegen voor een beter begrip van complexe meerschalige systemen, die voorkomen in een breed scala van fysieke systemen", zegt Frey. + Verder verkennen
Biologische patroonvormende systemen worden beter gekarakteriseerd door geometrie dan simulaties
 Feiten over Nylon
Feiten over Nylon Nieuwe mogelijkheden voor lichtgevende kunststoffen met patroonlicht
Nieuwe mogelijkheden voor lichtgevende kunststoffen met patroonlicht Nieuw onderzoek toont aan dat alle solid-state batterijen met de hoogste energiedichtheid nu mogelijk zijn
Nieuw onderzoek toont aan dat alle solid-state batterijen met de hoogste energiedichtheid nu mogelijk zijn Extreme verbetering van koolwaterstofvergassing via mechanochemie
Extreme verbetering van koolwaterstofvergassing via mechanochemie Team vervaardigt magneten volledig van zeldzame aardmetalen uit de VS
Team vervaardigt magneten volledig van zeldzame aardmetalen uit de VS
Hoofdlijnen
- Genomische analyse onthult de ware oorsprong van hondachtigen in Zuid-Amerika
- Vissenseks zo luid dat dolfijnen doof kunnen worden
- Wat is TA Cloning?
- Wat is de Chromatins-functie?
- Epigenetica legt uit waarom je DNA je lot niet voorspelt
- Nieuwe methode om sneller en nauwkeuriger antigenen te vinden die specifieke immuuncellen activeren
- 10 manieren waarop uw geheugen volledig onnauwkeurig is
- Dode vissen en depressies aan de oevers van de Oder
- Gene ontdekking kan cassaveziekte bestrijden, voedselzekerheid vergroten
 Vijf manieren waarop India zijn boeren moet helpen de dreiging van klimaatverandering het hoofd te bieden
Vijf manieren waarop India zijn boeren moet helpen de dreiging van klimaatverandering het hoofd te bieden Bodemsoorten in North Carolina
Bodemsoorten in North Carolina Onderzoekers kijken in detail naar de interfaces in perovskiet-zonnecellen
Onderzoekers kijken in detail naar de interfaces in perovskiet-zonnecellen Natuurkundigen breiden quantum machine learning uit tot oneindige dimensies
Natuurkundigen breiden quantum machine learning uit tot oneindige dimensies Wetenschappers bouwen M29-clustermodelkatalysator
Wetenschappers bouwen M29-clustermodelkatalysator De methaanbom onschadelijk maken - we kunnen nog steeds een verschil maken
De methaanbom onschadelijk maken - we kunnen nog steeds een verschil maken Autonome machines op weg naar grotere onafhankelijkheid
Autonome machines op weg naar grotere onafhankelijkheid Cijfers beperken hoe nauwkeurig digitale computers chaos modelleren
Cijfers beperken hoe nauwkeurig digitale computers chaos modelleren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com