
Wetenschap
Wetenschappers tasten de grenzen van ijs af

Krediet:CC0 Publiek Domein
Hoe klein is het kleinst mogelijke ijsdeeltje? Het is geen sneeuwvlok, meten op maar liefst een fractie van een inch. Volgens nieuw onderzoek gepubliceerd in Proceedings van de National Academy of Sciences , de kleinste nanodruppel water waarin zich ijs kan vormen, is slechts zo groot als 90 watermoleculen - een tiende van de grootte van het kleinste virus. Op die kleine schaal, volgens de scheikundeprofessor van de Universiteit van Utah en co-auteur Valeria Molinero, de overgang tussen ijs en water wordt een beetje kroezend.
"Als je een glas water met ijs drinkt, je ziet niet dat het water in het glas alle ijs en alle vloeistof als functie van de tijd verandert, " zegt ze. In de kleinste water nanodruppels, ze zegt, dat is precies wat er gebeurt.
Waarom "ijs ik" belangrijk is
De overgang tussen water en ijs is een van de belangrijkste transformaties tussen fasen (vaste stoffen, vloeistoffen en gassen) op onze planeet, waar het unieke effecten heeft op ons klimaat en tegelijkertijd de levensvatbaarheid van het leven reguleert. Inzicht in de omstandigheden die leiden tot de vorming van ijs, dan, is een actieve zoektocht in gebieden die milieu- en aardwetenschappen omvatten, natuurkunde, scheikunde, biologie en techniek.
IJs bestaat bijna uitsluitend op aarde in de zeer geordende hexagonale kristalstructuur die bekend staat als 'ijs I'. In onze atmosfeer, kleine waterclusters vormen en bevriezen vervolgens, grotere kristallen en uiteindelijk wolken zaaien. Als gevolg van concurrerende thermodynamische effecten, echter, onder een bepaalde diameter kunnen deze waterclusters geen thermodynamisch stabiel ijs I vormen. Het exacte groottebereik van waterclusters die stabiel ijs I kunnen vormen, is jarenlang onderzocht door middel van experimenten en theorie, waarbij de meest recente schattingen het bereik verkleinden van slechts 90 watermoleculen tot wel 400.
Onderkoeling:laag en langzaam
Vroeger, een belangrijke barrière bij het experimenteel bestuderen van deze limiet was het langzaam genoeg afkoelen van de onderkoelde vloeistofclusters om het ijs I-rooster goed te laten vormen. Door te snel af te koelen ontstaan clusters van amorf ijs, een minder geordende fase. Als de clusters niet langzaam en gelijkmatig worden afgekoeld, het resultaat is een onnatuurlijke combinatie van ijsfasen. Computersimulaties van ijsvorming worden ook geconfronteerd met hun eigen uitdagingen bij het repliceren van fysica en ijsvorming op nanoschaal.
In de nieuwe studie onderzoekers van de Universiteit van Utah, de Universiteit van Californië, San Diego, de Universität Göttingen, de Max Planck Institutes for Solar System Research and Dynamics and Self-Organization in Göttingen combineren recente vooruitgang in simulatie en experiment om de wisselwerking tussen de beperkingen die optreden op de ijs-vloeistofovergang in clusters van nanometergrootte te ontrafelen.
Om het koelprobleem op te lossen, het Göttingen-team gebruikte een moleculaire bundel die clusters van de gewenste grootte genereert door aanvankelijk een mengsel van water en argon te expanderen door een mondstuk met een diameter van ongeveer 60 micrometer. De resulterende bundel wordt vervolgens door drie verschillende zones geleid waar de koelsnelheid wordt verlaagd om de vorming van de clusters te beheersen, het bereiken van een lage temperatuur van 150 K (-123 °C of -189 °F). Computermodellen van water ontwikkeld door de teams van San Diego en Utah werden gebruikt om de eigenschappen van de nanodruppels te simuleren.
Het einde van ijs
Met behulp van infrarood spectroscopische handtekeningen om de overgang naar ijs I in de clusters te volgen, de onderzoekers vonden veelbelovende overeenstemming tussen de experimentele en theoretische benaderingen. De resultaten leveren sterk bewijs dat het "einde van ijs" optreedt wanneer clusters ongeveer 90 watermoleculen zijn. Op deze maat, de clusters zijn slechts ongeveer 2 nanometer in diameter, of ongeveer een miljoen keer kleiner dan een typische sneeuwvlok.
Francesco Paesani aan de Universiteit van Californië, San Diego legt uit, "Dit werk verbindt op een consistente manier experimentele en theoretische concepten voor het bestuderen van microscopische watereigenschappen van de afgelopen drie decennia, die nu kan worden gezien in een gemeenschappelijk perspectief."
Onverwachte oscillatie
Onverwacht, de onderzoekers ontdekten in zowel simulatie als experiment dat het naast elkaar bestaan van ijs zich anders gedraagt in clusters van 90 tot 150 watermoleculen van de scherpe, goed gedefinieerde smelttransitie die we ervaren met macroscopisch (grootschalig) ijs en water dat optreedt bij 0 ° C. De clusters bleken in plaats daarvan over te gaan over een reeks temperaturen en in de tijd te oscilleren tussen de vloeibare en ijstoestand, een effect van hun kleine omvang dat drie decennia geleden voor het eerst werd voorspeld, maar tot nu toe ontbrak experimenteel bewijs.
Thomas Zeuch van de Universität Göttingen merkt op, "Macroscopische systemen hebben geen analoog mechanisme; water is vloeibaar of vast. Dit oscillerende gedrag lijkt uniek voor clusters in dit grootte- en temperatuurbereik."
"Er gaat niets boven deze oscillaties in onze ervaring van fasecoëxistentie in de macroscopische wereld!" voegt Molinero toe. In een glas water, ze zegt, zowel het ijs als het water zijn stabiel en kunnen naast elkaar bestaan, ongeacht de grootte van de ijsblokjes. Maar in een nanodruppel die zowel vloeistof als ijs bevat, de meeste watermoleculen zouden zich op het grensvlak tussen ijs en water bevinden - dus het hele tweefasencluster wordt onstabiel en oscilleert tussen een vaste stof en een vloeistof.
Wanneer ijs raar wordt
Waterclusters van de afmetingen en temperaturen in het experiment komen veel voor in interstellaire objecten en in planetaire atmosferen, inclusief die van ons, zegt Molinero. Ze bestaan ook in de mesosfeer, een atmosferische laag boven de stratosfeer.
"Ze kunnen ook bestaan als waterzakken in een matrix van een materiaal, inclusief in holtes van eiwitten, " ze zegt.
Als de oscillerende overgangen kunnen worden gecontroleerd, Molinero zegt, ze zouden mogelijk de basis kunnen vormen van een nanoklep die de doorgang van materialen mogelijk maakt als ze vloeibaar zijn en de stroom stopt als ze een vaste stof zijn.
De resultaten gaan verder dan alleen ijs en water. Molinero zegt dat de kleinschalige verschijnselen zouden moeten gebeuren voor elke stof op dezelfde schaal. "Op die manier, " ze zegt, "ons werk gaat verder dan water en kijkt meer in het algemeen naar de coda van een faseovergang, hoe het transformeert van scherp naar oscillerend en dan verdwijnen de fasen zelf en gedraagt het systeem zich als een groot molecuul."
 Risico's van natuurbranden verminderen voor beter beheer en een betere toewijzing van middelen
Risico's van natuurbranden verminderen voor beter beheer en een betere toewijzing van middelen Nieuwe NASA-inzichten in het geheime leven van planten
Nieuwe NASA-inzichten in het geheime leven van planten NASA ziet Irwin voordat het verzwakte tot een tropische storm
NASA ziet Irwin voordat het verzwakte tot een tropische storm Een circulaire economie kan een einde maken aan verspilling – ten koste van onze privacy
Een circulaire economie kan een einde maken aan verspilling – ten koste van onze privacy Lijst met unieke planten voor loofbossen
Lijst met unieke planten voor loofbossen
Hoofdlijnen
- Studie beantwoordt een al lang bestaand mysterie over slangenpredatie
- Campylobacter gebruikt andere organismen als Trojaans paard om nieuwe gastheren te infecteren
- Studie vindt potentiële celreceptoren om antibioticaresistentie te verminderen
- De meeste hondensnoepjes overschrijden de aanbevolen dagelijkse hoeveelheid energie
- Nieuwe procedure voor snellere detectie van milieueffecten van zalmkwekerijen
- De illegale schildpaddenhandel - waarom wetenschappers geheimen bewaren
- Wat is de rol van het IgM-antilichaam?
- Hoe moleculaire scharen ziekten kunnen oplossen en DNA kunnen bewerken
- Colombia,
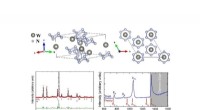
- Stabiele fauteuilachtige hexazinaatring in wolfraamhexanitride
- De nadelen van verpakkingen

- Atoomschakelaars door plasmonische verwarming van metalen contactpunten

- Het zit hem allemaal in de twist:natuurkundigen stapelen 2D-materialen onder een hoek om deeltjes op te vangen

- Lasermethode veelbelovend voor detectie van sporenchemicaliën in lucht

 Parker Solar Probe meldt goede status na nauwe zonne-aanpak
Parker Solar Probe meldt goede status na nauwe zonne-aanpak Virtuele en gemengde realiteit inferieur aan traditioneel leren in anatomieonderwijs
Virtuele en gemengde realiteit inferieur aan traditioneel leren in anatomieonderwijs Onderzoek naar de mysterieuze oorsprong van de meest extreme lichtflitsen in het universum
Onderzoek naar de mysterieuze oorsprong van de meest extreme lichtflitsen in het universum Effective Space tekent deal met satellietbedrijf om drones te gebruiken om de levensduur van satellieten in een baan om de aarde te verlengen
Effective Space tekent deal met satellietbedrijf om drones te gebruiken om de levensduur van satellieten in een baan om de aarde te verlengen Hoe heet waren de oceanen toen het leven zich voor het eerst ontwikkelde?
Hoe heet waren de oceanen toen het leven zich voor het eerst ontwikkelde? De inverse van een functie vinden
De inverse van een functie vinden "Bobcat 743 Specifications
"Bobcat 743 Specifications De gemiddelde windsnelheid tijdens een onweersbui
De gemiddelde windsnelheid tijdens een onweersbui
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

