
Wetenschap
Dynamiek van microtubuli
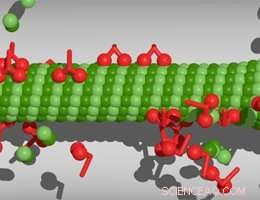
Moleculaire motoren die langs een microtubule lopen. Krediet:M. Rang/PRL
Filamenteuze polymeren, microtubuli genaamd, spelen een vitale rol bij chromosoomsegregatie en moleculair transport. Een LMU-team heeft nu onderzocht hoe de lengte van microtubuli varieert als reactie op veranderingen in de beschikbaarheid van hun eiwitcomponenten.
Cellen hebben een inwendig skelet, waardoor ze hun vorm kunnen veranderen en actief kunnen migreren. Dit cytoskelet is samengesteld uit een aantal filamentsystemen, waarvan microtubuli er één zijn. Cilindrische microtubuli hebben wanden die bestaan uit 13 protofilamenten, elk bestaande uit heterodimere subeenheden die twee verwante tubuline-eiwitten bevatten. Microtubuli verlenen niet alleen mechanische stabiliteit aan cellen en dicteren hun vorm, ze dienen ook als een intracellulair transportnetwerk. Verder, microtubuli zijn de belangrijkste bestanddelen van de mitotische spoel, die de ordelijke scheiding van de gerepliceerde chromosoomsets in de twee dochtercellen tijdens celdeling bemiddelt. Al deze functies vereisen dynamische regulering van de lengtes van microtubuli. Een groep LMU-fysici onder leiding van professor Erwin Frey, in samenwerking met Professor Stefan Diez (Technische Universiteit van Dresden en Max Planck Instituut voor Moleculaire Celbiologie en Genetica, Dresden), hebben nu een model ontwikkeld waarin de motoreiwitten die verantwoordelijk zijn voor het transport van lading langs protofilamenten ook dienen om de lengte van microtubuli te reguleren. Het model is beschreven en experimenteel gevalideerd in het tijdschrift Fysieke beoordelingsbrieven .
In eerder werk, Frey's groep had aangetoond dat de dichtheid van moleculaire motoren die aan de filamenten zijn bevestigd, van invloed is op het feit of de microtubulus groeit of krimpt, en dat hun effect afhangt van de lengte van het betreffende filament. Hoe langer de microtubuli, hoe groter het aantal motoreiwitten dat het kan accommoderen. Motormoleculen genaamd kinesines gaan langs het protofilament, stappen van het ene dimeer naar het andere. Wanneer een kinesine-eiwit het einde bereikt, het komt los van het filament en neemt de tubuline mee waaraan het is gebonden. Bijgevolg, als de motordichtheid op het protofilament hoog is, krimp zal doorgaan. Anderzijds, een nieuw tubulinedimeer kan aan het uiteinde binden. Aan het einde, motorafhankelijke krimp concurreert dus met de groei van microtubuli. "Vandaar, ervan uitgaande dat middelen (d.w.z. zowel tubulines als moleculaire motoren) aanwezig zijn bij toegang, er zal een filamentlengte zijn waarbij de groei- en krimpsnelheden in evenwicht zijn, " zegt Matthias Rank, eerste auteur van de studie. Echter, in een echte cel, het is onwaarschijnlijk dat deze componenten in onbeperkte hoeveelheden beschikbaar zijn. Bijvoorbeeld, vorming van de mitotische spoel vermindert het aantal vrije tubulinemoleculen in de oplosbare fase van het cytoplasma aanzienlijk. In de nieuwe studie de onderzoekers onderzochten de effecten van een dergelijke beperking van hulpbronnen op de regulering van de lengte van de microtubuli.
Met behulp van simulaties gebaseerd op een wiskundig model van polymeerdynamica, ze ontdekten dat onder deze omstandigheden twee verschillende mechanismen van lengteregulatie een rol spelen. Welke van deze dominant wordt, hangt af van de relatieve concentraties van de tubulinen en de motoreiwitten:in een bepaald concentratiebereik werkt het dynamische evenwicht tussen groei en krimp van de microtubuli zoals het zou zijn als de middelen niet beperkend zouden zijn. "Maar het ligt anders als een van de benodigde middelen schaars is", zegt Rang. "Dat is het geval, bijvoorbeeld, wanneer er niet genoeg motormoleculen beschikbaar zijn om een snelle depolymerisatie van de protofilamenten teweeg te brengen." In deze situatie, de microtubuli blijven groeien totdat de tubulineconcentratie onder een kritische waarde zakt. Verder, er is een concentratiebereik waarin beide processen actief zijn. "In dit geval, we zien dat de microtubuli in twee maten komen en dat ze soms wisselen tussen de twee lengtes", zegt Frey. "In fysiek opzicht dit kan worden omschreven als een faseovergang." In vitro-experimenten uitgevoerd door hun co-auteur in Dresden hebben het bestaan van dit overgangsregime voorspeld door het model van München bevestigd. Het team is ervan overtuigd dat hun resultaten ook van toepassing zijn op andere polymeersystemen , en ze vermoeden dat de beperking van belangrijke hulpbronnen een belangrijke rol kan spelen bij het reguleren van andere cellulaire processen.
 Nieuwe katalyse met één atoom zorgt voor reductieve amineringsreactie
Nieuwe katalyse met één atoom zorgt voor reductieve amineringsreactie Diagnose van kunstacne in Georgia OKeeffes-schilderijen
Diagnose van kunstacne in Georgia OKeeffes-schilderijen Waarom bevat water nul calorieën?
Waarom bevat water nul calorieën?  Een organokatalysator gebruiken om de polymerisatie te stereocontroleren
Een organokatalysator gebruiken om de polymerisatie te stereocontroleren Wie gaat er nu door met het valideren van forensische wetenschappelijke disciplines?
Wie gaat er nu door met het valideren van forensische wetenschappelijke disciplines?
 Ambtenaren in Californië dagen fracking van kustlijn uit
Ambtenaren in Californië dagen fracking van kustlijn uit Onderzoekers ontrafelen het mysterie van niet-cotectische magmatische gesteenten
Onderzoekers ontrafelen het mysterie van niet-cotectische magmatische gesteenten Rooktrends bij bosbranden verslechteren voor westelijke VS
Rooktrends bij bosbranden verslechteren voor westelijke VS De hoofdstad van Senegal overstroomt opnieuw omdat experts de slechte planning de schuld geven
De hoofdstad van Senegal overstroomt opnieuw omdat experts de slechte planning de schuld geven Je hoeft de natuur niet te kennen om ervan te houden:studeren
Je hoeft de natuur niet te kennen om ervan te houden:studeren
Hoofdlijnen
- Welke bijdrage heeft Avery geleverd aan de ontdekking van DNA?
- Waarom is chemie belangrijk voor de studie van anatomie en fysiologie?
- Bacteriën kunnen antibioticaresistentie via de bodem verspreiden
- Wat zijn de verschillen tussen PCR en klonen?
- De kenmerken van de mitochondria
- Hongerige berencrisis grijpt in het verre oosten van Rusland
- Zijn domme mensen gelukkiger?
- Wat zijn twee manieren waarop Enzymen minder effectief worden?
- Gekapte tropische regenwouden ondersteunen nog steeds de biodiversiteit, zelfs als de hitte aan staat
- Lucky Tetrachromats Zie de wereld met tot 100 miljoen kleuren

- Verstrengeling met meerdere partijen:wanneer alles met elkaar verbonden is

- Nucleaire straling visualiseren:team foto's gammastralen om Fukushima te helpen ontsmetten

- Natuurkundigen manipuleren Abrikosov draaikolken

- Spiraal gedraaide fotonische kristalvezels
 Laboratoriumtechnieken aanpassen voor instructie op afstand
Laboratoriumtechnieken aanpassen voor instructie op afstand Hoogtepunt:demping van akoestische trillingen in gouden nanodeeltjes
Hoogtepunt:demping van akoestische trillingen in gouden nanodeeltjes Het machtigen van verkiezingsfunctionarissen is cruciaal voor het opbouwen van betere verkiezingen
Het machtigen van verkiezingsfunctionarissen is cruciaal voor het opbouwen van betere verkiezingen Studie onderzoekt productiviteitspotentieel van thuisblijvers
Studie onderzoekt productiviteitspotentieel van thuisblijvers SAVI-camera dumpt lange lens voor beelden op afstand
SAVI-camera dumpt lange lens voor beelden op afstand Bedrijfsconcentratie in het Amerikaanse voedselsysteem maakt voedsel duurder en minder toegankelijk voor veel Amerikanen
Bedrijfsconcentratie in het Amerikaanse voedselsysteem maakt voedsel duurder en minder toegankelijk voor veel Amerikanen Kolencentrales grootste vervuilers in Europa
Kolencentrales grootste vervuilers in Europa Van wilde kamelen tot cocaïne-nijlpaarden, grote dieren verwilderen de wereld
Van wilde kamelen tot cocaïne-nijlpaarden, grote dieren verwilderen de wereld
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

