
Wetenschap
Hoe zout opgelost in water elektrische geleidbaarheid mogelijk maakt
Door Jesaja David Bijgewerkt op 24 maart 2022
Visage/Stockbyte/Getty Images
Elektriciteit en geleidbaarheid
Om te begrijpen waarom zout water elektriciteit geleidt, moeten we eerst elektriciteit definiëren. Elektriciteit is de stroom van geladen deeltjes – voornamelijk elektronen – door een medium. In metalen zoals koper bewegen elektronen vrij en voeren ze rechtstreeks stroom. In elektrolyten zoals zout water wordt stroom getransporteerd door ionen.
Comstock-afbeeldingen/Comstock/Getty-afbeeldingen
Zout oplossen in water
Zuiver water is een slechte geleider; er kan slechts een minuscule hoeveelheid stroom doorheen. Wanneer natriumchloride (NaCl) oplost in water, dissociëren de moleculen in natrium- (Na⁺) en chloride- (Cl⁻) ionen. Het Na⁺-ion, dat een elektron heeft verloren, heeft een positieve lading, terwijl het Cl⁻-ion, dat een elektron heeft gewonnen, een negatieve lading draagt.
Thinkstock/Comstock/Getty Images
Een stroom genereren in zout water
Door een elektrische bron toe te passen, ontstaan er twee aansluitingen:een negatieve (kathode) en een positieve (anode). Opposite charges attract, so Na⁺ ions are drawn toward the cathode and Cl⁻ ions toward the anode. Deze ionen pendelen elektronen tussen de aansluitingen en vormen een continu geleidend pad waardoor een meetbare stroom kan stromen.
Digitale visie./Digitale visie/Getty Images
 Welke groep elementen werkt als metalen en niet -metalen?
Welke groep elementen werkt als metalen en niet -metalen?  Waarom moet een atoom gelijk aantal protonen en elektronen bevatten?
Waarom moet een atoom gelijk aantal protonen en elektronen bevatten?  Nieuwe niet-covalente binding blokkeert de afstotende geur van isocyaniden
Nieuwe niet-covalente binding blokkeert de afstotende geur van isocyaniden Structure-ID-techniek zou de chemie kunnen verschuiven naar warp-snelheid
Structure-ID-techniek zou de chemie kunnen verschuiven naar warp-snelheid Waarom ondergaan slechts de halve hoeveelheid atomen verval?
Waarom ondergaan slechts de halve hoeveelheid atomen verval?
 VK roept noodtoestand uit op door storm getroffen Maagdeneilanden stuurt hulp
VK roept noodtoestand uit op door storm getroffen Maagdeneilanden stuurt hulp Geologische vingerafdrukken van vulkanische as
Geologische vingerafdrukken van vulkanische as Uitlaatgassen van schepen maken oceanische onweersbuien intenser
Uitlaatgassen van schepen maken oceanische onweersbuien intenser Abiotische factoren van de Neritische Zone
Abiotische factoren van de Neritische Zone Wat is een reagerende variabele in wetenschappelijke projecten?
Wat is een reagerende variabele in wetenschappelijke projecten?
Wetenschappers ontwerpen experimenten om te zoeken naar oorzaak-en-gevolg relaties; waar veranderingen in één ding een voorspelbare verandering in iets anders kunnen veroorzaken. Deze
Hoofdlijnen
- Waarom is de vorm van plantencellen belangrijk?
- Hebben bomen celwanden in hun cellen?
- Bacter die hun eigen voedsel synthetiseert van koolstofdioxide en water in aanwezigheid van licht genoemd?
- Welk type cellen bevat 23 enkele chromosomen?
- Elite prestatiepaarden zijn topsporters. Hoe je ze ethisch kunt trainen
- Hoe beïnvloeden bacterie en virussen het lichaam?
- Hoe ver ben je van de boom gevallen? Wetenschappers schatten de mutatiesnelheid van chimpanseeouders tot hun nakomelingen
- Kun je een cel maken door moleculen in het laboratorium te combineren waarom of waarom niet?
- Het type levenscyclus dat in planten wordt gezien, wordt genoemd?
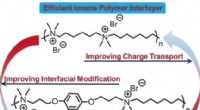
- Fullerenen overbruggen geleidende kloof in organische fotovoltaïsche energie
- Hoog rijden? Chemici zetten stappen richting marihuana-ademanalysator

- Krimp beheersen:nauwkeurige berekening en preventietips

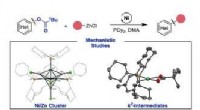
- Katalytische koppelingen begrijpen:niet alle synergieën zijn eenvoudig
- 3D-printen van zetmeel voor gepersonaliseerde medicijnontwikkeling

 Ontdekking van massaloze elektronen in materialen met faseverandering biedt volgende stap voor toekomstige elektronica
Ontdekking van massaloze elektronen in materialen met faseverandering biedt volgende stap voor toekomstige elektronica Nieuwe tool die Facebook-gegevens gebruikt, toont wereldwijde genderkloof
Nieuwe tool die Facebook-gegevens gebruikt, toont wereldwijde genderkloof Wat wordt er in actieve vulkanen gevonden?
Wat wordt er in actieve vulkanen gevonden?  Cellulaire ademhaling:hoe cellen gassen uitwisselen voor energie
Cellulaire ademhaling:hoe cellen gassen uitwisselen voor energie  Wat zijn de belangrijkste opdringerige functies gemaakt door Volcano?
Wat zijn de belangrijkste opdringerige functies gemaakt door Volcano?  Stadslandbouw bloeit in New York
Stadslandbouw bloeit in New York Wanneer kalium en zwavel reageren om sulfide een ionische verbinding te vormen, wat gebeurt er?
Wanneer kalium en zwavel reageren om sulfide een ionische verbinding te vormen, wat gebeurt er?  Welk een enkel object kan zowel tegelijkertijd water bevriezen als koken?
Welk een enkel object kan zowel tegelijkertijd water bevriezen als koken?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

