
Wetenschap
Hoe u het vriespunt van elke vloeistof kunt bepalen
Door Kevin Beck | Bijgewerkt op 24 maart 2022
Besjunior/iStock/GettyImages
Iedereen is getuige geweest van de transformatie van een vloeistof in vast ijs of omgekeerd. Begrijpen wanneer deze faseverandering plaatsvindt, is essentieel voor het dagelijks leven, van veilig autorijden in de winter tot koken en wetenschappelijke experimenten.
Wat zijn bevriezen en smelten?
De meeste stoffen bestaan in drie fasen:vast, vloeibaar of gasvormig, afhankelijk van temperatuur en druk. Water is uniek omdat het bij comfortabel lage temperaturen vast en vloeibaar kan zijn, en bij 100°C (212°F) in gas verandert, een temperatuur die voor de meeste mensen toegankelijk is. De overgang van vast naar vloeibaar wordt smelten genoemd; het tegenovergestelde, van vloeibaar naar vast, is bevriezen of verharding. Wanneer een vloeistof een gas wordt, is deze kokend , terwijl het omgekeerde proces condensatie is . In zeldzame gevallen kan een vaste stof de vloeibare fase omzeilen en direct in gas veranderen door middel van sublimatie , of een gas kan zich rechtstreeks op een vast oppervlak afzetten.
Wat beïnvloedt vries- en smeltpunten?
Het vriespunt van een stof hangt af van de moleculaire structuur ervan. Water heeft bijvoorbeeld een relatief hoog vriespunt van 0°C omdat de waterstofbruggen gemakkelijk aan elkaar ‘vergrendelen’, terwijl ethylalcohol (CH₃CH₂OH) bevriest bij –114°C (–174°F). Wanneer verschillende vloeistoffen worden gemengd of wanneer een vaste stof in een vloeistof wordt opgelost, verschuift het vriespunt van het resulterende mengsel voorspelbaar op basis van de betrokken componenten.
Opgeloste stoffen, oplosmiddelen en oplossingen
In een oplossing wordt de opgeloste vaste stof de opgeloste stof genoemd en de vloeistof die het draagt is het oplosmiddel . Het toevoegen van een opgeloste stof verlaagt het vriespunt van het oplosmiddel, een fenomeen dat bekend staat als vriespuntverlaging , een klassieke colligatieve eigenschap . Het effect hangt af van het aantal deeltjes dat door de opgeloste stof wordt geproduceerd, en niet van de chemische identiteit ervan.
Vriespunt van NaCl-oplossing
Keukenzout (natriumchloride) lost op in water en verlaagt het vriespunt. Daarom verspreiden wegploegen in de winter zout om het ijs te laten smelten. NaCl valt uiteen in twee ionen (Na⁺ en Cl⁻), dus elke mol zout levert twee deeltjes op die het vriespunt verlagen. Een opgeloste stof die meer deeltjes per formule-eenheid produceert, zou het vriespunt nog verder verlagen.
Vriespuntcalculator
Gebruik een online vriespuntcalculator om de temperaturen van gewone vloeistoffen in Celsius, Fahrenheit en Kelvin op te zoeken. Het vergelijken van de vriespunten van verschillende stoffen kan patronen onthullen die verband houden met hun moleculaire structuren.
 Welke producten zijn gelijk aan soda -as?
Welke producten zijn gelijk aan soda -as?  Oplosbaarheid in ammoniak:chemische eigenschappen begrijpen
Oplosbaarheid in ammoniak:chemische eigenschappen begrijpen  De verbrandingswarmte van paraffine Wax
De verbrandingswarmte van paraffine Wax Begrijpen hoe de monomeersequentie de geleiding in 'moleculaire draden' beïnvloedt
Begrijpen hoe de monomeersequentie de geleiding in 'moleculaire draden' beïnvloedt  Inzicht in de ferro-elektrische eigenschappen van relaxor kan tot veel vooruitgang leiden
Inzicht in de ferro-elektrische eigenschappen van relaxor kan tot veel vooruitgang leiden
 Projecties van Antarctisch ijsverlies en wereldwijde zeespiegelstijging verfijnen
Projecties van Antarctisch ijsverlies en wereldwijde zeespiegelstijging verfijnen Klimaat van Wetland Swamp Ecosystems
Klimaat van Wetland Swamp Ecosystems  Verschillen tussen noord- en zuidflank
Verschillen tussen noord- en zuidflank Een miljoen vroegtijdige sterfgevallen als gevolg van luchtvervuiling door ozon
Een miljoen vroegtijdige sterfgevallen als gevolg van luchtvervuiling door ozon Uit onderzoek blijkt dat federalisme nog steeds effectief is tegen potentiële sterke mannen zoals Trump
Uit onderzoek blijkt dat federalisme nog steeds effectief is tegen potentiële sterke mannen zoals Trump
Hoofdlijnen
- Wat is over reproductie?
- Is RNA een voorbeeld van koolstofdioxide?
- Wat gebeurt er in plantencellen tijdens fotosynthese?
- Wat voor soort hormoon is glucagon?
- Hoe de genetische blauwdrukken voor ledematen van vissen kwamen
- Wat is moleculaire gastronomie?
- Bevroren bezittingen:wie krijgt de embryo’s als een koppel uit elkaar gaat?
- Welke twee groepen bacteriën kunnen worden onderscheiden met de catalasetest?
- Zijn mensen geëvolueerd uit apen? Menselijke evolutie uitgelegd
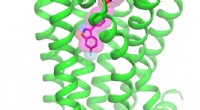
- Moleculaire geheimen onthuld:antipsychoticum gedokt in zijn receptor
- Hoe metalen samenwerken om sterke stikstof-stikstofbindingen te verzwakken
- Nieuwe melkzuurbacteriën zorgen voor natuurlijke zoetheid in yoghurt

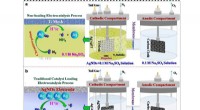
- Nieuw elektrokatalysesysteem realiseert elektrosynthese van ammoniak in de omgeving
- Nieuwe test identificeert giftige paddenstoelen

 Wat zijn de juiste hemelvaart en declinatie van Star Procyon?
Wat zijn de juiste hemelvaart en declinatie van Star Procyon?  Feiten over Cirrostratus Clouds
Feiten over Cirrostratus Clouds  Is er een psychologische reden waarom mensen gemeen zijn op internet?
Is er een psychologische reden waarom mensen gemeen zijn op internet?  Wat is de totale hoeveelheid kinetische energie in deeltjes van een object?
Wat is de totale hoeveelheid kinetische energie in deeltjes van een object?  Voorbeelden van aaltjes
Voorbeelden van aaltjes  Waarom geleiden verbindingen geen elektriciteit als ze vast zijn, maar kunnen ze wel smelten?
Waarom geleiden verbindingen geen elektriciteit als ze vast zijn, maar kunnen ze wel smelten?  Onderzoek naar plantenchemie onderzoekt trends in vergroening
Onderzoek naar plantenchemie onderzoekt trends in vergroening Sociale media zijn niet allemaal slecht - het redt levens in rampgebieden
Sociale media zijn niet allemaal slecht - het redt levens in rampgebieden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

