
Wetenschap
Bufferoplossingen berekenen:een stapsgewijze handleiding
Door Robert Schrader Bijgewerkt op 24 maart 2022
In de scheikunde is een "buffer" een oplossing die je aan een andere oplossing toevoegt om de pH, de relatieve zuurgraad of de alkaliteit ervan in evenwicht te brengen. Je maakt een buffer met respectievelijk een "zwak" zuur of een "zwakke" base en zijn "geconjugeerde" base of zuur. Om de pH van een buffer te bepalen (of uit de pH de concentratie van een van de componenten ervan te extrapoleren) kun je een reeks berekeningen maken op basis van de Henderson-Hasselbalch-vergelijking, ook wel de 'buffervergelijking' genoemd.
Stap 1
Gebruik de buffervergelijking om de pH van een zure bufferoplossing te bepalen, gegeven bepaalde zuur-base-concentraties. De Henderson-Hasselbalch-vergelijking is als volgt:pH =pKa + log ([A-]/[HA]), waarbij "pKa" de dissociatieconstante is, een getal dat uniek is voor elk zuur, "[A-]" de concentratie van de geconjugeerde base in mol per liter (M) vertegenwoordigt en "[HA]" de concentratie van het zuur zelf vertegenwoordigt. Beschouw bijvoorbeeld een buffer die 2,3 M koolzuur (H2CO3) combineert met 0,78 M waterstofcarbonaation (HCO3-). Raadpleeg een pKa-tabel om te zien dat koolzuur een pKa van 6,37 heeft. Als je deze waarden in de vergelijking stopt, zie je dat pH =6,37 + log (.78/2.3) =6,37 + log (.339) =6,37 + (-0,470) =5,9.
Stap 2
Bereken de pH van een alkalische (of basische) bufferoplossing. Je kunt de Henderson-Hasselbalch-vergelijking voor basen herschrijven:pOH =pKb + log ([B+]/[BOH]), waarbij "pKb" de dissociatieconstante van de base is, "[B+]" staat voor de concentratie van het geconjugeerde zuur van een base en "[BOH]" de concentratie van de base is. Overweeg een buffer die 4,0 M ammoniak (NH3) combineert met 1,3 M ammoniumion (NH4+). Raadpleeg een pKb-tabel om de pKb van ammoniak te vinden, 4,75. Bepaal met behulp van de buffervergelijking dat pOH =4,75 + log (1,3/4,0) =4,75 + log (.325) =4,75 + (-.488) =4,6. Onthoud dat pOH =14 – pH, dus pH =14 -pOH =14 – 4,6 =9,4.
Stap 3
Bepaal de concentratie van een zwak zuur (of zijn geconjugeerde base), gegeven de pH, pKa en de concentratie van het zwakke zuur (of zijn geconjugeerde base). Houd er rekening mee dat u een "quotiënt" van logaritmen kunt herschrijven, d.w.z. log (x/y) – als log x – log y, herschrijf de Henderson Hasselbalch-vergelijking als pH =pKa + log [A-] – log [HA]. Als je een koolzuurbuffer hebt met een pH van 6,2 waarvan je weet dat deze gemaakt is met 1,37 M waterstofcarbonaat, bereken dan de [HA] ervan als volgt:6,2 =6,37 + log(1,37) – log[HA] =6,37 + 0,137 – log[HA]. Met andere woorden log[HA] =6,37 – 6,2 + .137 =.307. Bereken [HA] door de "inverse log" (10^x op uw rekenmachine) van .307 te nemen. De concentratie koolzuur bedraagt dus 2,03 M.
Stap 4
Bereken de concentratie van een zwakke base (of zijn geconjugeerde zuur), gegeven de pH, pKb en de concentratie van het zwakke zuur (of zijn geconjugeerde base). Bepaal de concentratie ammoniak in een ammoniakbuffer met een pH van 10,1 en een ammoniumionenconcentratie van 0,98 M, waarbij je er rekening mee houdt dat de Henderson Hasselbalch-vergelijking ook werkt voor basen, zolang je maar pOH gebruikt in plaats van pH. Converteer uw pH als volgt naar pOH:pOH =14 – pH =14 – 10,1 =3,9. Voer vervolgens uw waarden als volgt in voor de alkalische buffervergelijking "pOH =pKb + log[B+] – log [BOH]":3,9 =4,75 + log[.98] – log[BOH] =4,75 + (-0,009) – log[BOH]. Aangezien log[BOH] =4,75 – 3,9 – .009 =.841, is de ammoniakconcentratie de inverse log (10^x) of .841, oftewel 6,93 M.
Dingen die nodig zijn
- Wetenschappelijke rekenmachine
- pKa-tabel
TL;DR (te lang; niet gelezen)
Mogelijk ziet u twee waarden voor koolzuur als u uw pKa-tabel raadpleegt. Dit komt omdat H2CO3 twee waterstofatomen heeft – en dus twee ‘protonen’ – en tweemaal kan dissociëren, volgens de vergelijkingen H2CO3 + H2O –> HCO3 – + H3O + en HCO3 – + H2O –> CO3 (2-) + H3O. Voor de berekening hoeft u alleen rekening te houden met de eerste waarde.
 Onderzoekers krijgen nieuwe inzichten in een dynamisch eiwit gericht op kankertherapie
Onderzoekers krijgen nieuwe inzichten in een dynamisch eiwit gericht op kankertherapie Waarom vereisen sommige materialen geen te gebruiken snijvloeistoffen?
Waarom vereisen sommige materialen geen te gebruiken snijvloeistoffen?  Oxidatietoestanden van reacties tussen kaliumoxide en koolstofdioxide?
Oxidatietoestanden van reacties tussen kaliumoxide en koolstofdioxide?  Klei gebruiken om eeuwige gifstoffen te bestrijden:wetenschappers verduidelijken de basis voor een innovatief PFAS-filter gemaakt van klei
Klei gebruiken om eeuwige gifstoffen te bestrijden:wetenschappers verduidelijken de basis voor een innovatief PFAS-filter gemaakt van klei  Wat is een instabiel atoom?
Wat is een instabiel atoom?
 De vervuiling van Italië overtreedt voortdurend EU-wetgeving:rechtbank
De vervuiling van Italië overtreedt voortdurend EU-wetgeving:rechtbank Wetenschappers verzamelen bijna twee decennia van gletsjerijsverlies wereldwijd
Wetenschappers verzamelen bijna twee decennia van gletsjerijsverlies wereldwijd Gone to hell:de strijd om het oudste meer van Europa te redden
Gone to hell:de strijd om het oudste meer van Europa te redden Terwijl 2 stormen de Golfkust bedreigen, bewoners zetten zich schrap voor zondvloed
Terwijl 2 stormen de Golfkust bedreigen, bewoners zetten zich schrap voor zondvloed Wat verklaart een patroon dat in de natuur wordt gevonden?
Wat verklaart een patroon dat in de natuur wordt gevonden?
Hoofdlijnen
- Onderzoekers bestuderen het suikeropnamemechanisme van industrieel micro-organisme
- Wat is een weefsel dat luchtpassages lijnen?
- Wat zijn isostopes?
- Dichte vloeistofdruppels fungeren als mobiele computers
- Wat is de naam van suikermolecule in DNA -necleotiden?
- Hoe komt stikstof uit organismen terug in de atmosfeer?
- Nieuw model suggereert hoe de hersenen in balans kunnen blijven
- Extra Y-chromosoom bij mannen
- Tardigrades:de ultieme overlevenden van aarde en ruimte
- Nieuwe hulpmiddelen om bioactieve lipiden te bestuderen

- De biologisch afbreekbare batterij die in 3D is geprint, wegwerp en gemaakt van papier

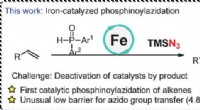
- PcFe-gekatalyseerde radicale fosfinoylazidatie van alkenen met een snelle azido-overdrachtsstap
- Een goede zaak beter maken:een zuurtest die niet in water verdrinkt
- Oleo Sponge succesvol in echte omstandigheden voor de kust van Californië

 Gaming grafische kaart zorgt voor snellere, nauwkeurigere controle van fusie-energie-experimenten
Gaming grafische kaart zorgt voor snellere, nauwkeurigere controle van fusie-energie-experimenten Fossiel van dinosaurussen worden gevonden in Krijt Rock maar geen tertiaire rots?
Fossiel van dinosaurussen worden gevonden in Krijt Rock maar geen tertiaire rots?  Wat is opwaartse verplaatsing van gas?
Wat is opwaartse verplaatsing van gas?  Wat is het grote verschil tussen biomen?
Wat is het grote verschil tussen biomen?  Zijn voertuigen ontworpen met zowel plastic als elastische waarden om energie te absorberen?
Zijn voertuigen ontworpen met zowel plastic als elastische waarden om energie te absorberen?  NASA ziet de wedergeboorte van de tropische depressie Harveys
NASA ziet de wedergeboorte van de tropische depressie Harveys Kunnen mini-Neptunussen bestraalde oceaanplaneten zijn?
Kunnen mini-Neptunussen bestraalde oceaanplaneten zijn?  Sid the Science Kid je bent wind?
Sid the Science Kid je bent wind?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

