
Wetenschap
Oplossingsmolariteit stimuleren:bewezen technieken en praktische tips
Door Matthew Perdue Bijgewerkt op 24 maart 2022
Een oplossing is een mengsel van twee delen:een opgeloste stof en een oplosmiddel. De opgeloste stof is het opgeloste deeltje in de oplossing en het oplosmiddel is het deel dat de opgeloste stof oplost. Zout water is bijvoorbeeld een oplossing die bestaat uit natriumchloride, de opgeloste stof, opgelost in water, het oplosmiddel. Molariteit is een meting die wordt gebruikt om de hoeveelheid opgeloste stof, in mol, opgelost in een oplosmiddel per volume te identificeren en wordt uitgedrukt als mol per liter (mol/l). De molariteit is daarom direct evenredig met de hoeveelheid opgeloste stof in oplossing en indirect evenredig met het volume van de oplossing. Deze twee relaties kunnen worden gebruikt om te bepalen hoe de molariteit van een oplossing kan worden verhoogd.
De molariteit verhogen met volume
Stap 1
Bepaal het aantal mol opgeloste stof in een bepaalde oplossing door het aantal gram opgeloste stof te delen door de molecuulmassa. Een zoutwateroplossing die 5 gram natriumchloride bevat, zou bijvoorbeeld 0,18 mol bevatten, zoals bepaald door de hoeveelheid opgeloste stof, in grammen, te delen door de molecuulmassa (5 g / 28 g/mol =0,18 mol opgeloste stof).
Stap 2
Doe de oplossing in een maatbeker en identificeer het volume van de oplossing. Bij de meeste bekers zijn de afmetingen aangegeven in milliliter. Omdat de molariteit in liters wordt weergegeven, moet het volume in milliliters worden omgerekend naar liters door vermenigvuldiging met de conversiefactor van 1 l/1000 ml. Als we het zoutwatervoorbeeld gebruiken, zou een gemeten volume van 150 ml gelijk zijn aan 0,15 l met behulp van de conversiefactor:150 ml x (1 l / 1000 ml) =0,15 l.
Stap 3
Identificeer de molariteit (M) van de oplossing op basis van het berekende aantal mol opgeloste stof en het waargenomen volume in milliliter. De molariteit van de zoutwateroplossing zou 0,18 mol opgeloste stof per 0,15 L zijn, of 1,2 M omdat 0,18 mol / 0,15 L =1,2 mol/L.
Stap 4
Bepaal de volumeverandering die nodig is om de molariteit tot een gespecificeerde waarde te verhogen met behulp van de vergelijking M1 x V1 =M2 x V2, waarbij M1 en M2 respectievelijk de initiële en nieuwe molariteiten zijn en V1 en V2 de initiële en uiteindelijke volumes. Het verdubbelen van de molariteit van de voorbeeldzoutwateroplossing van 1,2 naar 2,4 zou een nieuw volume van 0,08 L vereisen, zoals bepaald door het oplossen van V2 in de vergelijking 1,2 M x 0,15 L =2,4 M x V2.
Stap 5
Maak de nieuwe oplossing met dezelfde hoeveelheid opgeloste stof en het nieuw berekende volume oplosmiddel. De nieuwe zoutwateroplossing zou nog steeds 5 g natriumchloride bevatten, maar slechts 0,075 l of 75 ml water, wat zou resulteren in een nieuwe oplossing met een molariteit van 2,4. Daarom resulteert een afname van het volume van een oplossing met dezelfde hoeveelheid opgeloste stof in een toename van de molariteit.
Verhoog de molariteit met opgeloste stof
Stap 1
Bepaal de molariteit van een bepaalde oplossing volgens stap 1 tot en met 3 in de vorige sectie.
Stap 2
Identificeer de gewenste toename in molariteit voor de oplossing. Stel bijvoorbeeld dat een initiële oplossing van 1,2 M zout water moet worden verhoogd tot een oplossing van 2,4 M met hetzelfde volume.
Stap 3
Bepaal hoeveel opgeloste stof aan de oplossing moet worden toegevoegd om de molariteit tot de opgegeven waarde te verhogen. Een oplossing van 2,4 M zou 2,4 mol per liter bevatten en de oplossing bevat 0,15 l. De hoeveelheid opgeloste stof, in mol, van de nieuwe oplossing wordt vervolgens geïdentificeerd door een verhouding in te stellen die wordt gegeven als 2,4 mol/1 l =x mol/0,15 l en op te lossen voor de onbekende x-waarde. Deze berekening identificeert een waarde van 0,36 mol natriumchloride die nodig is voor de nieuwe oplossing. Vermenigvuldigen met de molecuulmassa van natriumchloride (28 g/mol) geeft dan de benodigde hoeveelheid in gram opgeloste stof als 10,1 g.
Stap 4
Trek de initiële hoeveelheid opgeloste stof af van de nieuw berekende hoeveelheid om de hoeveelheid opgeloste stof te bepalen die moet worden toegevoegd om de molariteit te verhogen. Om een 1,2 M zoutwateroplossing met 5 gram natriumchloride te verhogen tot een 2,4 M oplossing is de toevoeging van 5,1 gram natriumchloride nodig, zoals bepaald door de initiële hoeveelheid van 5 g af te trekken van de nieuw vereiste hoeveelheid van 10,1 g. Daarom zou het toevoegen van 5,1 g natriumchloride aan een 1,2 M zoutwateroplossing de molariteit verhogen tot 2,4 M.
Dingen die nodig zijn
- Gegradueerde beker
- Periodiek systeem
- Rekenmachine
- Natriumchloride
- Water
 Wat is de volledige vergelijking wanneer alum Kalso42.12H2O reageert met bariumchloride BACL2?
Wat is de volledige vergelijking wanneer alum Kalso42.12H2O reageert met bariumchloride BACL2?  De stijfste poreuze lichtgewicht materialen ooit
De stijfste poreuze lichtgewicht materialen ooit PPM omzetten naar NTU:een stapsgewijze kalibratiegids
PPM omzetten naar NTU:een stapsgewijze kalibratiegids  Neutralisatiereacties:beperkingen en overwegingen
Neutralisatiereacties:beperkingen en overwegingen  Waar komt de positron die tijdens de emissie wordt geproduceerd vandaan?
Waar komt de positron die tijdens de emissie wordt geproduceerd vandaan?
 Uit welke gassen bestaat de lucht die we inademen?
Uit welke gassen bestaat de lucht die we inademen?  Lijst geërfde eigenschappen van een plant in het regenwoud?
Lijst geërfde eigenschappen van een plant in het regenwoud?  Bosbranden gekoppeld aan tienduizenden vermijdbare sterfgevallen
Bosbranden gekoppeld aan tienduizenden vermijdbare sterfgevallen Effecten op millenniumschaal van menselijke verstoringen op tropische bossen
Effecten op millenniumschaal van menselijke verstoringen op tropische bossen Heeft klimaatverandering invloed op de vastgoedprijzen? Alleen als je erin gelooft
Heeft klimaatverandering invloed op de vastgoedprijzen? Alleen als je erin gelooft
Hoofdlijnen
- Wat geloofden de meeste mensen over genetica vóór Gregor Mendel en onderzoek?
- Wat is een voorbeeld van open populatie in de wetenschap?
- Is hangry een echte emotie?
- Hoe de cholerabacterie waterroofdieren overleeft
- Onderzoekers ontdekken een manier om in eiwitten te kijken en te zien hoe ze in elkaar zitten
- Wat is een computersoftwareprogramma dat bestaat uit cellen met rijen en colums?
- Kunnen ziektedetecterende honden de dikhoornschapen in South Dakota helpen redden?
- Wat is de dominante generatie van bryophytes?
- Wat is de belangrijkste van plantenfysiologie in de landbouw?
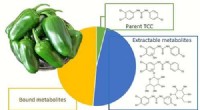
- Peperplant zuigt antibioticum voor persoonlijke verzorging op
- Onderzoek naar oxidatieve routes in nucleaire brandstof

- Wetenschappers betrappen planten terwijl ze de chemie veranderen, waarvan gedacht wordt dat ze onveranderlijk zijn omdat ze noodzakelijk zijn voor het leven

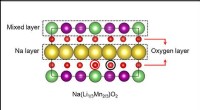
- Nieuw materiaal kan helpen de batterijkosten voor elektrische auto's te verlagen, telefoons
- Papavers analyseren om betere medicijnen te maken

 Waarom straalt een zwarte radiator meer warmte uit dan een witte?
Waarom straalt een zwarte radiator meer warmte uit dan een witte?  Wat is sterke wind?
Wat is sterke wind?  Waarom March Madness een bijzondere tijd van het jaar is voor de staatsbegrotingen
Waarom March Madness een bijzondere tijd van het jaar is voor de staatsbegrotingen  Welke twee dingen hebben Galileo bijgedragen aan de moderne wetenschap?
Welke twee dingen hebben Galileo bijgedragen aan de moderne wetenschap?  Klimaatakkoord:wat de wetenschappers zeggen
Klimaatakkoord:wat de wetenschappers zeggen  Wat is maximale toegepaste kracht?
Wat is maximale toegepaste kracht?  Bepaalt het geotropisme de groeirichting?
Bepaalt het geotropisme de groeirichting?  Welke fundamentele natuurkracht is verantwoordelijk om u op het aardse oppervlak te houden?
Welke fundamentele natuurkracht is verantwoordelijk om u op het aardse oppervlak te houden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

