
Wetenschap
De magnesiumoxidevergelijking in evenwicht brengen:een stapsgewijze handleiding
Door Caroline Depalma, bijgewerkt op 24 maart 2022
Hemera Technologies/PhotoObjects.net/Getty Images
Het in evenwicht brengen van chemische vergelijkingen is een fundamentele vaardigheid in de scheikunde, die ervoor zorgt dat de wet van behoud van massa geldt. In deze beknopte handleiding bespreken we het eenvoudigste voorbeeld:het vormen van magnesiumoxide (MgO) uit magnesium (Mg) en zuurstofgas (O2 ). De stappen zijn bedoeld om duidelijk te zijn voor studenten, docenten en iedereen die geïnteresseerd is in het versterken van hun begrip van stoichiometrie en ionische binding.
Stap 1:Identificeer reagentia en producten
Schrijf de ongebalanceerde vergelijking:
Mg + O2 → MgO
Stap 2:Tel atomen aan elke kant
Aan de linkerkant heb je 1 Mg-atoom en 2 O-atomen (aangezien O2 is diatomisch). Aan de rechterkant heb je 1 Mg- en 1 O-atoom.
Stap 3:Ionische bindingsprincipes toepassen
Magnesium (een metaal uit groep 2) vormt doorgaans een 2+ ion, terwijl zuurstof (een niet-metaal uit groep 16) twee elektronen accepteert om een 2− ion te vormen. De resulterende formule, MgO, weerspiegelt deze 1:1-verhouding van Mg²⁺ tot O²⁻.
Stap 4:Breng de vergelijking in evenwicht
Om het zuurstofaantal te evenaren, plaatst u een coëfficiënt van 2 vóór magnesium aan de kant van de reactanten en een coëfficiënt van 2 vóór MgO aan de productzijde:
2 mg + O2 → 2 MgO
Dingen die je nodig hebt
- Periodiek systeem (om oxidatietoestanden te bevestigen)
- Basiskennis van ionische binding
- Potlood en papier (of een digitale notitie-app)
TL;DR
Voor ionische verbindingen weerspiegelt de verhouding van de elementen vaak hun typische ladingen. Hier koppelt Mg (2+) zich aan O (2−) om MgO te vormen, dus je verdubbelt simpelweg de magnesiumcoëfficiënt om de zuurstof in evenwicht te brengen.
Belangrijke opmerking
Hoewel dit voorbeeld duidelijk is, kunnen bij reacties in de echte wereld meerdere reactanten, producten of omkeerbare processen betrokken zijn. Controleer altijd uw specifieke context en raadpleeg bij twijfel uw instructeur of een betrouwbare scheikundige hulpbron.
Referentie
- Tro, Nivaldo. Chemie:een moleculaire benadering , 2007.
 Wat betekent het woord experiment?
Wat betekent het woord experiment?  Nieuwe kaarten van Maleisisch Borneo onthullen verslechterende koolstofverliezen langs bosranden
Nieuwe kaarten van Maleisisch Borneo onthullen verslechterende koolstofverliezen langs bosranden Waarom heeft het milieu water nodig?
Waarom heeft het milieu water nodig?  Door de brandoperaties voorgeschreven brandcombo vermindert de ernst van de natuurbrand tot 72%
Door de brandoperaties voorgeschreven brandcombo vermindert de ernst van de natuurbrand tot 72% VN waarschuwt dat impact van Caribische vulkaan andere eilanden kan treffen
VN waarschuwt dat impact van Caribische vulkaan andere eilanden kan treffen
Hoofdlijnen
- Hoe genereer je een hypothese?
- Hoe worden een waarneembare eigenschappen genoemd?
- Hoe is het menselijk skelet zoals plantenstam?
- Waarom zijn er zo weinig vissen in de oceanen van de aarde?
- Uit herbebossingsonderzoek blijkt dat slechts enkele boomsoorten een eeuw van snelle klimaatverandering kunnen overleven
- Hersenonderzoek:Zingende muizen vertonen tekenen van leren
- Wat betekent fenomologie?
- Wat zijn twee detritivoren van het Taiga Biome?
- De impact van biotechnologie op het dagelijks leven:voedsel, gezondheid en meer
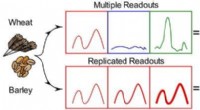
- Een stap in de richting van een gevoelige en snelle glutendetectie
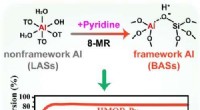
- Dynamische evolutie van aluminiumcoördinatieomgevingen in mordenietzeoliet
- pH berekenen op basis van pKa:een praktische gids

- Protonen, neutronen en elektronen:hun ladingen uitgelegd

- Electrospun vezels weven nieuwe medische innovaties

 Wat is een constante kracht F uitgeoefend op een object met massa M?
Wat is een constante kracht F uitgeoefend op een object met massa M?  Jeff Bezos wil de zware industrie naar de ruimte verplaatsen
Jeff Bezos wil de zware industrie naar de ruimte verplaatsen  Hoe het ontwerpen van een AV-veiligheidsmodel betere veiligheidsoplossingen mogelijk maakte voor menselijke bestuurders
Hoe het ontwerpen van een AV-veiligheidsmodel betere veiligheidsoplossingen mogelijk maakte voor menselijke bestuurders Hoe heet een slapende bacterie?
Hoe heet een slapende bacterie?  Waarom de eerste Amerikaanse regels voor openbaarmaking van het klimaat veel zwakker zijn dan gepland en wat ze betekenen voor bedrijven
Waarom de eerste Amerikaanse regels voor openbaarmaking van het klimaat veel zwakker zijn dan gepland en wat ze betekenen voor bedrijven  Hoe beschrijft u de Fromation of Natural Levee?
Hoe beschrijft u de Fromation of Natural Levee?  RPD berekenen
RPD berekenen  Wat zit er in het midden van Saturnus?
Wat zit er in het midden van Saturnus?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

