
Wetenschap
pH berekenen op basis van pKa:een praktische gids
Sinhyu/iStock/GettyImages
Als je aan zuren denkt (azijn, bleekmiddel of zelfs de zuurte van citroenzuur), dan heb je te maken met de pH-schaal, het hulpmiddel dat de zuurgraad in waterige oplossingen kwantificeert. Begrijpen hoe je de intrinsieke zuurgraad van een stof kunt vertalen (de zuurdissociatieconstante (Ka) ) omzetten in een meetbare pH-waarde is essentieel voor scheikundigen, docenten en iedereen die met zuren werkt.
Zuren in oplossing
In water doneert een zuur een proton (H⁺) en wordt het een anion. Het vrijgekomen proton associeert zich met een watermolecuul en vormt het hydroniumion (H₃O⁺). Het oorspronkelijke zuur wordt zijn geconjugeerde base. Koolzuur (H₂CO₃) dissocieert bijvoorbeeld in H₃O⁺ en bicarbonaat (HCO₃⁻).
Sterke zuren zoals zoutzuur (HCl) geven gemakkelijk protonen af, zelfs in reeds zure media, terwijl zwakke zuren alleen merkbaar ioniseren als de omringende protonconcentratie laag is (dat wil zeggen bij een hogere pH).
De pH-schaal
De pH-schaal is logaritmisch, variërend van ongeveer 1 (zeer zuur) tot 14 (zeer basisch). Het wordt gedefinieerd door:
\(\text{pH} =-\log_{10}[\text{H}^+]\)
waarbij \([\text{H}^+]\) de molaire concentratie van vrije protonen is. Elke tienvoudige toename van de protonconcentratie verlaagt de pH met één eenheid.
Voorbeeld: Een protonoplossing van 0,025 M heeft
\(\text{pH} =-\log_{10}(0,025) =1,602\)
De zuurionisatieconstante (Ka)
Ka kwantificeert de neiging van een zuur om te dissociëren:
\(K_a =\dfrac{[A^-][\text{H}_3\text{O}^+]}{[HA]}\)
Hogere Ka-waarden duiden op sterkere zuren, wat een volledigere dissociatie bij evenwicht betekent.
Van Ka naar pKa
Door de negatieve logaritme van Ka te nemen, verkrijgen we de pKa van het zuur:
\(\text{pKa} =-\log_{10}K_a\)
De pH berekenen met behulp van de Henderson-Hasselbalch-vergelijking
De Henderson-Hasselbalch-vergelijking koppelt pH, pKa en de verhouding van geconjugeerde base tot zuur:
\(\text{pH} =\text{pKa} + \log_{10}\dfrac{[A^-]}{[HA]}\)
Deze relatie is vooral nuttig voor bufferoplossingen, waar zowel het zuur als de geconjugeerde base aanwezig zijn.
Voorbeeld: Azijnzuur (CH₃COOH) heeft \(K_a =1,77 \maal 10^{-5}\). Als slechts 10% van het zuur wordt gedissocieerd, dan is \([A^-]/[HA] =0,1\). Bereken eerst de pKa:
\(\text{pKa} =-\log_{10}(1,77 \times 10^{-5}) =4,75\)
Pas dan Henderson–Hasselbalch toe:
\(\text{pH} =4,75 + \log_{10}(0,1) =4,75 - 1 =3,75\)
Bij een pH gelijk aan de pKa zijn de concentraties van het zuur en de geconjugeerde base gelijk, wat betekent dat 50% van het zuur wordt gedissocieerd.
Deze vergelijkingen bieden een eenvoudige methode om de pH te voorspellen van elke oplossing waarvan de Ka en de concentratie van het zuur bekend zijn.
Belangrijkste punten
• De pH-schaal meet de protonconcentratie op een logaritmische schaal.
• Ka drukt de dissociatieneiging van een zuur uit; pKa is de logaritmische tegenhanger.
• De Henderson-Hasselbalch-vergelijking overbrugt pH, pKa en de zuur/base-verhouding, waardoor nauwkeurige pH-berekeningen voor buffers en zwakke zuren mogelijk zijn.
 Een bepaalde massa koolstof reageert met 13,6 g zuurstof om monoxide te vormen Welke hoeveelheid gram zou hetzelfde dioxide reageren?
Een bepaalde massa koolstof reageert met 13,6 g zuurstof om monoxide te vormen Welke hoeveelheid gram zou hetzelfde dioxide reageren?  Wat is de chemische verbinding in vuil?
Wat is de chemische verbinding in vuil?  Microscopie laat zien hoe atoomhoge stappen de oxidatie van metaaloppervlakken belemmeren
Microscopie laat zien hoe atoomhoge stappen de oxidatie van metaaloppervlakken belemmeren  Permanganaattitraties in zure oplossingen:waarom en hoe
Permanganaattitraties in zure oplossingen:waarom en hoe  Wat is een vloeistof die wordt gebruikt om andere stoffen op te lossen?
Wat is een vloeistof die wordt gebruikt om andere stoffen op te lossen?
 Brandonderzoek onthult hoe land, codevariaties hebben invloed op de ontsnappingstijd
Brandonderzoek onthult hoe land, codevariaties hebben invloed op de ontsnappingstijd Onderzoekers gaan koekoek over Antarctische pinguïnpoep
Onderzoekers gaan koekoek over Antarctische pinguïnpoep Wat zijn de verschillende soorten ecologische relaties?
Wat zijn de verschillende soorten ecologische relaties?  China auto dilemma:Peking wil elektrisch, kopers willen SUV's
China auto dilemma:Peking wil elektrisch, kopers willen SUV's Arctisch zee-ijsverlies heeft minimale invloed op extreem koud winterweer, uit onderzoek blijkt
Arctisch zee-ijsverlies heeft minimale invloed op extreem koud winterweer, uit onderzoek blijkt
Hoofdlijnen
- Hoe heet het organisme dat energie haalt uit voedsel dat het eet?
- Wat bevindt zich buiten het kernmembraan en plaats vele chemische reacties?
- Welk type cel maakt pus wat het sterft?
- Wat zijn etercellen?
- Wat beweegt osmose door het celmembraan?
- Wat zijn de bulbouretherale klieren?
- Jonge, koelbloedige dieren lijden het meest door de opwarming van de aarde, blijkt uit onderzoek
- Hoe ondersteunt biochemisch bewijs de evolutie?
- Wat is het type RNA dat tijdens translatie omgezet in een eiwit?
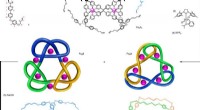
- Onderzoekers creëren de meest verwarde, in elkaar grijpende molecule ooit
- Wetenschappers ontdekken dat watermicrodruppels kunnen veranderen in waterstofperoxide wanneer ze condenseren op koude oppervlakken

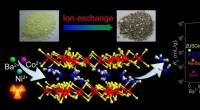
- Selectieve afvang van ionen uit afvalwater met gelaagd metaalsulfide
- Wetenschappers hebben eetbare films gemaakt voor voedselverpakkingen

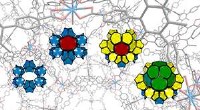
- Twee eenvoudige bouwstenen produceren complex 3D-materiaal
 Afzijdige neutronen kunnen in feite kort met elkaar praten in een nieuw soort symmetrie
Afzijdige neutronen kunnen in feite kort met elkaar praten in een nieuw soort symmetrie Wetenschapsprojecten met neon en atomen
Wetenschapsprojecten met neon en atomen  Bepalen of een verbinding polair of niet-polair is:een praktische gids
Bepalen of een verbinding polair of niet-polair is:een praktische gids  E-waste-etend eiwit creëert zeldzame aardelementen
E-waste-etend eiwit creëert zeldzame aardelementen Hoe u zich kunt voorbereiden op een hyperactief orkaanseizoen
Hoe u zich kunt voorbereiden op een hyperactief orkaanseizoen  Wetenschappers vergelijken bodemmicroben in no-till, conventionele grondbewerkingssystemen van boerderijen in de Pacific Northwest
Wetenschappers vergelijken bodemmicroben in no-till, conventionele grondbewerkingssystemen van boerderijen in de Pacific Northwest Samenwerking na oogcontact:gender is belangrijk
Samenwerking na oogcontact:gender is belangrijk Reizen de voedingsstoffen door zuurstofarm bloed om de lichaamscel te bereiken?
Reizen de voedingsstoffen door zuurstofarm bloed om de lichaamscel te bereiken?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

