
Wetenschap
Waarom vormen atomen chemische bindingen? Een duidelijke, deskundige gids
Door Kevin Beck, bijgewerkt op 30 augustus 2022
In de scheikunde is de vorming van chemische bindingen een fundamenteel concept dat verklaart hoe atomen op elkaar inwerken om moleculen en verbindingen te creëren. Of je nu een student bent die de basisbeginselen doorneemt of een nieuwsgierige lezer bent, het begrijpen van de onderliggende redenen achter de vorming van bindingen geeft inzicht in het gedrag van materie.
Basisprincipes van het atoom
Atomen bestaan uit een kern die protonen en neutronen bevat, omgeven door elektronen die in gekwantiseerde energieniveaus ronddraaien. Waterstof is een speciaal geval, met één proton en één elektron. Voor neutrale atomen is het aantal protonen gelijk aan het aantal elektronen, wat de identiteit van het element definieert. Terwijl protonen en neutronen een vergelijkbare massa delen en zich in de kern bevinden, zijn elektronen grofweg 2000 keer lichter, waardoor ze vrij rond de kern kunnen bewegen.
Het zijn de buitenste elektronen – die in de valentieschil – die het chemische gedrag dicteren. Als deze schillen vol zijn, zijn atomen energetisch stabiel; anders zoeken ze stabiliteit door elektronen uit te wisselen of te delen.
Classificatie van chemische bindingen
Atomen kunnen op verschillende manieren met elkaar worden verbonden, elk gedreven door het doel om valentieschillen te voltooien:
- Covalente bindingen :Atomen delen een of meer elektronenparen. Een watermolecuul (H2 O) heeft twee identieke covalente H-O-bindingen die voldoen aan de valentie-eisen van waterstof en zuurstof.
- Ionische bindingen :Het ene atoom doneert elektronen terwijl het andere ze accepteert, waardoor tegengesteld geladen ionen ontstaan die elkaar aantrekken. Natriumchloride (NaCl) is hiervan een voorbeeld, waarbij natrium een elektron afstaat aan chloor.
- Metaalverbindingen :In metalen worden valentie-elektronen gedelokaliseerd, waardoor een ‘elektronenzee’ ontstaat die vrij door het rooster beweegt. Deze delokalisatie houdt rekening met eigenschappen zoals elektrische geleidbaarheid en maakbaarheid in zuivere metalen zoals goud en platina.
- Waterstofbruggen :Een speciale, zwakkere interactie waarbij een waterstofatoom dat covalent gebonden is aan een elektronegatief atoom (bijvoorbeeld zuurstof) een ander elektronegatief atoom aantrekt. Dit fenomeen is cruciaal in water en draagt bij aan het hoge kookpunt ervan in vergelijking met andere lichtmoleculen.
Waarom atomen volledige Valence Shells “willen”
Atomen worden inherent gedreven om hun potentiële energie te verlagen. Een gevulde valentieschil vertegenwoordigt een gesloten, energiezuinige configuratie die lijkt op de stabiliteit van de edelgassen. Wanneer elektronen worden gedeeld, gedoneerd of gedelokaliseerd, verminderen atomen de elektronenafstoting en bereiken ze een energetisch gunstigere toestand. Dit streven naar stabiliteit verklaart de universele neiging van atomen om bindingen te vormen.
 Wat voor soort mengsel is deeg die ik nodig heb, hulpvraag?
Wat voor soort mengsel is deeg die ik nodig heb, hulpvraag?  Waarom heeft zwaveldioxide een laag kookpunt?
Waarom heeft zwaveldioxide een laag kookpunt?  Hoe de hoeveelheid condensaat per hoeveelheid stoom te berekenen
Hoe de hoeveelheid condensaat per hoeveelheid stoom te berekenen Welke van deze paren elementen zou ionisch binden met chloor?
Welke van deze paren elementen zou ionisch binden met chloor?  Onderzoek toont aan dat stomerijvloeistof veelbelovend is voor duurzame organische synthese
Onderzoek toont aan dat stomerijvloeistof veelbelovend is voor duurzame organische synthese
 Is tropisch regenwoud biotisch of abiotisch?
Is tropisch regenwoud biotisch of abiotisch?  Welke niet -levende dingen leven in de rivier?
Welke niet -levende dingen leven in de rivier?  Hoe reageert Plant op licht?
Hoe reageert Plant op licht?  Pogingen om de in gevaar gebrachte Pando te herstellen, tonen belofte
Pogingen om de in gevaar gebrachte Pando te herstellen, tonen belofte Dood graag? De race om natuurfoto’s op sociale media kan ecosystemen verwoesten of tot snelle uitsterving leiden
Dood graag? De race om natuurfoto’s op sociale media kan ecosystemen verwoesten of tot snelle uitsterving leiden
Hoofdlijnen
- Genetische aanwijzingen over hoe honden de beste vrienden van de mens werden
- Wat zijn de namen van producten Cellulaire ademhaling?
- Het ontsluiten van de geheimen van hoe cellen communiceren biedt inzichten in de behandeling van ziekten
- Waarom wordt de afzonderlijke typenhypothese door de meeste biologen zo onwaarschijnlijk beschouwd?
- Wat is de wetenschappelijke naam voor een bodembacterie?
- Wat zijn alle organellen van een dierencel?
- Wat is het verschil van bacteriecellen van cellen van dieren en planten?
- Welke organel is geen gemeenschappelijke bestemming voor kleine blaasjes die het Golgi -apparaat van het Golgi -apparaat ontsnappen?
- Wat is de term voor een groep onderwerpen die alle variabelen ontvangt behalve onafhankelijke variabele in een experiment?
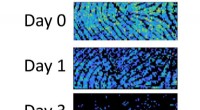
- Residuen in vingerafdrukken bevatten aanwijzingen voor hun leeftijd
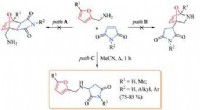
- Chemici identificeren de structuur van het middel dat mutaties veroorzaakt in embryo's van koraalduivels
- Nanofiltratiemembranen voor de behandeling van industrieel afvalwater van zware metalen

- Hoe suikerminnende microben toekomstige auto's van stroom kunnen voorzien

- Zeer efficiënte katalysator met één atoom kan de auto-industrie helpen

 Binaire ionische samengestelde naam voor CO2O3?
Binaire ionische samengestelde naam voor CO2O3?  Waarom zijn gekke wormen een potentieel probleem of uitdaging voor onze ecosystemen?
Waarom zijn gekke wormen een potentieel probleem of uitdaging voor onze ecosystemen?  Laserbehandeling toont potentieel voor vermindering van industriële chemische verwerking van voertuigen
Laserbehandeling toont potentieel voor vermindering van industriële chemische verwerking van voertuigen Wat is een voorbeeld van meercellige organismen?
Wat is een voorbeeld van meercellige organismen?  Wilt u 41 procent van de zeer bedreigde gewervelde planeten redden? Werken op eilanden
Wilt u 41 procent van de zeer bedreigde gewervelde planeten redden? Werken op eilanden Britse werknemersvertegenwoordigers hebben een lager vertrouwen in managers dan in enig ander EU-land, uit onderzoek blijkt
Britse werknemersvertegenwoordigers hebben een lager vertrouwen in managers dan in enig ander EU-land, uit onderzoek blijkt Wat zijn de nieuwste toepassingen van aardgas?
Wat zijn de nieuwste toepassingen van aardgas?  Waarom bevindt Hawaii zich niet op een plaatgrens?
Waarom bevindt Hawaii zich niet op een plaatgrens?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

