
Wetenschap
Elektronische geometrie versus moleculaire vorm:belangrijkste verschillen verklaard
Door Rosann Kozlowski Bijgewerkt op 30 augustus 2022
DragonImages/iStock/GettyImages
Elektronische geometrie en moleculaire vorm beschrijven hoe elektronen en atomen rond een centraal atoom in een driedimensionale ruimte zijn gepositioneerd, waardoor de vorm en bindingshoeken van het molecuul worden bepaald.
Definities:elektronische geometrie versus moleculaire vorm
Elektronische geometrie verwijst naar de rangschikking van elektronengroepen – zowel bindingsparen als alleenstaande paren – rond een centraal atoom. De moleculaire vorm beschrijft daarentegen alleen de ruimtelijke rangschikking van de gebonden atomen. Wanneer een molecuul geen alleenstaande paren bevat, vallen de twee concepten samen; anders vervormen alleenstaande paren de vorm.
VSEPR-theorie en zijn rol bij het voorspellen van geometrie
Het Valence-Shell Electron-Pair Repulsion (VSEPR)-model voorspelt de geometrie van een molecuul door de afstoting tussen elektronenparen te minimaliseren. Alleenstaande paren stoten sterker af dan bindingsparen, waardoor de bindingshoeken iets kleiner worden vergeleken met de ideale waarden voor een gegeven elektronische geometrie.
Elektronische geometrie op basis van het aantal elektronengroepen
- 2 groepen:lineair (180°)
- 3 groepen:trigonaal vlak (120°)
- 4 groepen:tetraëdrisch (109,5°)
- 5 groepen:trigonaal bipiramidaal (120°/90°)
- 6 groepen:achtvlakkig (90°)
Gemeenschappelijke vormen afgeleid van elke elektronische geometrie
Hieronder staan de typische moleculaire vormen die ontstaan wanneer alleenstaande paren de elektronengroepen bezetten. De vorm die als eerste voor elke geometrie wordt vermeld, is de enige waarbij de elektronische geometrie en de moleculaire vorm overeenkomen.
Lineair (2 groepen)
- Lineair – 180° (elektronengeometrie =moleculaire vorm)
Trigonaal vlak (3 groepen)
- Trigonaal vlak – 120° (geen alleenstaande paren)
- Gebogen – 2 verbindingen, 1 alleenstaand paar (verbindingshoek <120°)
Tetraëdrisch (4 groepen)
- Tetraëdrisch – 109,5° (geen alleenstaande paren)
- Trigonaal piramidaal – 3 bindingen, 1 vrijstaand paar (bindingshoek <109,5°)
- Gebogen – 2 bindingen, 2 losse paren (bindingshoek <109,5°)
Trigonaal bipyramidaal (5 groepen)
- Trigonaal bipiramidaal – 120°/90° (geen alleenstaande paren)
- Wip – 4 bindingen, 1 alleenstaand paar (eenzaam paar neemt de axiale positie in)
- T-vormig – 3 bindingen, 2 losse paren
- Lineair – 2 bindingen tegenover elkaar, 3 eenzame paren
Octahedraal (6 groepen)
- Octahedrisch – 90° (geen alleenstaande paren)
- Vierkant piramidaal – 5 bindingen, 1 alleenstaand paar (eenzaam paar neemt de axiale positie in)
- Vierkant vlak – 4 bindingen, 2 alleenstaande paren (alleenstaande paren bezetten axiale posities)
Dankzij deze relaties kunnen scheikundigen zowel de vorm van een molecuul als de bindingshoeken ervan voorspellen op basis van een eenvoudige telling van elektronenparen.
 Online game leert spelers hoe ze afval correct kunnen sorteren
Online game leert spelers hoe ze afval correct kunnen sorteren Wat is de zwaartekrachtattractie van appel op aarde?
Wat is de zwaartekrachtattractie van appel op aarde?  Wat absorberen bossen?
Wat absorberen bossen?  Het VN-rapport over invasieve soorten onthult de omvang van de bedreiging voor de natuur en de mens – en hoe deze wordt beheerd
Het VN-rapport over invasieve soorten onthult de omvang van de bedreiging voor de natuur en de mens – en hoe deze wordt beheerd  Weer versus klimaat:hoe je een ongewone koudegolf kunt begrijpen terwijl de wereld heter is dan ooit
Weer versus klimaat:hoe je een ongewone koudegolf kunt begrijpen terwijl de wereld heter is dan ooit
Hoofdlijnen
- De meeste soorten, inclusief mensen, die in hun vroege levensjaren tegenslagen ervaren, lijden als volwassenen. Waarin verschillen gorilla's?
- Welke sequentie in mRNA complementeert de DNA-template?
- Wat zijn de oorzaken van genotype en fenotype?
- Welk fenotype wordt geproduceerd door AA -genotype?
- Waarom zijn er minder organismen aan de top van een biomassapiramide?
- Wat is de meest waarschijnlijke functie van een groepscellen die mitochondriën met een hoog aantal bevatten?
- Het gebruik van pinguïns om de gezondheid van de oceaan te monitoren is mogelijk niet effectief
- Thomas Malthus: Biografie, Populatietheorie & Feiten
- Inzicht in hoe DNA zichzelf herstelt, kan leiden tot een betere behandeling van kanker
- Biologisch afbreekbare glitter en vervuilende microalgen:de nieuwe materialen geïnspireerd door de natuur

- Synthese op het oppervlak van grafeenmoleculen en hun superroosters
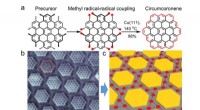
- Koolstof vertoont kwantumeffecten

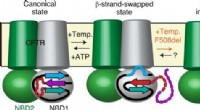
- Uiterlijk van cystische fibrose op moleculaire schaal
- Gecontroleerde fabricage van multimetalen bouwstenen voor hybride nanomaterialen

 Welke cellen van het lichaam zijn het meest gevoelig voor stralingsschade?
Welke cellen van het lichaam zijn het meest gevoelig voor stralingsschade?  Koolwaterstoffen in de diepe aarde?
Koolwaterstoffen in de diepe aarde?  Koolstofdioxide bestaat uit atomen koolstof en?
Koolstofdioxide bestaat uit atomen koolstof en?  Koolstof versus chloor Elektronegativiteit:een gedetailleerde vergelijking
Koolstof versus chloor Elektronegativiteit:een gedetailleerde vergelijking  Wetenschappers onthullen hoe wasmiddelen eigenlijk werken
Wetenschappers onthullen hoe wasmiddelen eigenlijk werken Welke componenten in een circuit proberen de elektriciteit die erdoorheen stroomt?
Welke componenten in een circuit proberen de elektriciteit die erdoorheen stroomt?  Welke sfeer van de aarde wordt alle rots boven en onder de aardoppervlak gemaakt?
Welke sfeer van de aarde wordt alle rots boven en onder de aardoppervlak gemaakt?  Neurowetenschappers trainen een diep neuraal netwerk om geluiden te verwerken zoals mensen dat doen
Neurowetenschappers trainen een diep neuraal netwerk om geluiden te verwerken zoals mensen dat doen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

