
Wetenschap
Biologische buffers begrijpen:hoe ze ons lichaam in balans houden
Door Riti Gupta
Bijgewerkt op 30 augustus 2022
Ken je het verhaal van Goudlokje en de drie beren nog? Toen Goudlokje het huis van de beren binnenkwam, proefde ze elke kom pap. De eerste was te warm, de tweede te koud en de derde was precies goed. Op dezelfde manier zoeken levende organismen naar een omgeving die ‘precies goed’ is. Maar wat betekent ‘precies goed’ voor een cel of een organisme?
Fysiologische pH
Menselijk bloed is enigszins basisch, met een normale pH van ongeveer 7,4. Wanneer de pH van het bloed onder de 7,35 daalt, wordt aangenomen dat iemand in fysiologische acidose verkeert, een aandoening die de orgaanfunctie kan aantasten. Een pH lager dan 7,0 is vaak fataal. Het lichaam moet daarom de hele dag een stabiele pH-waarde handhaven, ongeacht activiteit, dieet of ziekte.
Wat zijn biologische buffers?
Een biologische buffer is een organische verbinding die overtollige waterstofionen (H⁺) neutraliseert, waardoor het interne milieu van het lichaam binnen een smal pH-bereik blijft. De meeste biologische buffers bestaan uit een zwak zuur en de geconjugeerde zwakke base ervan. Ze kunnen toegevoegde zuren of basen absorberen en de oplossing terugbrengen naar de oorspronkelijke pH.
Het klassieke voorbeeld in bloed is het koolzuur-bicarbonaatbuffersysteem. Koolzuur (H₂CO₃) dissocieert en produceert bicarbonaationen (HCO₃⁻). Wanneer overtollige H⁺-ionen zich ophopen, zoals tijdens intensieve inspanning, binden de bicarbonaationen de protonen, waardoor koolzuur wordt hervormd en een gevaarlijke daling van de pH wordt voorkomen.
Waarom zijn buffers belangrijk?
Enzymen en cellulaire processen functioneren alleen optimaal binnen een smal pH-venster. Zelfs een kleine afwijking kan metabolische reacties stopzetten, de zenuwsignalering belemmeren en de immuniteit in gevaar brengen. Biologische buffers zijn daarom alomtegenwoordig in levende systemen en zorgen ervoor dat cellen en weefsels onder veranderende omstandigheden functioneel blijven.
Bij laboratoriumonderzoek kan de keuze van de buffer de experimentele resultaten dramatisch beïnvloeden. Een eiwit dat werkt bij een fysiologische pH (≈7,4) kan bijvoorbeeld activiteit verliezen als het wordt bestudeerd in een buffer bij pH 8,0. Door de pH van de buffer af te stemmen op de oorspronkelijke omgeving van het eiwit, kunnen onderzoekers natuurlijk gedrag observeren en betrouwbare gegevens verkrijgen.
Voorbeelden van biologische buffers
Wetenschappers gebruiken een verscheidenheid aan in de handel verkrijgbare buffers om de fysiologische pH op peil te houden. Een van de meest gebruikte is HEPES (4-(2-hydroxyethyl)-1-piperazineethaansulfonzuur), dat een constante pH tussen 6,8 en 8,2 houdt. Bij het selecteren van een buffer houden onderzoekers rekening met de doel-pH en het bereik waarbinnen stabiliteit vereist is.
Het kiezen van de juiste buffer is essentieel voor zowel klinische fysiologie als biochemische experimenten, en zorgt ervoor dat levende systemen en hun componenten presteren zoals ze dat in de natuur zouden doen.
 De 8 geografische regio's van de wereld
De 8 geografische regio's van de wereld  NASA krijgt een laatste blik op tropische cycloon Ockhis regenval
NASA krijgt een laatste blik op tropische cycloon Ockhis regenval Hoe Caterpillar schrankladers en multi-terrain werken
Hoe Caterpillar schrankladers en multi-terrain werken  Effecten van plantdata van bodembedekkers op bodemeigenschappen na 4 jaar
Effecten van plantdata van bodembedekkers op bodemeigenschappen na 4 jaar NASA ziet de intensivering van de tropische cycloon Ella nu naar het westen gaan
NASA ziet de intensivering van de tropische cycloon Ella nu naar het westen gaan
Hoofdlijnen
- Welke chemische structuur vormt het celmebraan?
- Hoe eindigt de transcriptie?
- Wat betekent communiceren in de wetenschap?
- Onderzoek suggereert dat de gastheerrespons samen met ander bacteriofaagonderzoek moet worden bestudeerd
- Waar geloofden mensen dat er dingen zijn gemaakt voordat cellen ontdekten?
- Welke cellen hebben meer ademhaling nodig?
- Wat is de wetenschappelijke betekenis van verplaatsing?
- AI kan onderzoekers helpen begrijpen wat virussen van plan zijn in de oceanen en in uw darmen
- Wat is SAC in Animal Cell?
- Wetenschappers ontcijferen het belangrijkste principe achter de reactie van metallo-enzymen

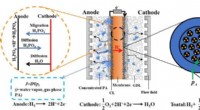
- Het voorspellen van de distributie van fosforzuur en water in een hoge-temperatuur polymeer elektrolytmembraan brandstofcel
- Onderzoekers helpen bij het ontwikkelen van duurzame polymeren

- Hoe alcoholthermometers werken:ontwerp, functie en praktisch gebruik

- Onderzoek naar gloeiende glasdruppels op het ISS

 Wat u kunt doen om lichtvervuiling te verminderen
Wat u kunt doen om lichtvervuiling te verminderen  Wat zijn vijf fysieke eigenschappen van chloor?
Wat zijn vijf fysieke eigenschappen van chloor?  De eigenschappen van een nieuwe klasse brillen voorspellen
De eigenschappen van een nieuwe klasse brillen voorspellen Wanneer is de maan tussen aarde en zon?
Wanneer is de maan tussen aarde en zon?  Juno vindt veranderingen in het magnetische veld van Jupiter
Juno vindt veranderingen in het magnetische veld van Jupiter Een jongen trapt een bal verticaal omhoog met een beginsnelheid van 12 m/s. Bereken de tijd die nodig is om de maximale hoogte en de maximale hoogte te bereiken die de bal bereikt.
Een jongen trapt een bal verticaal omhoog met een beginsnelheid van 12 m/s. Bereken de tijd die nodig is om de maximale hoogte en de maximale hoogte te bereiken die de bal bereikt.  Informatie die uit het menselijk genoom is 'verwijderd', kan de reden zijn dat wij zijn ontstaan
Informatie die uit het menselijk genoom is 'verwijderd', kan de reden zijn dat wij zijn ontstaan  Geurende reinigingsproducten: The New Smoking?
Geurende reinigingsproducten: The New Smoking?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

