
Wetenschap
Molaire concentratie bij STP:gaseigenschappen begrijpen
Dit is waarom:
* Ideale gaswet: De ideale gaswet luidt:PV =nRT, waarbij:
* P =druk
* V =volume
* n =aantal mol
* R =ideale gasconstante
* T =temperatuur
* STP-voorwaarden: STP wordt gedefinieerd als 0°C (273,15 K) en 1 atm druk.
* Molaarconcentratie: De molaire concentratie (ook wel molariteit genoemd) is het aantal mol van een stof per volume-eenheid (mol/liter).
Afleiding:
1. Vanuit de ideale gaswet kunnen we herschikken om n/V =P/RT te krijgen
2. Omdat n/V de molaire concentratie vertegenwoordigt, kunnen we zien dat bij een gegeven temperatuur en druk de molaire concentratie constant is, ongeacht de identiteit van het gas.
Daarom hebben bij STP alle ideale gassen dezelfde molaire concentratie, namelijk ongeveer 0,0446 mol/L.
Belangrijke opmerking: Hoewel de molaire concentratie hetzelfde is voor alle ideale gassen bij STP, zal de massadichtheid verschillen op basis van het molecuulgewicht van elk gas. Dit komt omdat een zwaarder gas meer massa per volume-eenheid zal hebben, zelfs als het aantal mol per volume-eenheid hetzelfde is.
 Wat omvatten de fysieke systemen van de aarde?
Wat omvatten de fysieke systemen van de aarde?  Gerangschikt:De milieu-impact van vijf verschillende frisdrankverpakkingen
Gerangschikt:De milieu-impact van vijf verschillende frisdrankverpakkingen Veranderende variabele in vergelijking die wordt gebruikt om klimaatverandering te projecteren om een nauwkeurigere schatting van neerslagveranderingen te geven
Veranderende variabele in vergelijking die wordt gebruikt om klimaatverandering te projecteren om een nauwkeurigere schatting van neerslagveranderingen te geven Cyanobacteriën leven 600 meter onder de grond zonder zonlicht
Cyanobacteriën leven 600 meter onder de grond zonder zonlicht NASA analyseert de waterdampconcentratie van tropische cycloon Phanfones
NASA analyseert de waterdampconcentratie van tropische cycloon Phanfones
Hoofdlijnen
- Welk proces biedt de grootste opbrengst van ATP voor levensprocessen lichaam?
- Onbeleefdheid op het werk:wordt het 'koninginbijensyndroom' erger?
- Welk type metabolisme doet Archaea?
- Hoe raden werkt
- Hoe reproduceren amoeboids zich?
- Wat zijn neurale cellen?
- Is het tijd dat ons begrip van evolutie evolueert?
- Hoe 2 ... Bepaal wat Google over u zegt
- Leg de rol van een hypothese uit bij wetenschappelijk onderzoek?
- Berekening van de pKa van een zwak zuur:een stapsgewijze handleiding

- AI- en NMR-spectroscopie bepalen in recordtijd de configuratie van atomen
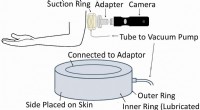
- Nieuw apparaat kan littekens bij cosmetische chirurgie helpen verminderen
- Studie onthult nieuwe bevindingen over synergie van antimicrobiële geneesmiddelen
- Energie opwekken uit vervuilde lucht

 Welke term wordt gebruikt om de fysieke kenmerken van het land te definiëren?
Welke term wordt gebruikt om de fysieke kenmerken van het land te definiëren?  Wat is de juiste hoek voor het installeren van een zonnepaneel?
Wat is de juiste hoek voor het installeren van een zonnepaneel?  Luchtfoto's van planthoogten kunnen boeren helpen om veldgewassen effectiever te beheren
Luchtfoto's van planthoogten kunnen boeren helpen om veldgewassen effectiever te beheren Onderzoekers voeren succesvolle aanvallen uit op het Tor-netwerk en laten zien hoe ze kunnen worden voorkomen
Onderzoekers voeren succesvolle aanvallen uit op het Tor-netwerk en laten zien hoe ze kunnen worden voorkomen  Een bonenvormig orgel dat homeostase in het lichaam onderhoudt?
Een bonenvormig orgel dat homeostase in het lichaam onderhoudt?  Getijdeboringen zijn zeldzaam,
Getijdeboringen zijn zeldzaam,  Welke dag is het? VAE werkt voor het eerst op vrijdag
Welke dag is het? VAE werkt voor het eerst op vrijdag Jura-dieet:waarom onze kennis van wat oude pterosauriërs aten misschien verkeerd is?
Jura-dieet:waarom onze kennis van wat oude pterosauriërs aten misschien verkeerd is?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

