
Wetenschap
Waarom lost olie niet op in water?
* Water is polair: Watermoleculen hebben een enigszins positief uiteinde (waterstofatomen) en een enigszins negatief uiteinde (zuurstofatoom). Met deze polariteit kunnen watermoleculen sterke waterstofbruggen met elkaar vormen.
* olie is niet -polair: Oliemoleculen bestaan uit lange ketens van koolwaterstoffen, die voornamelijk zijn samengesteld uit koolstof en waterstof. Deze ketens zijn niet polair en hebben niet dezelfde ladingscheiding als watermoleculen.
Waarom dit ertoe doet:
* "zoals oplost zoals": Polaire stoffen hebben de neiging om op te lossen in andere polaire stoffen en niet -polaire stoffen hebben de neiging op te lossen in andere niet -polaire stoffen. Dit komt omdat de aantrekkelijke krachten tussen moleculen sterker zijn wanneer ze vergelijkbare polariteiten hebben.
* Zwakke interacties: Wanneer olie en water worden gemengd, zijn de zwakke attracties tussen de niet -polaire oliemoleculen en de polaire watermoleculen niet sterk genoeg om de sterke waterstofbruggen tussen watermoleculen te overwinnen.
* scheiding: Als gevolg hiervan clusteren de oliemoleculen samen en vormen ze afzonderlijke druppeltjes, terwijl de watermoleculen aan elkaar blijven.
in eenvoudiger termen: Stel je voor dat je magneten probeert te mengen met knikkers. De magneten blijven bij elkaar omdat ze vergelijkbare polariteiten hebben, terwijl de knikkers gescheiden blijven omdat ze anders zijn. Evenzo mengen olie en water niet omdat hun moleculen verschillende polariteiten hebben en zich niet tot elkaar aangetrokken voelen.
 Wat zijn de drie stappen van een kettingreactie?
Wat zijn de drie stappen van een kettingreactie?  Wat is de reactie tussen NH4OH en NA2CO3?
Wat is de reactie tussen NH4OH en NA2CO3?  Welke chemische reactie vindt plaats in het lichaam als je bang bent?
Welke chemische reactie vindt plaats in het lichaam als je bang bent?  Geavanceerde nucleaire magnetische resonantietechniek onthult precieze structurele, dynamische details in zeolieten
Geavanceerde nucleaire magnetische resonantietechniek onthult precieze structurele, dynamische details in zeolieten  Wat is een element met 6 protonen in zijn kern?
Wat is een element met 6 protonen in zijn kern?
 Wat is gemeen door ijskoud water?
Wat is gemeen door ijskoud water?  Blauwdruk voor het verplicht stellen van de binnenluchtkwaliteit voor openbare gebouwen in de vorm van normen
Blauwdruk voor het verplicht stellen van de binnenluchtkwaliteit voor openbare gebouwen in de vorm van normen  Aanhoudend tropisch foerageren in de hooglanden van het terminale Pleistoceen/Holoceen Nieuw-Guinea
Aanhoudend tropisch foerageren in de hooglanden van het terminale Pleistoceen/Holoceen Nieuw-Guinea GIS-gebaseerde analyse van breukzonegeometrie en gevaar in een stedelijke omgeving
GIS-gebaseerde analyse van breukzonegeometrie en gevaar in een stedelijke omgeving Toekomstige veranderingen in het menselijk welzijn zijn meer afhankelijk van sociale dan economische factoren
Toekomstige veranderingen in het menselijk welzijn zijn meer afhankelijk van sociale dan economische factoren
Hoofdlijnen
- Waardoor parasieten in het foodweb passen?
- Zijn embryonale stamcellen en kunstmatige gelijkwaardig?
- Genoom onthult hoe Hessische vlieg gallen in tarwe veroorzaakt
- In het Ecuadoraanse Amazonegebied vormen vlinders een graadmeter voor de klimaatverandering
- Kan de wetenschap alle mysteries van het leven verklaren?
- Beschrijf de doorgang van zuurstofmoleculen uit lucht in een reagerende lichaamscel?
- Dugongs zullen waarschijnlijk functioneel uitgestorven zijn in China
- Wat doet Mitchondria in een cel?
- Hoe voert een plant fotosynthese uit?
- Nu kunnen metalen oppervlakken onmiddellijke bacteriedoders zijn

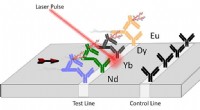
- Nieuwe technologie voor detectie van pathogenen aangedreven door lasers
- Weet u niet zeker of u al corona heeft gehad? Deze test kan het je (misschien) vertellen

- Kijken naar een toekomst waarin het ontdooien van vliegtuigen tot het verleden behoort

- Brandstoffen uit het niets:nieuwe weg naar het afvangen en opwaarderen van CO2

 Wat betekent vol energie?
Wat betekent vol energie?  Van welke zonne -pheomeon zou niet worden verwacht dat deze zal toenemen met een in Sunspot -nummer?
Van welke zonne -pheomeon zou niet worden verwacht dat deze zal toenemen met een in Sunspot -nummer?  Identificatie van Pacific Northwest Spiders
Identificatie van Pacific Northwest Spiders  Menselijke aantasting verandert de luchtkwaliteit boven het Amazone-regenwoud
Menselijke aantasting verandert de luchtkwaliteit boven het Amazone-regenwoud Kenmerken van micro-organismen
Kenmerken van micro-organismen  Waarom hebben Young Fold Mountains afgeronde pieken?
Waarom hebben Young Fold Mountains afgeronde pieken?  Hoe moderne technologie de gezondheid verbeteren?
Hoe moderne technologie de gezondheid verbeteren?  Grote revisie nodig voor netto nul toekomst
Grote revisie nodig voor netto nul toekomst
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

