
Wetenschap
Ionische verbindingen begrijpen:eigenschappen en binding
Hoge smelt- en kookpunten:
* Sterke elektrostatische krachten: De sterke aantrekkingskracht tussen positieve en negatieve ionen in een kristalrooster vergt veel energie om te overwinnen. Dit is de reden waarom ionische verbindingen hoge smelt- en kookpunten hebben.
Vast bij kamertemperatuur (op enkele uitzonderingen na):
* Stijve roosterstructuur: De sterke ionische bindingen creëren een stijve, geordende kristalroosterstructuur. Dit rooster is zeer stabiel en moeilijk te ontwrichten, wat resulteert in een vaste toestand bij kamertemperatuur.
Broze aard:
* Verstoring van roosters: Wanneer er kracht wordt uitgeoefend op een ionisch kristal, kan dit de ionen verplaatsen, waardoor ze op een lijn komen te staan die afstoting tussen soortgelijke ladingen creëert. Deze afstoting verstoort het rooster en zorgt ervoor dat het kristal breekt.
Geleidbaarheid:
* Vaste toestand: In de vaste toestand zitten de ionen vast in het rooster, zodat ze niet vrij kunnen bewegen om een elektrische stroom te geleiden. Daarom zijn ionische verbindingen slechte geleiders van elektriciteit in de vaste toestand.
* Gesmolten of opgeloste toestand: Wanneer ionische verbindingen worden gesmolten of opgelost, kunnen de ionen vrij bewegen en een elektrische stroom geleiden, waardoor ze in deze toestanden goede geleiders zijn.
Oplosbaarheid:
* Polaire oplosmiddelen: Ionische verbindingen hebben de neiging goed op te lossen in polaire oplosmiddelen zoals water. De positieve en negatieve uiteinden van watermoleculen werken samen met de tegengesteld geladen ionen, waardoor de ionische bindingen worden verbroken en de verbinding kan oplossen.
* Niet-polaire oplosmiddelen: Ionische verbindingen zijn over het algemeen onoplosbaar in niet-polaire oplosmiddelen zoals olie of hexaan. Dit komt omdat de niet-polaire oplosmiddelmoleculen niet effectief kunnen interageren met de geladen ionen.
Andere eigendommen:
* Vaak kristallijn: De geordende rangschikking van ionen in een ionisch kristal leidt tot verschillende kristalvormen.
* Hoge dichtheid: De sterke ionische bindingen pakken de ionen dicht bij elkaar, wat resulteert in een hoge dichtheid.
Samenvattend bepalen de sterke elektrostatische krachten tussen ionen in ionische verbindingen hun hoge smelt- en kookpunten, vaste toestand bij kamertemperatuur, brosse aard, geleidbaarheid, oplosbaarheid en andere karakteristieke eigenschappen.
 Thianthreniumchemie maakt reactiviteitsverandering van een nucleofiel aminozuur in een veelzijdig tussenproduct mogelijk
Thianthreniumchemie maakt reactiviteitsverandering van een nucleofiel aminozuur in een veelzijdig tussenproduct mogelijk  Wanneer vindt een chemische reactie plaats?
Wanneer vindt een chemische reactie plaats?  Wetenschappers vinden sneller uit, goedkopere strategie voor het ontwerpen van infrarood-emitterende materialen
Wetenschappers vinden sneller uit, goedkopere strategie voor het ontwerpen van infrarood-emitterende materialen Bevatten verbindingen altijd verschillende soorten atomen?
Bevatten verbindingen altijd verschillende soorten atomen?  Doodt waterstofperoxide bacteriën?
Doodt waterstofperoxide bacteriën?
 Sponzen en koralen:beoordelingen van de zeebodem ter bescherming tegen klimaatverandering
Sponzen en koralen:beoordelingen van de zeebodem ter bescherming tegen klimaatverandering Trends in verbrande gebieden in de Amazone vergelijkbaar met voorgaande jaren
Trends in verbrande gebieden in de Amazone vergelijkbaar met voorgaande jaren Zonne-radiosignalen kunnen worden gebruikt om smeltende ijskappen te volgen
Zonne-radiosignalen kunnen worden gebruikt om smeltende ijskappen te volgen Wat zijn de drie manieren waarop een natie kan groeien?
Wat zijn de drie manieren waarop een natie kan groeien?  Stikstofdioxidevervuiling in kaart gebracht
Stikstofdioxidevervuiling in kaart gebracht
Hoofdlijnen
- Wat doen de lysosomen voor cel?
- Welke eiwitvezel wordt gebruikt voor cellulaire beweging en zijn extreem dun in grootte?
- Artefacten suggereren aankomst van mensen in Australië 18,
- Genen die zich altijd laten zien, worden gebeld?
- Welk wetenschappelijk veld is betrokken bij de identificatieclassificatie en naamgeving van organismen?
- Ouders vertonen vooringenomenheid in rivaliteit tussen broers en zussen, zegt onderzoek
- Wat is een directe relatie in de wetenschap?
- Wat bevat eiwitten?
- Hoe stamcellen huid maken
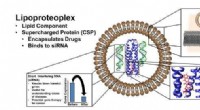
- Onderzoekers creëren biomateriaal dat zowel een krachtig medicijn als gendempers levert
- Nieuw ontworpen molecuul bindt stikstof
- Onderzoekers ontwerpen afstembare, zelfherstellende kleurstoffen voor gebruik in slimme apparaten van de volgende generatie

- Spontaan patronen creëren in synthetische materialen

- Video:Wordt het kombucha?

 Klinkt 20000 Hz luid of hoog?
Klinkt 20000 Hz luid of hoog?  Oudste geregistreerde zonsverduistering helpt bij het dateren van de Egyptische farao's
Oudste geregistreerde zonsverduistering helpt bij het dateren van de Egyptische farao's Hoe manuever in de exosfeer een space shuttle?
Hoe manuever in de exosfeer een space shuttle?  Versnelde berekeningen die onthullen hoe elektronen op elkaar inwerken in materialen
Versnelde berekeningen die onthullen hoe elektronen op elkaar inwerken in materialen  Welk apparaat is voor het verzenden van gecodeerde berichten via draden en elektriciteit?
Welk apparaat is voor het verzenden van gecodeerde berichten via draden en elektriciteit?  Wat zijn de kleine structuren in een cel?
Wat zijn de kleine structuren in een cel?  Tropische cycloon Haleh verzwakt in NASA-NOAA-satellietbeelden
Tropische cycloon Haleh verzwakt in NASA-NOAA-satellietbeelden Kennis van de Afrikaans-Amerikaanse taal en cultuur komt ten goede aan leraren in STEM-gebieden
Kennis van de Afrikaans-Amerikaanse taal en cultuur komt ten goede aan leraren in STEM-gebieden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

