
Wetenschap
Thianthreniumchemie maakt reactiviteitsverandering van een nucleofiel aminozuur in een veelzijdig tussenproduct mogelijk
Chemische diversificatie van eiwitten is een belangrijk concept bij de studie van biologische processen en de complexe structuren van de eiwitten zelf. Onderzoekers van de Max Planck Society hebben nu hun fascinerende bevindingen over een aminozuur gepubliceerd in Nature Chemistry .
Chemische diversificatie van eiwitten omvat het gebruik van snelle en milde reacties die zich selectief richten op een specifiek aminozuur en dus op een bouwsteen van eiwitten. Cysteïne is een prominent voorbeeld en kan momenteel op twee manieren worden aangepast. De eerste manier vereist de synthese van elektrofielen voor elke gewenste modificatie, bijvoorbeeld een fluorescentiesonde die het mogelijk maakt het molecuul te volgen in zeer complexe biologische mengsels.
De tweede manier maakt van cysteïne zelf een chemische spil, die vervolgens kan worden gediversifieerd. Tot nu toe werd dit uitgevoerd in meerstapssyntheses. Deze methoden hebben het nadeel dat de spil niet kan worden geïntroduceerd in aanwezigheid van externe reagentia die nodig zijn voor de diversificatie ervan. Dat gaat vaak gepaard met een beperkte keuze aan reagentia voor de functionaliteit, omdat de spil tijdens zuiveringsprocessen in oplossing moet blijven en daardoor een intrinsiek verminderde reactiviteit heeft.
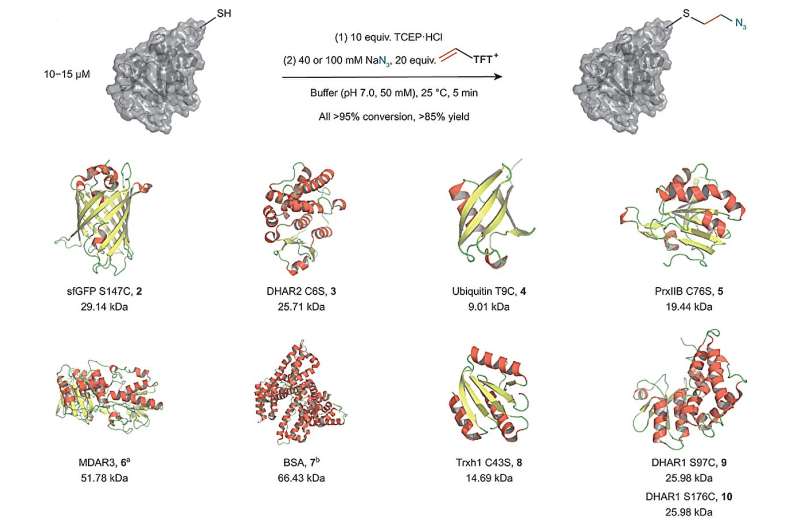
Een nieuwe techniek van de onderzoeksgroep van Tobias Ritter, directeur van het Max-Planck-Institut für Kohlenforschung, is intrigerend omdat het de introductie mogelijk maakt van een zeer reactief tussenproduct in een éénpotsproces op basis van één enkele elektrofiel. Bovendien maakt deze methode een brede diversificatie van het nieuwe tussenproduct mogelijk, zelfs in de aanwezigheid van externe reagentia.
In hun onderzoek vond de Ritter-groep een manier om vinylthianthreniumzouten te gebruiken om cysteïne in situ om te zetten in een zeer reactief episulfonium-elektrofiel. Deze aanpak maakt het mogelijk om cysteïne met verschillende andere externe nucleofielen te verbinden in één enkel proces, zonder dat er extra stappen nodig zijn. De methode stelt de wetenschappers in staat om verschillende biorelevante functionele groepen aan eiwitten te koppelen met behulp van een korte en stabiele ethyleenbinding zeer dicht bij het oppervlak van het eiwit. Dit biedt dus een nieuwe en aantrekkelijke manier om labels of functionaliteiten toe te voegen die de chemische omgeving van een eiwit veranderen.
Als er geen externe nucleofielen worden toegevoegd, kunnen andere aminozuren reageren met het episulfoniumtussenproduct in een intramoleculaire reactie. Die reactiviteit maakt eiwit-eiwitligatie en macrocyclisatie van lineaire peptiden mogelijk. Terwijl de eerste benadering het mogelijk maakt om eiwitcomplexen en hun vaak gewijzigde biologische activiteit te bestuderen, maakt de tweede benadering de peptiden stabieler ten opzichte van biologische afbraak als ze bijvoorbeeld als medicijn worden gebruikt.
Bovendien zorgde de synthese van vinylthianthreniumzouten uit ethyleengas ervoor dat de Ritter-groep reagentia kon synthetiseren met een andere samenstelling van isotopen. Deze met isotoop gelabelde verbindingen bezitten dezelfde reactiviteit als de niet-gelabelde derivaten, maar verschillen enigszins in hun molecuulgewicht. Daarom kunnen ze worden gebruikt in het state-of-the-art proteomics-onderzoek naar massaspectrometrie om kwantitatieve informatie uit hele cellulaire systemen te extraheren. Over het geheel genomen wordt de methode waarbij vinylthianthreniumzouten worden gebruikt, gepresenteerd als een nuttig en breed toepasbaar hulpmiddel op het gebied van de chemische biologie.
Meer informatie: Philipp Hartmann et al, Chemoselectieve umpolung van thiolen naar episulfoniums voor bioconjugatie van cysteïne, Natuurchemie (2023). DOI:10.1038/s41557-023-01388-7
Journaalinformatie: Natuurchemie
Aangeboden door Max Planck Society
 Wetenschappers raden aan een cryptozoïcum mineraal te gebruiken om nieuwe lichtgewicht koolstofcomposieten te maken
Wetenschappers raden aan een cryptozoïcum mineraal te gebruiken om nieuwe lichtgewicht koolstofcomposieten te maken Glanzende megakristallen die zichzelf bouwen
Glanzende megakristallen die zichzelf bouwen Directe elektrolyse heeft gemengde resultaten voor het extraheren van brandstofbronnen uit microalgen
Directe elektrolyse heeft gemengde resultaten voor het extraheren van brandstofbronnen uit microalgen De baanbrekende techniek van scheikundigen in Miami maakt ontwerpen mogelijk op het grensvlak van scheikunde en biologie
De baanbrekende techniek van scheikundigen in Miami maakt ontwerpen mogelijk op het grensvlak van scheikunde en biologie Stap voor stap naar het eindproduct via enzymkatalyse
Stap voor stap naar het eindproduct via enzymkatalyse
 GPM-satelliet vindt regenval weggeduwd van het centrum van tropische cycloon Cebiles
GPM-satelliet vindt regenval weggeduwd van het centrum van tropische cycloon Cebiles Lijst met buideldieren
Lijst met buideldieren Waarom nam de regenval over het Aziatische plateau in het binnenland rond 1999 abrupt af?
Waarom nam de regenval over het Aziatische plateau in het binnenland rond 1999 abrupt af? Wuhans lockdown verminderde luchtvervuiling tot 63% - nieuw onderzoek
Wuhans lockdown verminderde luchtvervuiling tot 63% - nieuw onderzoek Grote oliedeal met DR Congo kan nietig zijn:Watchdog
Grote oliedeal met DR Congo kan nietig zijn:Watchdog
Hoofdlijnen
- Hoeveel steenarenden zijn er?
- Hoe vogelgenetica zich aanpast aan klimaatverandering
- Een natuurlijke schimmelstam kan olielekkages opruimen en de oliezanden van Albertas weer tot leven brengen
- Stille mutaties helpen bacteriën antibiotica te ontwijken
- Slachtoffers van dolfijnen in de Zwarte Zee in de Russische oorlog in Oekraïne
- Politieke instabiliteit en zwak bestuur leiden tot verlies van soorten, studie vondsten
- Cellulair metabolisme: definitie, proces en de rol van ATP
- Welk vierkant is groter? Honingbijen zien visuele illusies zoals mensen dat doen
- Top 5 manieren om slimmer te worden
- Ontwerpen van flexibele en rekbare elektronische systemen met één kristal

- Nieuw 2D metalen organisch raamwerk met interessante elektrische geleidbaarheid en magnetische eigenschappen
- Onderzoekers ontcijferen structuur van veelbelovende metalen organische raamwerken

- Nieuw additief helpt onderzoekers om CO2 selectiever om te zetten in multicarbon-brandstoffen

- Een chemische aanwijzing voor hoe het leven op aarde begon

 Heroverweging van rijping:Ethylenen hebben een grotere rol gespeeld in de ontwikkeling en rijping van aardbeienfruit
Heroverweging van rijping:Ethylenen hebben een grotere rol gespeeld in de ontwikkeling en rijping van aardbeienfruit  Studie toont transportovertuigingen van 20 jaar geleden grotendeels mythen, voorspelt dat het vandaag ook zo zal zijn
Studie toont transportovertuigingen van 20 jaar geleden grotendeels mythen, voorspelt dat het vandaag ook zo zal zijn IBM lanceert commerciële quantum computing - waren niet klaar voor wat komen gaat
IBM lanceert commerciële quantum computing - waren niet klaar voor wat komen gaat Glas half leeg? Wat klimaatverandering betekent voor de Canadese wijnindustrie
Glas half leeg? Wat klimaatverandering betekent voor de Canadese wijnindustrie  Grote westerse merken vervuilen oceanen met goedkoop plastic in Filipijnen:rapport
Grote westerse merken vervuilen oceanen met goedkoop plastic in Filipijnen:rapport Kinderen die van zorg naar volwassen leven gaan, worden zwaar in de steek gelaten – en vallen ten prooi aan criminele bendes
Kinderen die van zorg naar volwassen leven gaan, worden zwaar in de steek gelaten – en vallen ten prooi aan criminele bendes Woorddetectives:wetenschap kan opiniecolumnist helpen
Woorddetectives:wetenschap kan opiniecolumnist helpen Waarom microfinanciering als hulp niet voldoende is om vrouwen mondiger te maken
Waarom microfinanciering als hulp niet voldoende is om vrouwen mondiger te maken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

