
Wetenschap
Smeltpunttrends in elementen van groep 7:atoomnummer en intermoleculaire krachten
* Algemene trend: Smeltpunten stijgen doorgaans terwijl je naar groep 7 gaat van fluor (F) naar astatine (At).
* Uitleg: Deze trend is voornamelijk te wijten aan de toenemende intermoleculaire krachten. Naarmate je lager in de groep komt, worden de atomen groter, met meer elektronen en een grotere polariseerbaarheid. Dit leidt tot sterkere London Dispersion Forces (LDF's) tussen de moleculen, waardoor er meer energie nodig is om ze uit elkaar te halen en de substantie te smelten.
* Uitzonderingen:
* Fluor (F) heeft een ongewoon laag smeltpunt vergeleken met de andere halogenen. Dit wordt toegeschreven aan de kleine omvang en de sterke elektronegativiteit van fluor, wat leidt tot zwakke LDF's.
* Chloor (Cl) en Broom (Br) hebben relatief vergelijkbare smeltpunten. Dit is waarschijnlijk te wijten aan het evenwicht tussen de toenemende LDF's en de afnemende elektronegativiteit, die de dipool-dipoolinteracties kunnen verzwakken.
Samengevat:
Hoewel er een algemene trend is van toenemende smeltpunten in Groep 7, is de relatie niet eenvoudig en zijn er opmerkelijke uitzonderingen. Het smeltpunt wordt beïnvloed door verschillende factoren, waaronder:
* Intermoleculaire krachten: De sterkte van de London Dispersion Forces (LDF’s) speelt een belangrijke rol.
* Atomische grootte: Grotere atomen hebben over het algemeen sterkere LDF's.
* Elektronegativiteit: Hoge elektronegativiteit kan de sterkte van dipool-dipoolinteracties beïnvloeden.
Hoofdlijnen
- Welke onderverdeling van anatomie omvat de onderzoeksorganen die samen functioneren?
- Welke soorten organismen gaan door anaërobe ademhaling?
- Wat is een levend organisme dat met uitsterven wordt bedreigd in zijn gehele of een aanzienlijk deel van zijn verspreidingsgebied?
- Wat is een organisme dat in staat is om zijn eigen voedsel te maken?
- De wetenschap achter euforie na de ontlasting (Poo-Phoria) en de gezondheidsvoordelen ervan
- Geowetenschappers vergelijken micro-organismen in de poolgebieden
- DNA wordt vaak gebruikt bij het oplossen van misdaden. Maar hoe werkt DNA-profilering eigenlijk?
- Hoe gebruik je een microscoop om cellen te bekijken?
- Relatie tussen DNA-basen Genen, eiwitten en eigenschappen
- Chemisch proces breekt lignine af en verandert berkenhout in bruikbare chemische producten

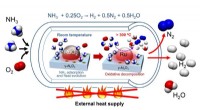
- Ontdekking van een eenvoudig proces voor H2-productie met ammoniak als drager
- Ingenieurs kunnen ultrazeldzame eiwitten in bloed detecteren met behulp van een mobiele camera

- Het mengen van zijde met polymeren kan leiden tot betere biomedische implantaten

- Complex leven is ontstaan uit de toevallige koppeling van kleine moleculen

 De psychologie van nepnieuws
De psychologie van nepnieuws Hoe digitale media de grens tussen Australië en China doen vervagen
Hoe digitale media de grens tussen Australië en China doen vervagen Feiten over de chromosfeer van de zon
Feiten over de chromosfeer van de zon  Methaan maken op Mars
Methaan maken op Mars Wat is Spaans voor met sneeuw bedekte bergen?
Wat is Spaans voor met sneeuw bedekte bergen?  De oorlog tegen afvalverzamelaars
De oorlog tegen afvalverzamelaars Studie daagt slacktivisme onder jonge volwassenen uit
Studie daagt slacktivisme onder jonge volwassenen uit Wetenschappers herscheppen wat misschien wel de eerste vonk van het leven zou kunnen zijn
Wetenschappers herscheppen wat misschien wel de eerste vonk van het leven zou kunnen zijn
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


