
Wetenschap
Converteer atomen naar grammen met een rekenmachine:een praktische gids
Door Riti Gupta | Bijgewerkt op 24 maart 2022
Het tellen van individuele atomen is onmogelijk met een balans, dus gebruiken scheikundigen het getal van Avogadro om de microscopische wereld te koppelen aan macroscopische metingen.
conejota/iStock/GettyImages
Het getal van Avogadro:de brug tussen atomen en mollen
Het getal van Avogadro is 6,022×10²³, de hoeveelheid deeltjes in één mol (mol). Eén mol kan een verzameling atomen, moleculen of ionen zijn, afhankelijk van de stof.
Wat is de massa van één mol?
De massa van een mol:de molaire massa —wordt uitgedrukt in gram per mol (gmol⁻¹). Je vindt het direct in het periodiek systeem (bijvoorbeeld chloor:35,45 gmol⁻¹). Voor verbindingen telt u de atoommassa's van alle samenstellende atomen bij elkaar op (water:2×1,008+15,999=18,02gmol⁻¹).
Van atomen naar grammen:het conversieproces
Om een bepaald aantal atomen om te rekenen naar grammen:
- Zet atomen om in mol:deel door het getal van Avogadro.
- Vermenigvuldig de resulterende mollen met de molaire massa.
Voorbeeld:3×10²⁴ chlooratomen
3×10²⁴atomenCl ÷ 6,022×10²³atomsmol⁻¹=4,98molCl
4,98molCl × 35,45gmol⁻¹=176,6gCl
Dus 3×10²⁴ chlooratomen wegen 176,6 gram.
Omgaan met verbindingen:atomen in een molecuul
Als je alleen het atoomaantal kent van een element dat in een verbinding voorkomt, bepaal dan eerst hoeveel moleculen van die verbinding je hebt, op basis van de atoom-tot-molecuul-verhouding.
Voorbeeld:5,55×10²³ zuurstofatomen in CO₂
5,55×10²³atomenO ÷ 2atomenOmol₂=2,78×10²³moleculenCO₂
2,78×10²³moleculenCO₂ ÷ 6,022×10²³moleculenmol⁻¹=0,462molCO₂
0,462molCO₂ × 44,01gmol⁻¹=20,3gCO₂
Houd bij elke stap altijd uw eenheden bij om fouten te voorkomen.
Referenties: IUPAC Groenboek, iupac.org ; Periodiek Systeem, PubChem .
 Welke discipline heeft bewijs gevonden voor evolutie op basis van de inheemse verdelingen van levende soorten?
Welke discipline heeft bewijs gevonden voor evolutie op basis van de inheemse verdelingen van levende soorten?  Model:Hoe ziet het toegenomen gebruik van houtachtige biomassa eruit voor het mondiale bosecosysteem
Model:Hoe ziet het toegenomen gebruik van houtachtige biomassa eruit voor het mondiale bosecosysteem  Het Lidar-netwerk heeft de potentie om vervuilende natuurbranden op het hele continent te volgen
Het Lidar-netwerk heeft de potentie om vervuilende natuurbranden op het hele continent te volgen Waarom is de temperatuur een factor die de natuurlijke vegetatie beïnvloedt?
Waarom is de temperatuur een factor die de natuurlijke vegetatie beïnvloedt?  Wat is een aantrekkingskracht tussen watergedeeltjes?
Wat is een aantrekkingskracht tussen watergedeeltjes?
Hoofdlijnen
- Wat is de structurele classificatie van het zenuwstelsel?
- Wat voor soort mutatie is een gunstig voor een organisme?
- Een decomposer is een insectenschimmel of bacteriën die dierenplanten breekt?
- Nieuwe studies zijn bedoeld om sociaalwetenschappelijke methoden in natuurbehoudonderzoek te stimuleren
- Welke verschillen zouden worden verwacht in experimenten met squash die niet zelf bestuiven?
- Wat is de beweging van chemische stoffen die meestal over het celmembraan opnieuw een concentratiegradiënt vereist, vereist cellen naar energie?
- Waarom schrijven wetenschappers conclusies voor experimenten?
- Wat wordt macromolecuul gevormd als monomeren samenvoegen?
- Kunnen genetica de vorm van een plant veranderen?
- Dieselbrandstof begrijpen:soorten, productie en impact op het milieu

- Ingenieurs produceren op additieve wijze elektriciteitspalen van biologisch afgeleide en gerecyclede materialen

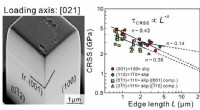
- Micropijlercompressie voor het vinden van hittebestendige legeringen
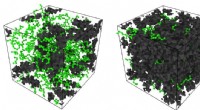
- Nauwe ruimtes tip aanwezigheid van petrochemicaliën
- Wetenschappers ontwerpen nieuwe eiwitstructuur
 Wat is geen categorie van mariene organismen?
Wat is geen categorie van mariene organismen?  De nadelen van lineaire programmering
De nadelen van lineaire programmering  Newtons Second Law stelt dat kracht gelijk is aan?
Newtons Second Law stelt dat kracht gelijk is aan?  Welke stoffen heeft een plant nodig om aminozuur en eiwitten van glucose te maken?
Welke stoffen heeft een plant nodig om aminozuur en eiwitten van glucose te maken?  Welke energieoverdracht vindt plaats wanneer een voetbal op een opwaartse richting wordt geschopt?
Welke energieoverdracht vindt plaats wanneer een voetbal op een opwaartse richting wordt geschopt?  Zijn kookpunten en bevriezingsvoorbeelden van chemische eigenschappen?
Zijn kookpunten en bevriezingsvoorbeelden van chemische eigenschappen?  Is windenergie een hernieuwbare energiebron en waarom?
Is windenergie een hernieuwbare energiebron en waarom?  Waarom reageren verschillende metalen anders met zuur?
Waarom reageren verschillende metalen anders met zuur?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

