
Wetenschap
Sterke elektrolyten, zuren en basen:de verbinding begrijpen
* Sterke elektrolyten: Dit zijn stoffen die volledig ioniseren (opbreken in ionen) wanneer ze worden opgelost in water. Dit betekent dat ze in oplossing een hoge concentratie ionen produceren, waardoor ze uitstekende elektriciteitsgeleiders zijn.
* Sterke zuren: Dit zijn zuren die in water volledig ioniseren, waarbij een hoge concentratie waterstofionen (H+) vrijkomt. Omdat ze volledig ioniseren, zijn het ook sterke elektrolyten.
* Sterke basis: Dit zijn basen die in water volledig ioniseren, waarbij een hoge concentratie hydroxide-ionen (OH-) vrijkomt. Net als sterke zuren zijn het sterke elektrolyten vanwege hun volledige ionisatie.
Belangrijkste punten:
* Niet alle sterke elektrolyten zijn zuren of basen: Zouten zoals natriumchloride (NaCl) zijn bijvoorbeeld sterke elektrolyten, maar ze zijn niet zuur of basisch.
* Niet alle zuren en basen zijn sterk: Zwakke zuren en zwakke basen ioniseren slechts gedeeltelijk in water, wat betekent dat het geen sterke elektrolyten zijn.
Voorbeelden:
* Sterk zuur en sterke elektrolyt: Zoutzuur (HCl) ioniseert volledig in H+ en Cl-ionen in water.
* Sterke basis en sterke elektrolyt: Natriumhydroxide (NaOH) ioniseert volledig in Na+ en OH- ionen in water.
* Zwak zuur en zwak elektrolyt: Azijnzuur (CH3COOH) ioniseert slechts gedeeltelijk in water, waardoor een lagere concentratie H+-ionen ontstaat in vergelijking met een sterk zuur.
Samengevat:
* Sterke zuren en sterke basen zijn subsets van sterke elektrolyten. Het zijn sterke elektrolyten omdat ze volledig ioniseren.
* Niet alle sterke elektrolyten zijn echter sterke zuren of basen.
 Waarom is de reactie van calciumhydroxide en zwavelzuur anders dan die van natriumzuur?
Waarom is de reactie van calciumhydroxide en zwavelzuur anders dan die van natriumzuur?  Hoe weet je of een chemische vergelijking endotherm is?
Hoe weet je of een chemische vergelijking endotherm is?  Is een brosse samengestelde moleculaire verbinding?
Is een brosse samengestelde moleculaire verbinding?  Apparaat simuleert filter- en ionentransportfuncties van menselijke nieren
Apparaat simuleert filter- en ionentransportfuncties van menselijke nieren Wat is de formule voor thalliumcarbonaat?
Wat is de formule voor thalliumcarbonaat?
 Wat is het woord voor gemeenschap van organismen en hun fysieke omgeving?
Wat is het woord voor gemeenschap van organismen en hun fysieke omgeving?  Wat zal een object dat warmer is dan de omgeving?
Wat zal een object dat warmer is dan de omgeving?  Bomen in de uiterwaarden van de Amazone stoten evenveel methaan uit als alle oceanen van de aarde samen
Bomen in de uiterwaarden van de Amazone stoten evenveel methaan uit als alle oceanen van de aarde samen Hoe lang houden grijze beren overwinteren?
Hoe lang houden grijze beren overwinteren?  Kijk in je eigen voorraadkast of koelkast om de grootste boosdoener van voedselverspilling te vinden
Kijk in je eigen voorraadkast of koelkast om de grootste boosdoener van voedselverspilling te vinden
Hoofdlijnen
- Kwalitatieve versus kwantitatieve eigenschappen:hoe genetica ons fenotype vormt
- Waarom wordt het plasmamembraan genaamd semipermeable membraan genaamd?
- Wat zijn de twee prokaryotische rijken?
- Is rhizoïden autotrofe voeding of hetetrofische voeding?
- Acht nieuwe soorten kleine gekko's tuimelen uit de regenwouden van Madagaskar
- Hoe bemiddelen onderstammen het zoutgehalte van de telg onder zoutstress?
- Genetisch hulpmiddel dat een soort onder VN-beoordeling kan veroordelen
- Wat bepaalt de verschillende waterbiomen?
- Wat is basispaaraffiniteit?
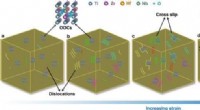
- Verbeterde sterkte en taaiheid in een legering met hoge entropie via geordende zuurstofcomplexen
- Stop die BPA-vrije drinkflessen in de vaatwasser voordat je ze gebruikt

- Glycanen als biomarkers voor kanker?
- Hydrogels aansteken via nanomaterialen

- Brandstofaërosolen die de vervuiling van het milieu verminderen

 Hoe invasieve soorten werken
Hoe invasieve soorten werken  Is geo thermische energie niet hernieuwbaar?
Is geo thermische energie niet hernieuwbaar?  Wat is het Avogadros-nummer?
Wat is het Avogadros-nummer?  Gebonden voor de EU, Biomassa van Amerikaanse makelij controleert de juiste vakjes
Gebonden voor de EU, Biomassa van Amerikaanse makelij controleert de juiste vakjes Nieuwe methode om therapeutische medicijnen toe te dienen met behulp van langwerpige nanokristallen
Nieuwe methode om therapeutische medicijnen toe te dienen met behulp van langwerpige nanokristallen Is het waar dat de temperatuur van een object een meting is De gemiddelde potentiële energiemoleculen in object?
Is het waar dat de temperatuur van een object een meting is De gemiddelde potentiële energiemoleculen in object?  Het manipuleren van rimpels kan leiden tot grafeenhalfgeleiders
Het manipuleren van rimpels kan leiden tot grafeenhalfgeleiders Wat is het gewicht van een gloedstick verlicht?
Wat is het gewicht van een gloedstick verlicht?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

