
Wetenschap
Waarom is de reactie van calciumhydroxide en zwavelzuur anders dan die van natriumzuur?
Calciumhydroxide en zwavelzuur:
Wanneer calciumhydroxide (Ca(OH)2) reageert met zwavelzuur (H2SO4), ondergaat het een dubbele verdringings- of neutralisatiereactie. De reactie kan worden weergegeven als:
Ca(OH)2 + H2SO4 → CaSO4 + 2H2O
In deze reactie:
- Calciumionen (Ca2+) uit calciumhydroxide combineren met sulfaationen (SO42-) uit zwavelzuur om calciumsulfaat (CaSO4) te vormen, een onoplosbare verbinding die neerslaat als een witte vaste stof.
- Waterstofionen (H+) uit zwavelzuur combineren met hydroxide-ionen (OH-) uit calciumhydroxide om watermoleculen (H2O) te vormen.
De reactie is exotherm, wat betekent dat er warmte vrijkomt.
Natriumzuur (natriumwaterstofsulfaat) en natriumhydroxide:
Natriumwaterstofsulfaat (NaHSO4), ook bekend als natriumbisulfaat of natriumzuursulfaat, is een zuur zout. Wanneer het reageert met natriumhydroxide (NaOH), ondergaat het een neutralisatiereactie. De reactie kan worden weergegeven als:
NaHSO4 + NaOH → Na2SO4 + H2O
In deze reactie:
- Waterstofionen (H+) uit natriumwaterstofsulfaat combineren met hydroxide-ionen (OH-) uit natriumhydroxide om watermoleculen (H2O) te vormen.
- Natriumionen (Na+) van beide reactanten vormen samen natriumsulfaat (Na2SO4), een oplosbare verbinding die opgelost blijft in de oplossing.
De reactie is ook exotherm, waarbij warmte vrijkomt.
Het belangrijkste verschil tussen de twee reacties is de vorming van een onoplosbare verbinding (calciumsulfaat) bij de reactie van calciumhydroxide en zwavelzuur, wat leidt tot het neerslaan van een vaste stof, terwijl de reactie van natriumwaterstofsulfaat en natriumhydroxide resulteert in de vorming van een oplosbare verbinding (natriumsulfaat) die opgelost blijft in de oplossing.
 Wat is het getal op het periodiek systeem voor HCl?
Wat is het getal op het periodiek systeem voor HCl?  Nieuw onderzoek biedt uitgebreide inzichten in de reactie van de hersenen op opioïden
Nieuw onderzoek biedt uitgebreide inzichten in de reactie van de hersenen op opioïden Een groenere manier om ketonen te maken
Een groenere manier om ketonen te maken Met gewone tape, onderzoekers maken chip die de ontwikkeling van medicijnen kan versnellen
Met gewone tape, onderzoekers maken chip die de ontwikkeling van medicijnen kan versnellen Als maagzuur een PH van 1 heeft en de persoon een tablet heeft ingenomen waardoor de pH naar 3 steeg, hoeveel was dan de toename van de PH?
Als maagzuur een PH van 1 heeft en de persoon een tablet heeft ingenomen waardoor de pH naar 3 steeg, hoeveel was dan de toename van de PH?
 Hoe beïnvloedt rommeligheid de voorkeur van consumenten voor eenvoud?
Hoe beïnvloedt rommeligheid de voorkeur van consumenten voor eenvoud?  Maak kennis met de made:hoe dit vleesminnende, kontademende wonder ons helpt moorden op te lossen
Maak kennis met de made:hoe dit vleesminnende, kontademende wonder ons helpt moorden op te lossen  Asteroïde inslag, geen vulkanen, maakte de aarde onbewoonbaar voor dinosaurussen
Asteroïde inslag, geen vulkanen, maakte de aarde onbewoonbaar voor dinosaurussen NASA volgt grote tropische cycloon Cebile in Zuid-Indische Oceaan
NASA volgt grote tropische cycloon Cebile in Zuid-Indische Oceaan Vraag en antwoord:Door de droogte van El Niño is het Kariba-meer in Zimbabwe slechts voor 13% vol – een ramp voor mensen en dieren in het wild
Vraag en antwoord:Door de droogte van El Niño is het Kariba-meer in Zimbabwe slechts voor 13% vol – een ramp voor mensen en dieren in het wild
Hoofdlijnen
- Waarom rechtopstaande kuifpinguïns hun eerste ei afwijzen en een tweede leggen
- Rechtbank vindt het goed om een soort uil te doden om het effect op andere uilen te zien
- Dahls paddenkopschildpad bedreigd door versnipperd leefgebied, krimpende bevolking
- Wordt kunstmatige intelligentie in alle disciplines op dezelfde manier gedefinieerd?
- Waar zijn spiervezels van gemaakt?
- Kenia mannelijke leeuwen gezien in intieme daad; binding, deskundigen zeggen
- Supercoiling duwt moleculaire handboeien langs chromatinevezels
- Onkruidverdelger glyfosaat, controversieel maar nog steeds het meest gebruikt
- The Anatomy of the Hydra
- De thermische geleidbaarheid van polymeren regelen met licht

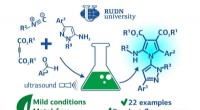
- Chemicus stelt milieuvriendelijke synthese van fluorescerende verbindingen voor medicijnen voor
- Hoe een COVID-19-infectie de bloedcellen op de lange termijn verandert

- Oog hebben voor kleuren:bedrukbare lichtsensoren

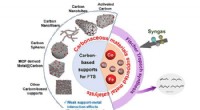
- Op koolstof gebaseerde katalysatoren die worden gebruikt voor Fischer-Tropsch-synthese
 Helpt of doet het pijn om uw kredietscore te controleren?
Helpt of doet het pijn om uw kredietscore te controleren? Robotic rectums geven Docs een gevoel voor prostaat
Robotic rectums geven Docs een gevoel voor prostaat  Is een lamp een bron van energie?
Is een lamp een bron van energie?  Hoeveel regenwoud hebben vogels nodig?
Hoeveel regenwoud hebben vogels nodig?  Hoe cellen kunstmatige ingrediënten 'lezen' die in een genetisch recept worden gegooid
Hoe cellen kunstmatige ingrediënten 'lezen' die in een genetisch recept worden gegooid  Solar Orbiter klaar voor wetenschap ondanks COVID-19 tegenslagen
Solar Orbiter klaar voor wetenschap ondanks COVID-19 tegenslagen Onbetrouwbare herinneringen maken het moeilijk om ethisch te winkelen
Onbetrouwbare herinneringen maken het moeilijk om ethisch te winkelen Grassland Biome-feiten
Grassland Biome-feiten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

