
Wetenschap
Broom- en waterreactie:disproportionering uitgelegd
Br₂ (l) + H₂O (l) ⇌ HBr (aq) + HOBr (aq)
Hier is een overzicht van wat er gebeurt:
* Oxidatie: Eén broomatoom krijgt een elektron om een bromide-ion (Br-) in HBr te vormen. Dit is een reductie.
* Reductie: Het andere broomatoom verliest een elektron en vormt een hypobromietion (OBr-) in HOBr. Dit is een oxidatie.
Belangrijke punten:
* De reactie is omkeerbaar, wat betekent dat het evenwicht kan verschuiven afhankelijk van de omstandigheden.
* HOBr is een zwak zuur en een krachtig oxidatiemiddel. Het is verantwoordelijk voor de blekende en desinfecterende eigenschappen van broomwater.
* De reactie wordt bevorderd door de aanwezigheid van overtollig water.
*De kleur van broomwater verandert van oranjebruin naar lichtgeel door de vorming van HOBr.
Toepassingen:
Deze reactie is belangrijk bij verschillende toepassingen, waaronder:
* Desinfectie: Broomwater wordt gebruikt als desinfectiemiddel in zwembaden en spa's.
* Bleken: HOBr is een krachtig bleekmiddel.
* Organische synthese: HOBr wordt gebruikt als reagens bij verschillende organische reacties.
Over het geheel genomen is de reactie tussen broom en water een complex maar belangrijk proces dat leidt tot de vorming van verschillende waardevolle chemische stoffen.
 Uitzoeken of een verbinding een sterke elektrolyt is
Uitzoeken of een verbinding een sterke elektrolyt is Is de toevoeging van warmte aan vast natriumchloride totdat het een chemische reactie smelt?
Is de toevoeging van warmte aan vast natriumchloride totdat het een chemische reactie smelt?  Hoeveel zwavelatomen zijn er in 3,6 mol zwavel?
Hoeveel zwavelatomen zijn er in 3,6 mol zwavel?  Fysieke versus chemische verandering:poederachtige stoffen begrijpen
Fysieke versus chemische verandering:poederachtige stoffen begrijpen  Is Bolling Water een chemische verandering?
Is Bolling Water een chemische verandering?
 Door na te gaan hoe de gevolgen van rampen escaleren, kunnen de reacties op noodsituaties worden verbeterd
Door na te gaan hoe de gevolgen van rampen escaleren, kunnen de reacties op noodsituaties worden verbeterd De Californische senator Blakespear zegt dat de kustspoorlijn zich op een klimaatkruispunt bevindt
De Californische senator Blakespear zegt dat de kustspoorlijn zich op een klimaatkruispunt bevindt  Onderzoek identificeert vingerafdrukken van klimaatverandering en aansprakelijkheid van emittenten
Onderzoek identificeert vingerafdrukken van klimaatverandering en aansprakelijkheid van emittenten Animals of Cold Desert Biomes
Animals of Cold Desert Biomes  Satellietbeeld legt ontwikkeling van tropische stormdepressie 8E vast
Satellietbeeld legt ontwikkeling van tropische stormdepressie 8E vast
Hoofdlijnen
- Welke soorten cellen hebben twee kern?
- Protisten die een multinucleate glob met cytoplasma produceren, is?
- Wat betekent het dat levende wezens delen van populaties evolueren?
- Zouden dierencellen normaal gesproken aan elkaar worden bevestigd?
- Evolutie begrijpen:een uitgebreid overzicht
- De meerderheid van de botten in het menselijk lichaam wordt doorgevoerd?
- Wat wordt verondersteld verantwoordelijk te zijn voor de snelle wateruitwisseling in plantencellen?
- Welk celweefsel kan stoffen absorberen en of scheiden?
- Waar wordt het paramecium gevonden in een menselijk lichaam?
- Bepaling van de optimale temperatuur voor enzymactiviteit

- Hoe oplosbaarheid wordt gekwantificeerd:eenheden en definities
- Chemici ontwikkelen nieuwe blauwdruk voor enzym betrokken bij kanker
- Het beste van twee werelden:hoge entropie ontmoet lage dimensies, opent oneindige mogelijkheden

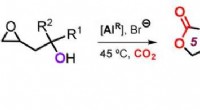
- Cascades met kooldioxide
 Welke organellen hebben kegelcellen?
Welke organellen hebben kegelcellen?  Sociale media voor seksuele voorlichting:Zuid-Afrikaanse tieners leggen uit hoe het hen zou helpen
Sociale media voor seksuele voorlichting:Zuid-Afrikaanse tieners leggen uit hoe het hen zou helpen  Waarom kunnen we planeten zien, ook al zijn ze geen lichtbron?
Waarom kunnen we planeten zien, ook al zijn ze geen lichtbron?  Wat gebeurt er met de opgeslagen chemische energie in droge cel wanneer de schakelaar is gesloten?
Wat gebeurt er met de opgeslagen chemische energie in droge cel wanneer de schakelaar is gesloten?  Wat is de naam van explosieve typen vulkanen?
Wat is de naam van explosieve typen vulkanen?  DNA is beter bestand tegen hydrolyse dan RNA Welk kenmerk van verantwoordelijk voor dit kenmerk?
DNA is beter bestand tegen hydrolyse dan RNA Welk kenmerk van verantwoordelijk voor dit kenmerk?  Wat is Supplex Nylon?
Wat is Supplex Nylon?  Wetenschapsactiviteiten voor 3- tot 5-jarigen
Wetenschapsactiviteiten voor 3- tot 5-jarigen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

