
Wetenschap
Covalente bindingen:het delen van elektronen in de chemie begrijpen
Hier is een overzicht:
* Covalente bindingen treedt op wanneer twee of meer atomen elektronen delen in hun buitenste schillen (valentieschillen). Door dit delen kunnen de atomen een stabiele elektronenconfiguratie bereiken, vergelijkbaar met die van edelgassen.
* De gedeelde elektronen worden aangetrokken door de kernen van beide atomen en houden ze bij elkaar.
* Covalente bindingen kunnen enkel, dubbel of drievoudig zijn , afhankelijk van het aantal gedeelde elektronenparen.
Hier zijn enkele belangrijke kenmerken van covalente bindingen:
* Sterke banden: Covalente bindingen zijn over het algemeen sterker dan andere soorten obligaties, zoals ionische bindingen.
* Richting: Covalente bindingen hebben een specifieke directionaliteit, wat betekent dat de gedeelde elektronen zich tussen de twee kernen bevinden. Hierdoor krijgen moleculen een specifieke vorm.
* Niet-polair en polair: Covalente bindingen kunnen niet-polair zijn (gelijke verdeling van elektronen) of polair (ongelijke verdeling van elektronen).
Voorbeelden van moleculen gevormd door covalente bindingen:
* Water (H2O) :Elk waterstofatoom deelt één elektron met het zuurstofatoom en vormt twee enkele covalente bindingen.
* Kooldioxide (CO2) :Het koolstofatoom deelt twee elektronen met elk zuurstofatoom en vormt twee dubbele covalente bindingen.
* Methaan (CH4) :Het koolstofatoom deelt één elektron met elk van de vier waterstofatomen en vormt vier enkele covalente bindingen.
Laat het me weten als je meer wilt weten over specifieke soorten covalente bindingen of de eigenschappen van de moleculen die daardoor worden gevormd.
 Wat trekt dingen naar de aarde?
Wat trekt dingen naar de aarde?  Verlies van individualiteit als gevolg van genetische manipulatie
Verlies van individualiteit als gevolg van genetische manipulatie Brazilië:het aantal gebruiksdagen van airconditioningapparatuur zal verdubbelen zonder klimaatactie
Brazilië:het aantal gebruiksdagen van airconditioningapparatuur zal verdubbelen zonder klimaatactie Het schatten van het emissiepotentieel van buiten gebruik gestelde gasbronnen op basis van schaliemonsters
Het schatten van het emissiepotentieel van buiten gebruik gestelde gasbronnen op basis van schaliemonsters  Onderzoek naar aardbevingen in Kaikoura suggereert nieuwe benadering van aardbevingsvoorspelling
Onderzoek naar aardbevingen in Kaikoura suggereert nieuwe benadering van aardbevingsvoorspelling
Hoofdlijnen
- Bevatten alle diploïde cellen in het menselijk lichaam hetzelfde genetische materiaal?
- Hoe zien de bewakingscellen en de huidmondjes eruit?
- Hoe activeert nematodeninfectie de afweerreactie van planten in sojabonen?
- Hoe verschilt selectief fokken van evolutie?
- Cellen groeien en delen met een abnormaal hoge snelheid in?
- Anabolisme:hoe verteerd voedsel de groei en het herstel van weefsel stimuleert
- Waar doen in de cel replicatie -vertaling en transcriptie zich voor?
- Welke wet stelt dat één alele van elk genenpaar naar sekscel gaat?
- Wat zijn de soorten stamcellen?
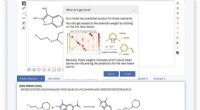
- Neurale netwerken gebruiken om resultaten van organische chemie te voorspellen
- Onderzoekers ontdekken een nieuw mechanisme dat de polariteit van vlakke cellen reguleert
- Hoogrenderende katalysator verbetert de elektrische reductieprestaties van kooldioxide

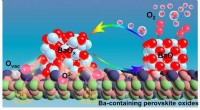
- Mechanisme van zuurstofactivering op bariumbevattende perovskietmaterialen
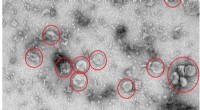
- Niet-invasieve diagnose van prostaatkanker, toezicht houden

 Nieuwe robot voor schedelbasischirurgie is zeer nauwkeurig, verlicht de werklast van chirurgen
Nieuwe robot voor schedelbasischirurgie is zeer nauwkeurig, verlicht de werklast van chirurgen Wat is de voedingsspanning in ons?
Wat is de voedingsspanning in ons?  Niet voor altijd:grootste roze diamantmijn ter wereld gaat dicht
Niet voor altijd:grootste roze diamantmijn ter wereld gaat dicht Hoeveel elektronen doneert één atoom van calcium aan zuurstof tijdens de Formation -verbinding Cao?
Hoeveel elektronen doneert één atoom van calcium aan zuurstof tijdens de Formation -verbinding Cao?  Wat is de eerste atoomtheorie?
Wat is de eerste atoomtheorie?  Belt E.T. een slimme zet?
Belt E.T. een slimme zet?  Hoe denkt u dat het vermogen verloren gaat als warmte in elektriciteit?
Hoe denkt u dat het vermogen verloren gaat als warmte in elektriciteit?  Welke energiebronnen vormen de meerderheid van de werelden die leveren?
Welke energiebronnen vormen de meerderheid van de werelden die leveren?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

