
Wetenschap
Valentie-elektronen:alkalische en aardalkalimetalen uitgelegd
Dit is waarom:
* Alkalimetalen (Groep 1): Deze elementen hebben één elektron in hun buitenste (valentie) schil. Ze zijn zeer reactief en hebben de neiging dit elektron te verliezen en positief geladen ionen met een lading van +1 te vormen. Voorbeelden zijn onder meer lithium (Li), natrium (Na) en kalium (K).
* Aardalkalimetalen (Groep 2): Deze elementen hebben twee elektronen in hun valentieschil. Ze zijn ook reactief, maar minder dan alkalimetalen. Ze hebben de neiging deze twee elektronen te verliezen en positief geladen ionen te vormen met een lading van +2. Voorbeelden hiervan zijn beryllium (Be), magnesium (Mg) en calcium (Ca).
Belangrijke opmerking: Hoewel het aantal valentie-elektronen deze groepen definieert, zijn er andere factoren die hun chemisch gedrag beïnvloeden.
 Wat planten ons kunnen leren over het opruimen van olievlekken en microfluïdica
Wat planten ons kunnen leren over het opruimen van olievlekken en microfluïdica  Een nieuwe manier om te zien of die plastic fles of zak gerecycled materiaal bevat
Een nieuwe manier om te zien of die plastic fles of zak gerecycled materiaal bevat Wetenschappers onderzoeken hoe verschillende vloeibare organellen in cellen worden gemaakt
Wetenschappers onderzoeken hoe verschillende vloeibare organellen in cellen worden gemaakt Wat is de enige voedingsstof die elementstikstof bevat?
Wat is de enige voedingsstof die elementstikstof bevat?  Een niet-equivalente co-gedoteerde strategie om de elektrische eigenschappen van piëzo-elektrische keramiek te verbeteren
Een niet-equivalente co-gedoteerde strategie om de elektrische eigenschappen van piëzo-elektrische keramiek te verbeteren
 Bijna 6 miljoen kinderen worden door de hete, droge ploegen van een sterke El Niño
Bijna 6 miljoen kinderen worden door de hete, droge ploegen van een sterke El Niño Het planten van een groenbedekkende gewasstrategie kan boeren helpen om met natte bronnen om te gaan
Het planten van een groenbedekkende gewasstrategie kan boeren helpen om met natte bronnen om te gaan Studie analyseert de ecologische duurzaamheid van diëten bij kinderen en adolescenten
Studie analyseert de ecologische duurzaamheid van diëten bij kinderen en adolescenten  Door meer dan de bomen het bos zien:behoud toevoegen aan holistische ontwikkeling
Door meer dan de bomen het bos zien:behoud toevoegen aan holistische ontwikkeling De impact van deeltjesvervuiling varieert sterk, afhankelijk van waar het vandaan komt
De impact van deeltjesvervuiling varieert sterk, afhankelijk van waar het vandaan komt
Hoofdlijnen
- Een garnalenverhaal - winnaars en verliezers in klimaatverandering
- Noorwegen zet hek op om rendierslachting te stoppen
- Nieuw onderzoek onthult aanwijzingen over hoe antilichamen verfijnd worden om infecties te bestrijden
- Wat is de locatie en rol van het lymfestelsel?
- Wat is de naam van het proces in levende organismen die warmte veroorzaakt?
- Hoe een virus zijn symmetrische omhulsels vormt
- Nieuwe celvrije eiwitkristallisatiemethode om structurele biologie te bevorderen
- Is er een manier om te voorkomen dat de hond van Biden mensen bijt?
- Waarom pijlgifkikkers dat zelf niet doen
- Nieuw onderzoek maakt de weg vrij voor het simuleren van katalysatoren onder reactieomstandigheden

- Wat WD-40 werkelijk betekent

- Nieuwe software om waardevolle verbindingen te ontdekken

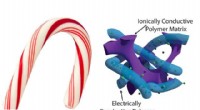
- Supercondensator met snoepriet kan snel opladen van mobiele telefoons mogelijk maken
- Kunstmatig longkankerweefsel kan helpen bij het vinden van nieuwe medicamenteuze behandelingen

 Wat zijn het gebruik van metaalcarbonaten?
Wat zijn het gebruik van metaalcarbonaten?  Waarom wordt koolstof geclassificeerd als een element in plaats van als verbinding?
Waarom wordt koolstof geclassificeerd als een element in plaats van als verbinding?  Blast de wind de hele nacht?
Blast de wind de hele nacht?  Nanodeeltjes richten zich op meerdere COVID-varianten via de twist in het spike-eiwit
Nanodeeltjes richten zich op meerdere COVID-varianten via de twist in het spike-eiwit  Moleculaire bibliotheken voor organische lichtemitterende diodes
Moleculaire bibliotheken voor organische lichtemitterende diodes Mechanische eigenschappen van viraal DNA bepalen het verloop van infectie
Mechanische eigenschappen van viraal DNA bepalen het verloop van infectie Waarom we kin hebben:Onderzoekers beweren dat de kin voortkomt uit evolutie, en niet uit mechanische krachten
Waarom we kin hebben:Onderzoekers beweren dat de kin voortkomt uit evolutie, en niet uit mechanische krachten  Nieuw beschreven algensoorten maken koralen sterker om opwarmende oceanen te doorstaan
Nieuw beschreven algensoorten maken koralen sterker om opwarmende oceanen te doorstaan
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

