
Wetenschap
Metaalzuiverheid en stabiliteit:het verschil begrijpen tussen metalen en ertsen
* Oxidatietoestand: Ertsen zijn verbindingen waarin het metaal zich in een gecombineerde toestand bevindt, vaak met zuurstof of andere elementen. Dit betekent dat het metaalatoom elektronen heeft verloren en zich in een hogere oxidatietoestand bevindt. Zuivere metalen hebben daarentegen een neutrale oxidatietoestand.
* Reactiviteit: Metalen in ertsen zijn vaak reactiever vanwege hun hogere oxidatietoestand. Het is waarschijnlijker dat ze verdere reacties en transformaties ondergaan. Zuivere metalen zijn minder reactief en stabieler.
* Energiestatus: Er is energie nodig om het metaal uit het erts te halen, de bindingen te verbreken en het metaal terug te brengen naar zijn elementaire staat. Dit suggereert dat het pure metaal zich in een lagere energietoestand bevindt en daarom stabieler is.
Voorbeeld: IJzererts (Fe2O3) is minder stabiel dan puur ijzer (Fe). Het ijzer in het erts is geoxideerd, terwijl het zuivere ijzer zich in zijn elementaire vorm bevindt. Om zuiver ijzer te verkrijgen, moeten we het ijzeroxide reduceren in een proces op hoge temperatuur, waarvoor energie nodig is.
Uitzonderingen:
* Edelmetalen: Sommige metalen, zoals goud en platina, komen van nature in hun pure vorm voor. Ze zijn inherent minder reactief en bevinden zich al in hun meest stabiele vorm.
* Legeringen: Sommige legeringen, mengsels van verschillende metalen, kunnen stabieler zijn dan hun afzonderlijke componenten. De combinatie van metalen kan een resistentere structuur creëren.
Samenvattend: Hoewel er uitzonderingen zijn, zijn zuivere metalen over het algemeen stabieler dan hun ertsen vanwege hun lagere oxidatietoestand, verminderde reactiviteit en lagere energietoestand.
 Wereld staat voor zware klimaatstrijd nu de Amerikaanse inspanningen te kort schieten
Wereld staat voor zware klimaatstrijd nu de Amerikaanse inspanningen te kort schieten Suomi NPP vindt ongeorganiseerde stormen in tropische depressie 29W
Suomi NPP vindt ongeorganiseerde stormen in tropische depressie 29W Rockfalls, gapende spleten maken de Mont Blanc voor velen buiten bereik
Rockfalls, gapende spleten maken de Mont Blanc voor velen buiten bereik Mangrovebossen slaan meer koolstof op als ze diverser zijn
Mangrovebossen slaan meer koolstof op als ze diverser zijn Nieuwe techniek identificeert microverontreinigingen in New Yorkse waterwegen
Nieuwe techniek identificeert microverontreinigingen in New Yorkse waterwegen
Hoofdlijnen
- Wat wordt cellulaire ademhaling uitgevoerd door?
- Welke cel is draadachtig en verzendt berichten?
- Wat zijn de toepassingen van elektroforese?
- Vertrouwen op GPS voorkomt dat delen van uw hersenen worden geactiveerd
- Welke structuren moeten organismen die geen celwand missen, ondersteuning bieden?
- Wat is de functie van eiwitten en carbhydraten die zijn ingebed in een celmembraan?
- Hoe vindt de uitscheiding plaats in eencellige organismen?
- De definitie van lichaamssystemen
- Is deze geit de GEIT? Kind met lange oren verovert Pakistan stormenderhand
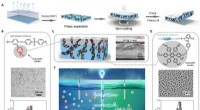
- Een efficiëntere op membraan gebaseerde generator voor het oogsten van osmotisch vermogen (update)
- Dubbele vervangingsreacties uitgelegd:hoe ionen gassen uitwisselen, neerslaan of vormen

- Een uitvinding maakt de productie van een natuurlijke zoetstof mogelijk
- Ongebruikelijke kobaltverbinding ontwikkeld voor dunnefilmproductie

- Antivries van de natuur inspireert revolutionaire cryopreservatietechniek voor bacteriën
 Als een geladen staaf dicht bij een elektroscoop wordt gebracht en vervolgens wordt verwijderd, wordt het?
Als een geladen staaf dicht bij een elektroscoop wordt gebracht en vervolgens wordt verwijderd, wordt het?  Onderzoek details regulering van een multi-drug transporter
Onderzoek details regulering van een multi-drug transporter Hoeveel waterstofatomen zijn er in 0,1262 mol H2SO4?
Hoeveel waterstofatomen zijn er in 0,1262 mol H2SO4?  Welke plantcellen zwemmen eigenlijk?
Welke plantcellen zwemmen eigenlijk?  Elektronensubschaalvormen begrijpen:het hoekmomentumkwantumgetal (l)
Elektronensubschaalvormen begrijpen:het hoekmomentumkwantumgetal (l)  Als Rusland vertrekt, wat is de volgende stap voor het internationale ruimtestation?
Als Rusland vertrekt, wat is de volgende stap voor het internationale ruimtestation? Nanodiamanten kunnen worden gebruikt bij de diagnose van ziekten
Nanodiamanten kunnen worden gebruikt bij de diagnose van ziekten Wat is 0,000000000025 in wetenschappelijke notatie?
Wat is 0,000000000025 in wetenschappelijke notatie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

