
Wetenschap
Dubbele vervangingsreacties uitgelegd:hoe ionen gassen uitwisselen, neerslaan of vormen
omega77/iStock/GettyImages
Een dubbele vervangingsreactie (dubbele verplaatsingsreactie) vindt plaats wanneer twee oplosbare zouten dissociëren in water, en hun kationen en anionen partners uitwisselen en twee nieuwe producten vormen. De reactie verloopt in waterige oplossing; de producten kunnen in oplossing blijven, zich ontwikkelen als een gas of neerslaan als een onoplosbare vaste stof.
TL;DR
Bij een dubbele vervangingsreactie wisselen ionen van plaats, wat leidt tot een neerslag of een zuur-base-reactie. Oplosbaarheidsregels bepalen of een vaste stof neerslaat, een gas ontstaat of de producten in oplossing blijven.
Hoe de reactie plaatsvindt
Overweeg twee generieke zouten, AB en CD. In water dissociëren ze in A + + B – en C + + D – . Omdat gelijke ladingen elkaar afstoten, recombineren de kationen en anionen om de nieuwe paren AD en CB te vormen. Afhankelijk van hun oplosbaarheid kunnen AD en CB verschijnen als een vast neerslag, opgelost blijven of een gas vormen.
Oplosbaarheidsregels
Oplosbaarheidsregels zijn essentieel voor het voorspellen van de uitkomst van een dubbele vervangingsreactie. Als een van beide reactanten onoplosbaar is, zal deze niet deelnemen. De meest gebruikte regels zijn:
- Alleen nitraat (NO3 ⁻) zouten zijn oplosbaar.
- Alkalimetaalzouten (Li + , Na + , K + , Rb + , Cs + ) zijn oplosbaar.
- Ammonium (NH4 + ) zouten zijn oplosbaar.
- De meeste halogenidezouten (Cl – , Br – , ik – ) zijn oplosbaar, behalve Ag + , Hg2 2+ , en Pb 2+ .
- De meeste sulfaatzouten (SO4 2– ) zijn oplosbaar, behalve Ca 2+ , Hg2 2+ , Pb 2+ , en Ba 2+ .
- De meeste hydroxidezouten zijn onoplosbaar, behalve Ca 2+ , Ba 2+ , en Sr 2+ .
- De meeste sulfide-, carbonaat-, fosfaat- en chromaatzouten zijn onoplosbaar, behalve die van alkalimetalen en NH4 + .
Neerslagreacties
Wanneer twee oplosbare zouten worden gemengd, is een veelvoorkomend resultaat de vorming van een onoplosbare vaste stof. Door bijvoorbeeld zinknitraat (Zn(NO3 )2 ) en natriumfosfaat (Na3 PO4 ) produceert natriumnitraat, dat in oplossing blijft, en zinkfosfaat (Zn3 (PO4 )2 ), wat neerslaat:
Zn(NO3 )2 (aq) + Na3 PO4 (aq) → 3NaNO3 (aq) + Zn3 (PO4 )2 (s)
Zuur-base-vervangingsreacties
Zuren en basen nemen ook deel aan dubbele vervangingsreacties. In oplossing doneert een zuur H + , terwijl een base OH – levert . De H + en OH – combineren om water te vormen, en de resterende ionen vormen een zout. Bijvoorbeeld:
HCl (aq) + NaOH (aq) → NaCl (aq) + H2 O (l)
In een complexer geval reageert natriumcarbonaat met zoutzuur, waarbij natriumchloride, kooldioxidegas en water ontstaan:
Na2 CO3 (aq) + 2HCl (aq) → 2NaCl (aq) + CO2 (g) + 3H2 O (l)
Deze voorbeelden illustreren hoe de oplosbaarheid van de reactanten en de identiteit van de ionen bepalen of er een neerslag, gas of oplosbaar zout ontstaat.
Voor onduidelijke gevallen waarin de producten oplosbaar blijven, zijn vaak aanvullende tests (bijvoorbeeld pH-meting, geleidbaarheid of spectroscopische analyse) nodig om te bevestigen dat er een reactie heeft plaatsgevonden.
 Een essentiële leemte in klimaatmodellen opvullen
Een essentiële leemte in klimaatmodellen opvullen Hoe berichtgeving het vertrouwen van het publiek in de wetenschap beïnvloedt
Hoe berichtgeving het vertrouwen van het publiek in de wetenschap beïnvloedt  Is een eucalyptus boom herbivore carnivore of omnivore?
Is een eucalyptus boom herbivore carnivore of omnivore?  Wat beschrijft de relatie tussen diepte en verdeling van het leven in een aquatisch ecosysteem?
Wat beschrijft de relatie tussen diepte en verdeling van het leven in een aquatisch ecosysteem?  NASA krijgt infraroodbeeld van Carolina Chris, de tropische storm
NASA krijgt infraroodbeeld van Carolina Chris, de tropische storm
Hoofdlijnen
- Wat doet de mitochandria voor cel?
- Wat is de locatie van het produceren van ribosomaal RNA?
- Wanneer wordt een mutatie in een DNA-molecuul doorgegeven aan nakomelingen?
- Hoe is de creatie van een nieuwe soort die wordt genoemd?
- Wat zijn de kenmerken die worden gebruikt om organismen in twee domeinen te classificeren?
- Welke groepen mensen hebben de neiging hun IQ te overschatten?
- Welk type celdeling mitose of meiose wordt gekenmerkt door groeiherstel en aseksuele reproduciton?
- Hoeveel cellen worden er gevormd tijdens mitose en ze identiek?
- Helpt osmose een cel bij het ontvangen van voeding?
- Klikreactie voor levende systemen:Bioorthogonale hydroaminering van geactiveerde lineaire alkynen

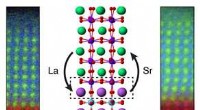
- Het benutten van verloren atomen kan helpen bij het maken van nieuwe, nooit eerder vertoonde oxiden
- De energieniveaus van organische halfgeleiders afstemmen

- Chemici leren computerprogramma's om krachten tussen atomen nauwkeurig te modelleren

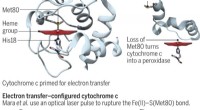
- Energetische kosten van de entatische toestand van cytochroom c gekwantificeerd
 Wat is een transgene organisme?
Wat is een transgene organisme?  Ghost Train Station is symbolische hoop op Koreaanse hereniging
Ghost Train Station is symbolische hoop op Koreaanse hereniging  Het vulkanische eiland Japan kan de sleutel zijn tot het overleven van koraal
Het vulkanische eiland Japan kan de sleutel zijn tot het overleven van koraal Nieuw proces verandert papierproductieafval in waardevolle chemicaliën
Nieuw proces verandert papierproductieafval in waardevolle chemicaliën Wat gebeurt er als organismen een nieuw gebied vullen en geografisch geïsoleerd zijn van andere populaties van dezelfde soort?
Wat gebeurt er als organismen een nieuw gebied vullen en geografisch geïsoleerd zijn van andere populaties van dezelfde soort?  Oude jagers bleven in het bevroren Noord-Europa in plaats van te migreren, bewijs van botten van poolvossen toont
Oude jagers bleven in het bevroren Noord-Europa in plaats van te migreren, bewijs van botten van poolvossen toont Wordt generator gebruikt voor kernenergie?
Wordt generator gebruikt voor kernenergie?  Zijn er plannen om Moon te terravormen?
Zijn er plannen om Moon te terravormen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

