
Wetenschap
Hoeveel waterstofatomen zijn er in 0,1262 mol H2SO4?
1. Begrijp de chemische formule:
* H₂so₄ vertegenwoordigt zwavelzuur.
* Het subscript "2" na de waterstof (H) geeft aan dat er twee waterstofatomen zijn in elk molecuul zwavelzuur.
2. Avogadro's nummer:
* Het nummer van Avogadro vertelt ons het aantal deeltjes (atomen, moleculen, enz.) In één mol van een stof. Het is ongeveer 6.022 x 10²³ deeltjes/mol.
3. Berekeningen:
* Stap 1: Bereken het aantal H₂so₄ -moleculen in 0,1262 mol:
0,1262 mol H₂so₄ x (6.022 x 10²³ Moleculen/mol) =7,60 x 10²² moleculen van h₂so₄
* Stap 2: Bereken het totale aantal waterstofatomen:
7.60 x 10²² moleculen van H₂so₄ x (2 H atomen/molecuul) =1,52 x 10²³ Waterstofatomen
Antwoord: Er zijn ongeveer 1,52 x 10²³ waterstofatomen in 0,1262 mol H₂so₄.
 Hoe berekent u de massa van 1,5 mol zuurstofmolecuul?
Hoe berekent u de massa van 1,5 mol zuurstofmolecuul?  Eenvoudige interesse vinden
Eenvoudige interesse vinden  Wat is de chemische term voor het verbranden van een brandstof?
Wat is de chemische term voor het verbranden van een brandstof?  Wat is het enige subatomaire deeltje dat direct betrokken is bij chemische reacties tussen atomen?
Wat is het enige subatomaire deeltje dat direct betrokken is bij chemische reacties tussen atomen?  Hoe te vinden hoeveel Mollen in een samenstelling zitten
Hoe te vinden hoeveel Mollen in een samenstelling zitten
 Gemeenschappelijke carnivoren in het gematigde woud
Gemeenschappelijke carnivoren in het gematigde woud  Wie is de auteur van of een boom in het bos valt en niemand in de buurt om te horen dat het geluid maakt?
Wie is de auteur van of een boom in het bos valt en niemand in de buurt om te horen dat het geluid maakt?  Minder vliegen? Wordt veganist? Hoe mensen klimaatactie kunnen ondernemen
Minder vliegen? Wordt veganist? Hoe mensen klimaatactie kunnen ondernemen Olie, gasreuzen kunnen biljoenen verspillen in een 2C-wereld:rapport
Olie, gasreuzen kunnen biljoenen verspillen in een 2C-wereld:rapport Drie manieren waarop het maken van een smartphone het milieu kan schaden
Drie manieren waarop het maken van een smartphone het milieu kan schaden
Hoofdlijnen
- Wat betekent het testen van de lymfoproliferatieve respons van mononucleaire cellen op polyklonale stimulatoren?
- Deskundigen ontwikkelen een manier om CRISPR-technologie te gebruiken om antimicrobiële resistentie aan te pakken
- Onderzoekers identificeren sleutelfactor in exosoom-gemedieerde virale transmissie van insecten naar planten
- Wat is de logica van de wetenschap?
- Welke structuren worden over het algemeen aangetroffen in prokaryotische cellen?
- Roundworms hebben spierweefsel en een darm met één opening?
- Waar komen haarcellen daar nuritioment vandaan?
- Wat is de definitie van merk -DNA?
- Hoe heeft technologie de manier veranderd waarop biologen levende wezens bestuderen, om een voorbeeld te geven?
- Mineraal ondergaat zelfgenezing van stralingsschade

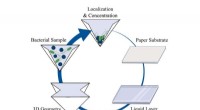
- Gevouwen papier creëert een draagbaar laboratorium voor veldlaboratoriumtests
- Nieuwe glasmaterialen gemaakt van organische en anorganische componenten

- Onderzoekers ontdekken een nieuwe gunstige functie van een oud eiwit
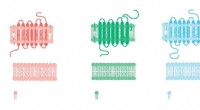
- Oppervlakken die als gekkovoeten vastgrijpen, kunnen gemakkelijk in massa worden geproduceerd

 Verschil tussen kwartsiet en graniet
Verschil tussen kwartsiet en graniet  Welk object heeft een constante snelheid?
Welk object heeft een constante snelheid?  Robots die als groep werken, kunnen de optimale volgorde van hun taken bepalen
Robots die als groep werken, kunnen de optimale volgorde van hun taken bepalen Tundra Klimaatfeiten
Tundra Klimaatfeiten  Bedrijven zijn klaar voor de totale zonsverduistering van april met donuts en bier met een hemels thema
Bedrijven zijn klaar voor de totale zonsverduistering van april met donuts en bier met een hemels thema  NASA lanceert door studenten gebouwd experiment door USU de ruimte in
NASA lanceert door studenten gebouwd experiment door USU de ruimte in Hoe houden zwaartekracht en traagheid de planeten in een baan om de aarde?
Hoe houden zwaartekracht en traagheid de planeten in een baan om de aarde?  Welke fysieke eigenschap kan worden bepaald door de verhouding van massa tot volume te vinden?
Welke fysieke eigenschap kan worden bepaald door de verhouding van massa tot volume te vinden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

