
Wetenschap
Elektronensubschaalvormen begrijpen:het hoekmomentumkwantumgetal (l)
Hier is een overzicht:
* Hoofdkwantumgetal (n): Bepaalt het energieniveau van het elektron.
* Kwantumgetal van impulsmoment (l): Bepaalt de vorm van de orbitaal van het elektron. Het kan waarden hebben variërend van 0 tot n-1.
* l =0:s orbitaal (bolvormig)
* l =1:p orbitaal (haltervormig)
* l =2:d orbitaal (complexere vormen)
* l =3:f orbitaal (nog complexere vormen)
* Magnetisch kwantumgetal (ml): Bepaalt de oriëntatie van de orbitaal in de ruimte.
* Spinkwantumgetal (ms): Beschrijft het intrinsieke impulsmoment van een elektron, vaak 'spin' genoemd.
Om de vorm van een elektronensubschil te bepalen, moet je dus kijken naar de waarde van het kwantumgetal van het impulsmoment (l) .
 Geometrie-adaptieve elektrokatalyse:de voorgestelde aanpak zou de efficiëntie van energieconversietechnologieën kunnen verdubbelen
Geometrie-adaptieve elektrokatalyse:de voorgestelde aanpak zou de efficiëntie van energieconversietechnologieën kunnen verdubbelen  Selectieve olefine-metathese met dubbele golflengte 3D-printen:hoe ingenieurs SWOMP gebruiken
Selectieve olefine-metathese met dubbele golflengte 3D-printen:hoe ingenieurs SWOMP gebruiken  Chemici ontwikkelen nieuwe Washington Red-kleurstof voor bio-imaging
Chemici ontwikkelen nieuwe Washington Red-kleurstof voor bio-imaging Hoe verkrijgt u een zuiver en droog monster van natriumchloridezout?
Hoe verkrijgt u een zuiver en droog monster van natriumchloridezout?  Wat zijn de ingrediënten van ferro sulfaat?
Wat zijn de ingrediënten van ferro sulfaat?
Hoofdlijnen
- Wat slaat voedsel of pigment in een cel op?
- Hoe zeealgen de wereld kunnen helpen voeden
- Waarom noemde DNA de blauwdruk van het leven?
- Wat is een groep organismen die opnieuw is geclassificeerd?
- Hebben prokaryote cellen een aparte kern?
- Studie:Hoe we omgaan met dieren werpt licht op de Amerikaanse sociale ongelijkheid
- Wat gebeurt er met voedsel en energie als lysosomen de cel binnenkomen?
- Wat zijn enkele praktische toepassingen van biotechnologie?
- Kijkend naar een cel onder microscoop, merkt u op dat deze Prokarote is?
- Topologische zaken:op weg naar een nieuw soort transistor

- Optische pincettechnologie aangepast om de gevaren van hitte te overwinnen

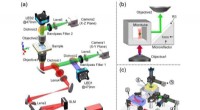
- Gelijktijdige optische trapping en beeldvorming in het axiale vlak voor interactie tussen licht en materie
- Licht dat wordt gebruikt om kwantuminformatie te detecteren die is opgeslagen in 100, 000 nucleaire kwantumbits

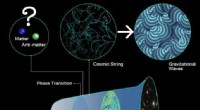
- Laat zien hoe de kleinste deeltjes in ons universum ons hebben gered van volledige vernietiging
 UITLEGGER:Waarom India herhaaldelijk problemen heeft met de luchtverontreiniging
UITLEGGER:Waarom India herhaaldelijk problemen heeft met de luchtverontreiniging  Wat is de afsluiting van een biochemisch pad veroorzaakt door belangrijke enzymengevoeligheid voor het product van niveau paden?
Wat is de afsluiting van een biochemisch pad veroorzaakt door belangrijke enzymengevoeligheid voor het product van niveau paden?  Wanneer de cellen van een organisme toenemen in aantal grootte of volume, wordt dit genoemd?
Wanneer de cellen van een organisme toenemen in aantal grootte of volume, wordt dit genoemd?  Wat is het laagste niveau van biologische organisatie om kenmerken te hebben leven?
Wat is het laagste niveau van biologische organisatie om kenmerken te hebben leven?  Google's autonome voertuigeenheid om semis te testen in Atlanta
Google's autonome voertuigeenheid om semis te testen in Atlanta Wat onderscheidt een eukaryotische cel van prokaryotische celln is de aanwezigheid van?
Wat onderscheidt een eukaryotische cel van prokaryotische celln is de aanwezigheid van?  Een nanostructuur die de groei van stamcellen stimuleert voor de behandeling van de ziekte van Parkinson
Een nanostructuur die de groei van stamcellen stimuleert voor de behandeling van de ziekte van Parkinson Onderzoek ontsluit potentieel van superverbinding
Onderzoek ontsluit potentieel van superverbinding
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

