
Wetenschap
Covalente obligaties:het delen van elektronen en de octetregel begrijpen
Dit is waarom:
* Valentie-elektronen: Dit zijn de elektronen in de buitenste schil van een atoom, die betrokken zijn bij chemische binding.
* Octetregel: Hoofdgroepelementen hebben de neiging elektronen te winnen, te verliezen of te delen om een stabiele elektronenconfiguratie met acht valentie-elektronen te bereiken (zoals een edelgas).
* Covalente binding: Atomen delen elektronen om deze stabiele configuratie te bereiken.
Voorbeeld:
Beschouw het molecuul zuurstof (O2). Elk zuurstofatoom heeft zes valentie-elektronen. Om een octet te bereiken, deelt elk zuurstofatoom twee van zijn elektronen met het andere zuurstofatoom. Dit resulteert in een dubbele binding met in totaal vier gedeelde elektronen (twee van elk atoom).
Hoewel het in sommige gevallen mogelijk is dat atomen meer dan acht elektronen delen (vooral bij overgangsmetalen), is dit niet gebruikelijk voor hoofdgroepelementen.
 Inzicht in gecompliceerde Arctische cloudprocessen
Inzicht in gecompliceerde Arctische cloudprocessen Laat verontreinigd Fukushima-water vrij in zee:Japan panel
Laat verontreinigd Fukushima-water vrij in zee:Japan panel Hoe schildpadden groeien en leven
Hoe schildpadden groeien en leven  Wetenschappers dragen bij aan belangrijk nieuw rapport over de impact van klimaatverandering op Britse kusten en zeeën
Wetenschappers dragen bij aan belangrijk nieuw rapport over de impact van klimaatverandering op Britse kusten en zeeën Meteoor waarschijnlijk oorzaak van felle flits in de nachtelijke hemel van Florida
Meteoor waarschijnlijk oorzaak van felle flits in de nachtelijke hemel van Florida
Hoofdlijnen
- Wat zijn 22 takken van biologie?
- Wat is de definitie die ten grondslag ligt aan ziekte?
- Wat kan schadelijk zijn als het de kansen voor overleven en reproductie vermindert?
- Wat is bedoeld door biologisch afbreekbaar?
- De persoon die voor het eerst een ietwat ruwe manier van classificatie voor organismen ontwikkelde, was?
- Hoe groter een kern is, hoe groter de kern is?
- Ontdekking van DNA-uitschakelingsmechanisme onthult hoe planten hun genoom beschermen
- Vloeibaar gedeelte van een cel wordt genoemd?
- Wat is de relatie tussen het darwinisme en het communisme?
- Geheimen van Lucretia schilderij dichter bij onthulling

- Verbinding van geneeskrachtig kruid doodt hersenetende amoeben in laboratoriumstudies

- Onderzoekers gebruiken een synthetische tong om whisky's te sorteren
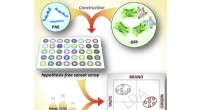
- Chemici ontwikkelen nieuw materiaal voor het scheiden van kooldioxide uit industriële afvalgassen

- Innovatieve verwerking en verpakking voor veilige, hoge kwaliteit, biologische bessenproducten

 Hoe vrije radicalen uw lichaam beïnvloeden
Hoe vrije radicalen uw lichaam beïnvloeden  Bioaccumulatie van uitgefaseerde brandvertragers neemt langzaam af bij Amerikaanse zeearenden
Bioaccumulatie van uitgefaseerde brandvertragers neemt langzaam af bij Amerikaanse zeearenden Wees de verandering die je in de wereld wilt zien:hoe individuen kunnen helpen de planeet te redden van een klimaatcatastrofe
Wees de verandering die je in de wereld wilt zien:hoe individuen kunnen helpen de planeet te redden van een klimaatcatastrofe Is Pluto het enige lichaam in het zonnestelsel met een elliptische baan?
Is Pluto het enige lichaam in het zonnestelsel met een elliptische baan?  Welke toestand van materie heeft een duidelijk volume of vorm?
Welke toestand van materie heeft een duidelijk volume of vorm?  Wat wordt afgebroken van voedselmoleculen?
Wat wordt afgebroken van voedselmoleculen?  Heeft u een speciale dimmerschakelaar nodig om MR 16 halogeenlichten te regelen?
Heeft u een speciale dimmerschakelaar nodig om MR 16 halogeenlichten te regelen?  Woestijnschade:de donkere kant van zonne-energie?
Woestijnschade:de donkere kant van zonne-energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

