
Wetenschap
Atomaire reactiviteit begrijpen:de rol van elektronen
* Valentie-elektronen: Dit zijn de elektronen in het buitenste energieniveau van een atoom. Zij zijn degenen die betrokken zijn bij chemische binding.
* Elektronenconfiguratie: Dit beschrijft hoe elektronen worden verdeeld binnen de verschillende energieniveaus en orbitalen van een atoom.
Hier ziet u hoe deze factoren de reactiviteit beïnvloeden:
* Atomen hebben de neiging stabiliteit te bereiken: Atomen zijn het meest stabiel als hun buitenste schil (valentieschil) vol is. Dit wordt vaak bereikt door elektronen te winnen, te verliezen of te delen om te lijken op de elektronenconfiguratie van een edelgas, dat volledige valentieschillen heeft en zeer niet-reactief is.
* Elektronegativiteit: Dit is een maatstaf voor het vermogen van een atoom om elektronen aan te trekken in een chemische binding. Atomen met een hoge elektronegativiteit hebben de neiging elektronen te winnen, terwijl atomen met een lage elektronegativiteit de neiging hebben elektronen te verliezen.
* Ionisatie-energie: Dit is de energie die nodig is om een elektron uit een atoom te verwijderen. Atomen met een lage ionisatie-energie verliezen gemakkelijk elektronen, terwijl atomen met een hoge ionisatie-energie hun elektronen stevig vasthouden.
Samengevat: De reactiviteit van een atoom wordt bepaald door zijn wens om een stabiele elektronenconfiguratie te bereiken, die wordt beïnvloed door het aantal valentie-elektronen en de elektronegativiteit en ionisatie-energie van het atoom.
Laat het me weten als je een meer gedetailleerde uitleg van een van deze factoren wilt!
 Wat heb je waargenomen terwijl benzoëzuur-zoutzout smelt?
Wat heb je waargenomen terwijl benzoëzuur-zoutzout smelt?  Chloorgas in WOI:redenen voor het gebruik en de impact ervan
Chloorgas in WOI:redenen voor het gebruik en de impact ervan  Een uitdrukking waarin symbolen en formules een chemische reactie vertegenwoordigen?
Een uitdrukking waarin symbolen en formules een chemische reactie vertegenwoordigen?  Waarom ondersteunen vaste stoffen objecten meer dan vloeistoffen?
Waarom ondersteunen vaste stoffen objecten meer dan vloeistoffen?  Woordvergelijking voor de reactie van halogenen met natrium?
Woordvergelijking voor de reactie van halogenen met natrium?
 Start-up ontwikkelt onderhoudsvrij, groenblijvende mosgevels voor een beter klimaat in steden
Start-up ontwikkelt onderhoudsvrij, groenblijvende mosgevels voor een beter klimaat in steden Verkenning van oceaanstromingen onder de Doomsday Glacier
Verkenning van oceaanstromingen onder de Doomsday Glacier Modet de groene toekomst van zeewierjassen en paddenstoelenschoenen
Modet de groene toekomst van zeewierjassen en paddenstoelenschoenen Hoe een Afrikaanse vogel een betere waterfles zou kunnen inspireren
Hoe een Afrikaanse vogel een betere waterfles zou kunnen inspireren  Wat eten meervallen?
Wat eten meervallen?
Hoofdlijnen
- Welke baan heeft een kern?
- Eiwitten:zijn het organische moleculen? - Een definitieve uitleg
- Bent u het ermee eens dat de cel een bouweenheid is van een Zo ja, leg uit waarom?
- Meiosis resulteert meestal in de productie van wat?
- Wat is wetenschappelijke hypothesen?
- Wat zijn enkele verschillen tussen spiercel en een witte bloedcel?
- Waar komen mitochondriën vandaan in de plantencel?
- Wat licht werpen op plantengroei zou kunnen betekenen voor kanker
- Wat gebeurt er met dierlijke cellen in zout water?
- Wetenschappers coderen Wizard of Oz in een verdwijnend klein plastic

- Nieuwe SERS-strategie ontwikkeld voor bepaling van bèta-galactosidase-activiteit
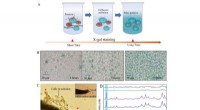
- Onderzoek naar de dynamiek van de vorming van nanodeeltjes uit een voorloper met atomaire resolutie

- Röntgenogen kijken dieper in dodelijke ziekteverwekker
- Plant op proefschaal om zeldzame aardelementen te winnen in het hart van het kolenland

 Wat werkt het STEM -orgel?
Wat werkt het STEM -orgel?  Wat is de potentiële elektrische energie van een geladen object?
Wat is de potentiële elektrische energie van een geladen object?  Hoe vormt een spontane reactie 298 K?
Hoe vormt een spontane reactie 298 K?  Een nieuwe en praktische fantastische route voor superomnifobe vloeistofvrije oppervlakken
Een nieuwe en praktische fantastische route voor superomnifobe vloeistofvrije oppervlakken Hoe beïnvloedt abnormaal lage druk het kookpunt van een verbinding?
Hoe beïnvloedt abnormaal lage druk het kookpunt van een verbinding?  Wat is de grootste groep rotsvormende mineralen?
Wat is de grootste groep rotsvormende mineralen?  Biobrandstofminnende microben temmen
Biobrandstofminnende microben temmen Hoe helpt de lichtreactie Calvin fietsen?
Hoe helpt de lichtreactie Calvin fietsen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

