
Wetenschap
Hoe behandelt het Schrodinger -model van Atom -elektronen?
1. Elektronen draaien niet in een baan om de kern in gedefinieerde paden: In plaats van rond de zon rond de zon te draaien, worden elektronen beschreven door golffuncties . Deze golffuncties vertegenwoordigen de kans om een elektron op een bepaald punt in de ruimte te vinden.
2. Elektronen bezetten atomaire orbitalen: De golffunctie van een elektron bepaalt zijn energieniveau en de vorm van zijn orbitaal, dat een driedimensionaal gebied van ruimte is waar het elektron waarschijnlijk zal worden gevonden. Elk orbitaal kan maximaal twee elektronen bevatten.
3. Elektronen hebben energie gekwantiseerd: Net als in het BOHR -model stelt het Schrödinger -model dat elektronen alleen in specifieke energieniveaus kunnen bestaan, wat betekent dat hun energie wordt gekwantificeerd. Het Schrödinger -model zorgt echter voor een veel breder scala aan energieniveaus en subablellen in het atoom.
4. Elektronen worden beschreven door vier kwantumnummers:
* Hoofdkwantumnummer (n): Bepaalt het energieniveau van het elektron (n =1, 2, 3, ...). Hogere waarden van N komen overeen met hogere energieniveaus.
* hoekmomentum of azimuthaal kwantumnummer (l): Beschrijft de vorm van het orbitaal van het elektron. Het varieert van 0 tot N-1, met 0 die overeenkomt met een sferische s-orbitale, 1 tot een halter gevormde p-orbitaal, 2 tot een complexer d orbitaal, enzovoort.
* magnetisch kwantumnummer (ml): Specificeert de oriëntatie van een orbitaal in de ruimte. Het varieert van -L tot +L, inclusief 0.
* Spin Quantum Number (MS): Geeft het intrinsieke hoekmomentum van een elektron aan, dat spin wordt genoemd. Het kan een waarde hebben van +1/2 of -1/2, die spin -up of spin naar beneden vertegenwoordigt.
Belangrijke verschillen tussen het Bohr -model en het Schrödinger -model:
* Bohr -model: Elektronen draaien de kern in gedefinieerde cirkelvormige paden met specifieke energieniveaus.
* Schrödinger -model: Elektronen worden beschreven door golffuncties en bezetten orbitalen met gekwantiseerde energieniveaus.
Samenvattend biedt het Schrödinger-model een meer accurate en verfijnde beschrijving van elektronen in atomen, waarbij ze worden behandeld als golfachtige deeltjes met waarschijnlijkheden om te worden gevonden in specifieke gebieden van ruimte die orbitalen worden genoemd.
 Gelijktijdige hete en droge zomers komen vaker voor in de toekomst:studie
Gelijktijdige hete en droge zomers komen vaker voor in de toekomst:studie Winter beperkt innovatie - Een nieuw model voor de biodiversiteit van tropische planten is gebaseerd op het opslageffect
Winter beperkt innovatie - Een nieuw model voor de biodiversiteit van tropische planten is gebaseerd op het opslageffect Goedkoop chloordoseerapparaat verbetert de veiligheid van kraanwater in regio's met weinig hulpbronnen
Goedkoop chloordoseerapparaat verbetert de veiligheid van kraanwater in regio's met weinig hulpbronnen Hoe kunnen insecten profiteren van bloeiende planten?
Hoe kunnen insecten profiteren van bloeiende planten?  Warm Arctisch betekent kouder, sneeuwrijkere winters in het noordoosten van de VS, studie zegt:
Warm Arctisch betekent kouder, sneeuwrijkere winters in het noordoosten van de VS, studie zegt:
Hoofdlijnen
- Een doorbraak voor snelle, efficiënte productie van menselijke immuuncellen
- Hoe een ‘evolutionaire speeltuin’ plantengenen bij elkaar brengt
- In welk orgelsysteem is de amoeba -cel?
- Wat welke koninkrijk prokaryoten?
- Hoe zijn modellen nuttig voor wetenschappers?
- Wat is TA Cloning?
- Rechtbank vindt het goed om een soort uil te doden om het effect op andere uilen te zien
- Wanneer u uw arm beweegt om computermuis te gebruiken, welke van deze spierceltypen is erbij betrokken?
- Het molecuul bestaande uit een rechte ketting glucosemoleculen is?
- Gebruik van geradicaliseerde NOₓ-derivaten op metaaloxiden

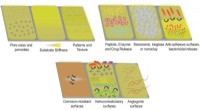
- Op polymeer gebaseerde coatings op metalen implantaten verbeteren de integratie van bot-implantaten
- Nieuw proces van bacteriën en algen kan helpen om het Britse leger koolstofarm te maken

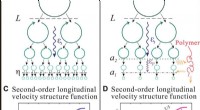
- Experimentele observatie van de schaal van het elastische bereik in turbulente stroming met polymeeradditieven
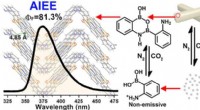
- Nieuw door aggregatie geïnduceerd aromatisch molecuul met verbeterde emissie ontdekt
 Wanneer je gezicht je instapkaart is
Wanneer je gezicht je instapkaart is  Onderzoekers ontwikkelen methode om prijsmodellen te vergelijken
Onderzoekers ontwikkelen methode om prijsmodellen te vergelijken Hoe zal de mens zich aanpassen aan de klimaatverandering? Vraag het aan een Viking
Hoe zal de mens zich aanpassen aan de klimaatverandering? Vraag het aan een Viking  Welke landvormen is kenmerkend voor een gebied met Karst -topografie?
Welke landvormen is kenmerkend voor een gebied met Karst -topografie?  Wanneer werd Skynet - satelliet gemaakt?
Wanneer werd Skynet - satelliet gemaakt?  Wat hebben fossielen te maken met Wegeners-theorie?
Wat hebben fossielen te maken met Wegeners-theorie?  Een model om logische poorten te ontwerpen, geïnspireerd op een eencellig organisme
Een model om logische poorten te ontwerpen, geïnspireerd op een eencellig organisme Terwijl aanvalsdrones zich vermenigvuldigen, Israëlische bedrijven ontwikkelen verdedigingswerken
Terwijl aanvalsdrones zich vermenigvuldigen, Israëlische bedrijven ontwikkelen verdedigingswerken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

