
Wetenschap
Wat gebeurt er met de deeltjes in broom tijdens het afkoelen?
broom bij kamertemperatuur:
* staat: Bromine is een roodbruine vloeistof bij kamertemperatuur.
* deeltjes: De broommoleculen (BR₂) liggen relatief ver uit elkaar en bewegen zich vrij, constant tegen elkaar.
Koeling broom:
* Verminderde kinetische energie: Terwijl broom afkoelt, verliezen de deeltjes kinetische energie. Dit betekent dat ze langzamer bewegen.
* Verminderde afstand: De langzamere bewegende deeltjes hebben minder energie om de aantrekkelijke krachten tussen hen te overwinnen. Bijgevolg beginnen ze dichter bij elkaar te komen.
* overgang naar vloeistof: Op het kookpunt van broom (59 ° C) hebben de deeltjes net voldoende energie om de intermoleculaire krachten te overwinnen en bestaan als een gas. Terwijl de temperatuur onder dit punt daalt, verliezen de broommoleculen energie en condenseren in een vloeibare toestand.
* Verhoogde dichtheid: De vloeibare broom heeft een hogere dichtheid dan de gasvormige broom omdat de deeltjes nauwer bij elkaar zijn verpakt.
* vriespunt: Verdere koeling zorgt ervoor dat de broomdeeltjes nog meer vertragen. Bij -7,2 ° C zijn de broommoleculen strak gepakt, met beperkte beweging. Dit markeert de overgang naar een vaste toestand, met een regelmatige kristallijne structuur.
vaste broom:
* staat: Solid broom is een brosse, kristallijne vaste stof.
* deeltjes: De broommoleculen zijn nauw gepakt en trillen in vaste posities in het kristalrooster.
Sleutelpunten:
* intermoleculaire krachten: De veranderingen in de toestand van Broom worden aangedreven door de sterkte van de intermoleculaire krachten (attracties) tussen de broommoleculen.
* energieniveaus: Terwijl de broommoleculen energie verliezen, verschuiven ze naar een lagere energietoestand, wat leidt tot een verandering in de fysieke toestand.
Laat het me weten als je meer details wilt over een specifiek aspect!
 In een terugkeer naar de natuur legaliseert Californië menselijke compostering voor milieuvoordelen
In een terugkeer naar de natuur legaliseert Californië menselijke compostering voor milieuvoordelen Zijn dinosaurussen echt? Wat we weten over de uitgestorven wezens
Zijn dinosaurussen echt? Wat we weten over de uitgestorven wezens  Definitie van Osteophytosis
Definitie van Osteophytosis  Waarom miljardair klimaatfilantropen altijd deel zullen uitmaken van het probleem
Waarom miljardair klimaatfilantropen altijd deel zullen uitmaken van het probleem Door ontdooiende permafrost komt oud broeikasgas vrij
Door ontdooiende permafrost komt oud broeikasgas vrij
Hoofdlijnen
- In welke periode geloven wetenschappers dat de tuinbouw begint?
- Onderzoek naar plantenenzymen toont aan dat eiwitten hun structurele rangschikking met verrassend gemak kunnen veranderen
- Waarom zijn fermentatiereacties belangrijk voor cellen?
- Een aanpassing om het oppervlak van een deelcel te vergroten die betrokken is bij cellulaire ademhaling?
- Hoe kunnen mutaties de eiwitsynthese in cellen beïnvloeden? Wat is het resultaat?
- Wat is functiebasis in een microscoop?
- Welke organellen worden gevonden in eiwitten?
- Moeten we de genen van buitengewone mensen sparen voor klonen?
- Plantencellen worden niet omgeven door een celwanddier?
- Wetenschappers presenteren nieuwe benadering voor het monitoren van zoetwatergezondheid

- De heilige graal van peptidechemie:peptide-actieve stoffen oraal beschikbaar maken
- Wetenschappers ontwikkelen op wolfraam gebaseerde waterstofdetectoren

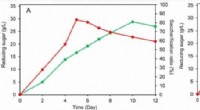
- Nieuwe geconsolideerde bio-saccharificatietechniek voor lignocelluloseconversie ontwikkeld
- Onderzoek verbetert het enzym dat plastic afbreekt
 Hoe telescopen werken
Hoe telescopen werken  Zuckerberg ontmoet EU-functionarissen terwijl nieuwe technische regels opdoemen
Zuckerberg ontmoet EU-functionarissen terwijl nieuwe technische regels opdoemen Sprong in lidar kan de veiligheid verbeteren, veiligheid van nieuwe technologie
Sprong in lidar kan de veiligheid verbeteren, veiligheid van nieuwe technologie Overleven van de mensheid onmogelijk als de VS zich niet opnieuw aansluiten bij de Overeenkomst van Parijs
Overleven van de mensheid onmogelijk als de VS zich niet opnieuw aansluiten bij de Overeenkomst van Parijs  Hebben gasgigantplaneten vaste kernen?
Hebben gasgigantplaneten vaste kernen?  Welke fossiele brandstofvoorraden moeten in de grond blijven om gevaarlijke klimaatverandering te voorkomen?
Welke fossiele brandstofvoorraden moeten in de grond blijven om gevaarlijke klimaatverandering te voorkomen?  Lichtgevende organische moleculen bewerken via oppervlaktemodificatie
Lichtgevende organische moleculen bewerken via oppervlaktemodificatie Is er een beschermheilige van astrologie?
Is er een beschermheilige van astrologie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

