
Wetenschap
Wanneer zinkmetaal wordt geplaatst in een oplossing van kopersulfaatroze pinkbruin gevormd, maar wanneer stuk zilver nog een verandering waargenomen waarom?
Inzicht in de reactiviteitsreeks
Metalen hebben verschillende neigingen om elektronen te verliezen en positieve ionen te vormen. Deze neiging wordt weergegeven door de reactiviteitsreeks, die metalen weergeeft in volgorde van afnemende reactiviteit.
* zeer reactieve metalen: Deze metalen verliezen gemakkelijk elektronen en vormen positieve ionen. Ze kunnen minder reactieve metalen van hun oplossingen verplaatsen.
* Minder reactieve metalen: Deze metalen houden hun elektronen steviger vast en zijn minder snel om ionen te vormen.
De reacties
* zink en kopersulfaat: Zink is reactiever dan koper. Wanneer zinkmetaal in een kopersulfaatoplossing wordt geplaatst, treedt de volgende reactie op:
`` `
Zn (S) + Cuso₄ (aq) → ZnSo₄ (aq) + cu (s)
`` `
* Zink verplaatst koper van de oplossing en vormt zinksulfaat (ZnSo₄) en koperen metaal.
* Het koperen metaal dat op het zink is afgezet, heeft een karakteristieke pinkbruine kleur.
* zilver en kopersulfaat: Zilver is minder reactief dan koper. Daarom treedt geen reactie op wanneer zilver in een kopersulfaatoplossing wordt geplaatst.
* Zilver kan koper niet van zijn oplossing verplaatsen omdat het minder snel elektronen verliest.
Samenvattend
Het verschil in reactiviteit tussen zink en zilver bepaalt of er een reactie zal optreden. Zink, meer reactief, verplaatst koper uit zijn oplossing, wat resulteert in een zichtbare kleurverandering. Zilver, minder reactief, reageert niet met kopersulfaat.
 Chloor verspreidt 2,04 sneller dan gas Q Zoek molecuulgewicht van Q?
Chloor verspreidt 2,04 sneller dan gas Q Zoek molecuulgewicht van Q?  Wanneer wordt een atoom als isotoop beschouwd?
Wanneer wordt een atoom als isotoop beschouwd?  Waarom verandert de kleur van kopersulfaat als je er een ijzeren spijker in doopt?
Waarom verandert de kleur van kopersulfaat als je er een ijzeren spijker in doopt?  De verschillen tussen zout en suiker
De verschillen tussen zout en suiker  Toegang krijgen tot DNA in de krachtpatser van de cellen om ziekten te behandelen
Toegang krijgen tot DNA in de krachtpatser van de cellen om ziekten te behandelen
 Londen wordt 's werelds eerste nationale parkstad
Londen wordt 's werelds eerste nationale parkstad  Stroomstoringen blijven voor miljoenen aanhouden terwijl een nieuwe ijzige storm opdoemt
Stroomstoringen blijven voor miljoenen aanhouden terwijl een nieuwe ijzige storm opdoemt Problemen met luchtvervuiling binnenshuis oplossen die het risico op COVID-19 voor inheemse Amerikanen verhogen
Problemen met luchtvervuiling binnenshuis oplossen die het risico op COVID-19 voor inheemse Amerikanen verhogen Welke klimaatzone heeft bijna geen vegetatie?
Welke klimaatzone heeft bijna geen vegetatie?  Wat groeien de planten in bladeren?
Wat groeien de planten in bladeren?
Hoofdlijnen
- Waar komt plastic vandaan?
- Als het vet uit voedsel komt, wat gaat er dan in?
- In welk koninkrijk classificeert wetenschapper Euglena?
- Wat is de meest waarschijnlijke oorzaak van de grote diversiteit die momenteel wordt waargenomen in meercellige levensvormen?
- Waarom gifkikkers zichzelf niet vergiftigen?
- Hoe reguleert de Euglena zijn interne omgeving?
- Wat zijn de vereiste moleculen in cellulaire ademhaling?
- Hoe wordt de wetenschap gebruikt in de creditcard?
- Wat doet SDS met cellen?
- Zink reguleert de opslag en afgifte van neurotransmitters

- Nieuwe goedkope en niet-toxische methode voor het maken van benzeenringen

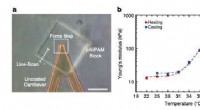
- Onderzoekers ontwikkelen 3D-microstructuren die reageren op temperatuur en licht
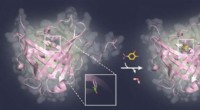
- Blokkeren van suikerstructuren op virussen en tumorcellen
- Nieuwe methode maakt gemakkelijke, veelzijdige synthese van lactonmoleculen mogelijk

 Is een chlooratoom of ion groter?
Is een chlooratoom of ion groter?  Betekent stripwinning bij het dragen van mineralen door schachten die in de grond zijn gegraven?
Betekent stripwinning bij het dragen van mineralen door schachten die in de grond zijn gegraven?  Computerhackers kunnen worden gedwarsboomd door nieuwe methode voor consistentie van misleiding
Computerhackers kunnen worden gedwarsboomd door nieuwe methode voor consistentie van misleiding Is kalk een zuur, een alkali of neutraal?
Is kalk een zuur, een alkali of neutraal?  Welk batterijsysteem is volledig oplaadbaar?
Welk batterijsysteem is volledig oplaadbaar?  Microscopie plus AI staat gelijk aan snelle COVID-19-detectie:studie
Microscopie plus AI staat gelijk aan snelle COVID-19-detectie:studie Naam van anion gevormd uit stikstof?
Naam van anion gevormd uit stikstof?  Hoe worden fossiele replica's gemaakt?
Hoe worden fossiele replica's gemaakt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

