
Wetenschap
Zijn de meeste hydroxideverbindingen oplosbaar in water?
Dit is waarom:
* Groep 1 Hydroxides (Lioh, Naoh, Koh, RBOH, CSOH): Deze zijn zeer oplosbaar vanwege de sterke ionische bindingen tussen de alkali -metalen en het hydroxide -ion.
* Groep 2 Hydroxides (CA (OH) 2, SR (OH) 2, BA (OH) 2): Deze zijn matig oplosbaar, waarbij de oplosbaarheid de groep toeneemt.
* Andere hydroxiden: De meerderheid van de hydroxiden gevormd met overgangsmetalen en niet-metalen zijn onoplosbaar in water. Dit komt omdat de binding tussen het metaalkation en het hydroxideanion vaak sterker is dan de aantrekkingskracht tussen de ionen en watermoleculen.
Uitzonderingen:
* ammoniumhydroxide (NH4OH): Hoewel technisch gezien een zwakke basis, is het zeer oplosbaar in water, waardoor ammoniumionen (NH4+) en hydroxide-ionen gemakkelijk worden gevormd (OH-).
Key Takeaway: Hoewel sommige hydroxiden zeer oplosbaar zijn, zijn velen dat niet. Over het algemeen worden hydroxiden oplosbaarder naarmate u de periodiek ernstige tabel in groepen 1 en 2 naar beneden beweegt.
 Waarom produceren auto's oxiden van zwaveldioxide?
Waarom produceren auto's oxiden van zwaveldioxide?  Welke witte stoffen vormen vorst?
Welke witte stoffen vormen vorst?  Krakende ontdekking:Japanse wetenschapper gebruikt eiwit voor schone energie
Krakende ontdekking:Japanse wetenschapper gebruikt eiwit voor schone energie T-celreceptoren uitrusten om een wijdverbreid en soms dodelijk virus te bestrijden
T-celreceptoren uitrusten om een wijdverbreid en soms dodelijk virus te bestrijden Als de formule voor ammoniak NH is, wat zou de massa van 3 mol in gram zijn?
Als de formule voor ammoniak NH is, wat zou de massa van 3 mol in gram zijn?
 Welke effecten hebben chloorfluorkoolstoffen op de mens?
Welke effecten hebben chloorfluorkoolstoffen op de mens?  Hoe kakkerlakken eruit zien?
Hoe kakkerlakken eruit zien?  Nord Stream-methaanlek zou het grootste ooit in de atmosfeer kunnen zijn
Nord Stream-methaanlek zou het grootste ooit in de atmosfeer kunnen zijn Diepe Antarctische boringen onthullen klimaatgeheimen die gevangen zitten in 1,5 miljoen jaar oud ijs
Diepe Antarctische boringen onthullen klimaatgeheimen die gevangen zitten in 1,5 miljoen jaar oud ijs Studie vindt 6, 600 lekkages door fracking in slechts vier staten
Studie vindt 6, 600 lekkages door fracking in slechts vier staten
Hoofdlijnen
- Welk orgaan is klein materiaal dat niet door het lichaam wordt gebruikt?
- Wat is het doel van transport voor eiwitten?
- Welk kenmerk binnen populaties zorgt ervoor dat de natuurlijke selectie opkomt?
- Welk kenmerk classificeert Escherichia coli als een levend wezen ondanks zijn extreem kleine formaat?
- Wat is larexboom?
- Wat is het onderdeel van holoenzyme?
- De vroegste landdieren hadden minder schedelbotten dan vissen, waardoor hun evolutie werd beperkt
- Wat zijn wetenschappelijke landbouwmethoden?
- Welk enzym breekt modder af?
- Water speelt een onverwachte rol bij de vorming van mineralen
- Water, overal water - en het is vreemder dan je denkt

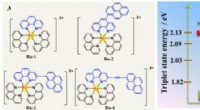
- Fijnafstemming van de aangeslagen toestand van Ru(II)-fotosensibilisatoren voor het stimuleren van de omzetting van kooldioxide
- Een kristallisatiekamer ontwerpen

- Wetenschapper lost een van de heilige gralen van de fysische chemie op na 17 jaar onderzoek

 Is koper nitraat polair of niet polair?
Is koper nitraat polair of niet polair?  VAE stelt lancering van eerste kernreactor verder uit
VAE stelt lancering van eerste kernreactor verder uit Is online winkelen veranderd hoeveel karton we gebruiken?
Is online winkelen veranderd hoeveel karton we gebruiken?  Delen op sociale media maakt ons overmoedig in onze kennis
Delen op sociale media maakt ons overmoedig in onze kennis Exotische faseovergangen ontgrendelen paden naar op superfluïde gebaseerde technologieën
Exotische faseovergangen ontgrendelen paden naar op superfluïde gebaseerde technologieën Koolstofnanobuisjes beloven verbeterde vlamwerende coating
Koolstofnanobuisjes beloven verbeterde vlamwerende coating Wat was de naam van Lunar Module eerste astronauten reed op de maan?
Wat was de naam van Lunar Module eerste astronauten reed op de maan?  Waarom bereken je de pH van de oplossing?
Waarom bereken je de pH van de oplossing?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

