
Wetenschap
Kan een chlooratoom slechts één ionische binding vormen?
* ionische bindingen: Chloor vormt meestal één ionische binding vanwege de hoge elektronegativiteit. Het krijgt één elektron om een stabiele octetconfiguratie te bereiken, die een -1 -lading vormt (CL⁻). Deze ionische binding wordt gevormd met een metaalatoom dat een elektron verliest.
* Covalente bindingen: Chloor kan ook covalente bindingen vormen en elektronen delen met andere niet -metalen atomen. Het kan één, twee of zelfs drie covalente bindingen vormen . Bijvoorbeeld:
* HCl: Chloor vormt één enkele covalente binding met waterstof.
* Cl₂: Chloor vormt een enkele covalente binding met een ander chlooratoom.
* clo₂: Chloor vormt twee covalente bindingen met zuurstofatomen.
Samenvattend: Chloor kan verschillende soorten bindingen vormen, afhankelijk van het andere betrokken atoom. Het vormt meestal één ionische binding, maar het kan ook meerdere covalente bindingen vormen.
 De chemische reactie tussen koperoxide en koolstof die dioxide produceert, is een voorbeeld van?
De chemische reactie tussen koperoxide en koolstof die dioxide produceert, is een voorbeeld van?  Kan gebruikt koffiedik helpen bij het opruimen van milieutoxines?
Kan gebruikt koffiedik helpen bij het opruimen van milieutoxines?  Wat is het tweede beste elektrodemateriaal voor elektrolyse van water?
Wat is het tweede beste elektrodemateriaal voor elektrolyse van water?  Waarom wordt watervrij natriumsulfaat toegevoegd aan de organische oplossing die overblijft na de extractie met 6 M HCl en NaOH?
Waarom wordt watervrij natriumsulfaat toegevoegd aan de organische oplossing die overblijft na de extractie met 6 M HCl en NaOH?  Wat is formule voor uranium 5 sulfide?
Wat is formule voor uranium 5 sulfide?
 Onderzoekers maken nieuwe software voor de nieuwe Europees-Japanse aardobservatiesatelliet EarthCARE
Onderzoekers maken nieuwe software voor de nieuwe Europees-Japanse aardobservatiesatelliet EarthCARE  Hittegolven zijn dodelijker voor sommige steden dan andere - hier is waarom
Hittegolven zijn dodelijker voor sommige steden dan andere - hier is waarom Menselijke activiteit veroorzaakte de langetermijngroei van broeikasgas methaan
Menselijke activiteit veroorzaakte de langetermijngroei van broeikasgas methaan Aan het Victoriameer, een groene vlek verspreidt zich over het blauwe hart van Afrika
Aan het Victoriameer, een groene vlek verspreidt zich over het blauwe hart van Afrika Nieuwe studie is in tegenspraak met aannames van constante elementomstandigheden in de oceanen
Nieuwe studie is in tegenspraak met aannames van constante elementomstandigheden in de oceanen
Hoofdlijnen
- Het vastleggen van de waardeketen leidt tot toekomstige bezorgdheid over de duurzaamheid van bossen
- Onderzoekers identificeren nieuwe oorzaken van antibioticaresistentie bij bacteriën
- Waarom zouden defecte recessieve allelen in de genenpool worden bewaard?
- Wat concludeerden Schleiden en Schwann over cel?
- Wat zijn de representatieve organismen van Kingdom Protist?
- Het eerste onderzoek in zijn soort toont aan dat natuurbehoudsacties effectief zijn in het stoppen en omkeren van het verlies aan biodiversiteit
- Hoe een celvorm zijn functie beïnvloedt
- Welk enzym is aanwezig in speeksel?
- Wat is asthenosfeer?
- Onderzoek verbetert theorieën over ionenverdamping en prestaties van elektrospraytoepassingen
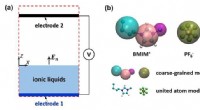
- Een nieuwe procedure voor het verkrijgen van een goedkope, ultrahard materiaal dat bestand is tegen radioactiviteit

- Onderzoekers ontwikkelen sensoren die menselijke biomarkers en giftig gas detecteren
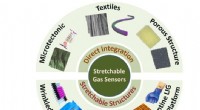
- Hoe nieuwe materialen de efficiëntie van directe ethanolbrandstofcellen verhogen

- Een kleur van poreuze materialen in- en uitschakelen met zuur

 Restaurants met zwarte eigenaren onevenredig zwaar getroffen tijdens pandemie
Restaurants met zwarte eigenaren onevenredig zwaar getroffen tijdens pandemie Samsung Electronics signaleert bijna -30% terugval in bedrijfsresultaat Q4
Samsung Electronics signaleert bijna -30% terugval in bedrijfsresultaat Q4 Akoestisch apparaat laat piëzo-elektrische apparaten op een ander deuntje zingen
Akoestisch apparaat laat piëzo-elektrische apparaten op een ander deuntje zingen Wat betekent Nie in de chemie?
Wat betekent Nie in de chemie?  Waarom ontleden fruit?
Waarom ontleden fruit?  Wat is een ander woord voor energie?
Wat is een ander woord voor energie?  Welke vorm van energie wordt gebruikt als een persoon ladder beklimt?
Welke vorm van energie wordt gebruikt als een persoon ladder beklimt?  Welk hemelse object beweegt achteruit tussen sterren?
Welk hemelse object beweegt achteruit tussen sterren?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

