
Wetenschap
De chemische reactie tussen koperoxide en koolstof die dioxide produceert, is een voorbeeld van?
De chemische reactie tussen koperoxide en koolstof die koper en koolstofdioxide produceert, is een voorbeeld van een reductie-oxidatiereactie (Ook bekend als een redox -reactie ). Dit is waarom:
* reductie: Koperoxide (CUO) is verminderd. Het koper in de oxide wint elektronen en zijn oxidatietoestand neemt af van +2 naar 0. Dit wordt weergegeven door de volgende halve reactie:
* Cuo + 2e- → Cu + O2-
* oxidatie: Koolstof (C) wordt geoxideerd. Het verliest elektronen en zijn oxidatietoestand neemt toe van 0 tot +4. Dit wordt weergegeven door de volgende halve reactie:
* C → CO2 + 4E-
Algemene reactie:
Cuo + C → Cu + CO2
In deze reactie fungeert koperoxide als een oxidatiemiddel (het accepteert elektronen) en koolstof werkt als een reductiemiddel (het doneert elektronen).
 De vaste binnenkern van de aarde kan zowel papperig als hard ijzer bevatten
De vaste binnenkern van de aarde kan zowel papperig als hard ijzer bevatten Extreme rituelen:wat is de sociale rol van geweld in deze culturele evenementen?
Extreme rituelen:wat is de sociale rol van geweld in deze culturele evenementen?  Minstens 40 doden bij ernstige overstromingen in Noord-Turkije
Minstens 40 doden bij ernstige overstromingen in Noord-Turkije De aarde bevindt zich in een nieuw tijdperk vanwege de mens,
De aarde bevindt zich in een nieuw tijdperk vanwege de mens,  Vulkanische explosie hervormde top van de Indonesische berg Sinabung
Vulkanische explosie hervormde top van de Indonesische berg Sinabung
Hoofdlijnen
- Wat zou een diagram van een enzym maltose combineren met twee glucosemoleculen om Moaltose te vormen?
- Waarom is het belangrijk dat u dingen wetenschappelijk classificeert?
- Wat is het doel van sporen die binnen sommige bacteriën leven?
- Wat is de belangrijkste organel in een cel en waarom?
- Wat is het verschil tussen de Charls -theorie van natuurlijke selectie en sociaal overleving fittest?
- Zijn protozoanen warm bloedig of koelbloedig?
- Welke consumenten voeden zich met algen?
- Het testen van chimpansees in Tanzania gedurende tientallen jaren suggereert dat persoonlijkheidstypes stabiel zijn
- Kunnen sociale media worden gebruikt om uitbraken van ziekten op te sporen?
- Onderzoekers komen op de golflengte van de consument met InSb-technologie
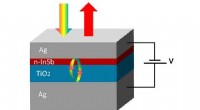
- Zinkoxide:sleutelcomponent voor de methanolsynthesereactie op koperkatalysatoren
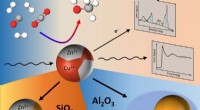
- Studie onthult de ingewikkelde manier waarop twee eiwitten interageren om celbeweging te bevorderen, metastase
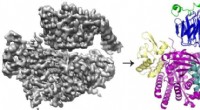
- Wetenschappers ontwikkelen diagnostische test die erop gericht is antibioticaresistentie in minder dan 45 minuten op te sporen

- Houtalternatieven vinden voor bedreigde ebbenhout

 Hoe vindt een wolf eten?
Hoe vindt een wolf eten?  NASA lanceert raket op zoek naar antwoorden op poollicht
NASA lanceert raket op zoek naar antwoorden op poollicht Waar worden cellen gecategoriseerd?
Waar worden cellen gecategoriseerd?  Hoe werd de leeftijd van rotsen in oceaanbekkens bepaald?
Hoe werd de leeftijd van rotsen in oceaanbekkens bepaald?  Wat is -0celsius in Fahrenheit?
Wat is -0celsius in Fahrenheit?  Beeldgestuurde borstkankertherapie mogelijk gemaakt door nanodrug
Beeldgestuurde borstkankertherapie mogelijk gemaakt door nanodrug Onderzoekers creëren een nauwkeuriger model van hoe sommige microben naar voedingsstoffen zoeken
Onderzoekers creëren een nauwkeuriger model van hoe sommige microben naar voedingsstoffen zoeken  Welzijn van achtergebleven kinderen in Kirgizië focus van studie
Welzijn van achtergebleven kinderen in Kirgizië focus van studie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

