
Wetenschap
Waarom is waterstof onoplosbaar in water?
Dit is waarom:
* Zwakke intermoleculaire krachten: Waterstofgas (H₂) is niet -polair, terwijl water zeer polair is. Dit betekent dat er een zwakke interactie is tussen waterstof- en watermoleculen. Het ontbreken van sterke aantrekkelijke krachten beperkt de oplosbaarheid van waterstof in water.
* Laag molecuulgewicht: Waterstof heeft een zeer laag molecuulgewicht, wat bijdraagt aan zijn slechte oplosbaarheid. Kleinere moleculen zijn meestal meer oplosbaar, maar de kleine omvang van de waterstof maakt het minder waarschijnlijk om te interageren met watermoleculen.
Het is echter belangrijk op te merken:
* Oplosbaarheid hangt af van voorwaarden: De oplosbaarheid van waterstof in water neemt toe bij hogere drukken en lagere temperaturen.
* Sommige waterstof kan oplossen: Hoewel de hoeveelheid waterstof die oplost in water relatief klein is, is het niet volledig te verwaarlozen.
Samenvattend, hoewel waterstof niet sterk oplosbaar is in water, is het ook niet helemaal onoplosbaar. De zwakke intermoleculaire krachten en het lage molecuulgewicht dragen bij aan zijn slechte oplosbaarheid.
 Is Iron II Oxide Fe2O3 correct?
Is Iron II Oxide Fe2O3 correct?  Wat is de oplosbaarheid van ethylacetaat in water?
Wat is de oplosbaarheid van ethylacetaat in water?  Waarom hebben verschillende vloeistoffen een viswaardigheid?
Waarom hebben verschillende vloeistoffen een viswaardigheid?  Onderzoekers ontwikkelen stabiele en efficiënte anorganische CsPbI3-zonnecellen
Onderzoekers ontwikkelen stabiele en efficiënte anorganische CsPbI3-zonnecellen  Wat is de naam van Allotrope die zestig koolstofatomen in zijn molecuul bevat?
Wat is de naam van Allotrope die zestig koolstofatomen in zijn molecuul bevat?
 Ontdekking daagt de recente herinterpretatie van magmakamers uit
Ontdekking daagt de recente herinterpretatie van magmakamers uit NASA bereidt zich voor op nieuwe wetenschappelijke vluchten boven de kust van Louisiana
NASA bereidt zich voor op nieuwe wetenschappelijke vluchten boven de kust van Louisiana Gevaar niet voorbij:gaslekken, schimmel weefgetouw voor Harvey evacués
Gevaar niet voorbij:gaslekken, schimmel weefgetouw voor Harvey evacués Hoe klimaatverandering de stroom van de Colorado-rivier verminderde
Hoe klimaatverandering de stroom van de Colorado-rivier verminderde  Stikstofstoot heeft sargassum veranderd in 's werelds grootste schadelijke algenbloei
Stikstofstoot heeft sargassum veranderd in 's werelds grootste schadelijke algenbloei
Hoofdlijnen
- Wat is een virus en hoe wordt het een gevaar voor het menselijk leven?
- Gen-experts gaan ongediertebestrijding aanpakken
- Celmembraan Feiten
- Tijdens de menselijke ontwikkeling moet welk proces plaatsvinden voordat de celdeling kan plaatsvinden?
- Het homeostatische mechanisme dat constant fluctueert, wordt het wat genoemd?
- Welke term beschrijft bacteriën die rond of sferisch gevormd zijn?
- Kunnen huisdieren apenpokken krijgen? Het komt zelden voor, maar experts zeggen ja:dit is wat u moet weten
- Hoe communiceren bacteriën?
- Waarom dacht Gregor Mendel dat genen die zijn geërfd in paren?
- Geneesmiddelenscreening op de chip voor het identificeren van antibiotica-interacties in acht uur

- Wereldwijd gebruikte angstdrug tegen lage kosten uit afvalwater verwijderen
- Onderzoekers maken potentiële doorbraak in de ontwikkeling van kankergeneesmiddelen

- Gerecycleerde bureaustoelen omgetoverd tot hard-shell rugzakken en fietstassen

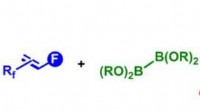
- Chemici ontsluiten het potentieel van fluoralkenen
 Een nieuwe composiet voor treksterkte
Een nieuwe composiet voor treksterkte Een rots van 10 kg wordt van de rand van een brug geduwd 50 meter boven de grond wat kinetische energie was op Midway Point zijn val?
Een rots van 10 kg wordt van de rand van een brug geduwd 50 meter boven de grond wat kinetische energie was op Midway Point zijn val?  Hoe komt regen neer uit wolken?
Hoe komt regen neer uit wolken?  De elektrostatische kracht tussen twee ladingen op 2 meter uit elkaar is 0,10N. Wat zal een 2-C lading en een 8-c elkaar aantrekken wanneer ze dezelfde afstand uit elkaar hebben geplaatst?
De elektrostatische kracht tussen twee ladingen op 2 meter uit elkaar is 0,10N. Wat zal een 2-C lading en een 8-c elkaar aantrekken wanneer ze dezelfde afstand uit elkaar hebben geplaatst?  Onthulling van een nieuwe AAK1-remmer:hoe chemische proteomics therapeutisch potentieel ontsluiten
Onthulling van een nieuwe AAK1-remmer:hoe chemische proteomics therapeutisch potentieel ontsluiten  Bereken Alkaliteit
Bereken Alkaliteit  Hoe haal je goud uit de aardkorst?
Hoe haal je goud uit de aardkorst?  Beweegt de zon en de maan?
Beweegt de zon en de maan?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

