
Wetenschap
Wat is de samengestelde xecl8?
Dit is waarom:
* Xenon's (XE) bindingscapaciteit: Xenon is een edelgas, wat betekent dat het een volledige buitenste schaal van elektronen heeft en over het algemeen niet reactief is. Hoewel het verbindingen kan vormen, doet het dit alleen onder specifieke omstandigheden en met zeer elektronegatieve elementen zoals fluor en zuurstof.
* het bindgedrag van chloor (CL): Chloor is een halogeen, wat betekent dat het meestal enkele bindingen vormt met andere elementen. Het vormt zelden meer dan één binding met een enkel atoom.
De reden dat Xecl8 niet mogelijk is, is dat:
* Grootte en stabiliteit: De atomaire straal van Xenon is relatief groot, waardoor het moeilijk is om er acht chlooratomen omheen te huisvesten.
* Laaddichtheid: Acht chlooratomen zouden een significante negatieve ladingsdichtheid creëren rond het centrale Xenon -atoom, dat het molecuul zou destabiliseren.
Conclusie, XECL8 is een hypothetische verbinding die waarschijnlijk niet zal worden gevormd op basis van de chemische eigenschappen van xenon en chloor.
 Karakterisering van de structuur van een lid van de L-Aminozuur Transporter (LAT) familie
Karakterisering van de structuur van een lid van de L-Aminozuur Transporter (LAT) familie Geconstrueerde insuline die kan worden geactiveerd door een hoge bloedsuikerspiegel kan de levenskwaliteit van diabetici verbeteren
Geconstrueerde insuline die kan worden geactiveerd door een hoge bloedsuikerspiegel kan de levenskwaliteit van diabetici verbeteren Wat hebben natriumhydroxide en kalium met elkaar gemeen?
Wat hebben natriumhydroxide en kalium met elkaar gemeen?  Waarom moet water vloeistof worden genoemd?
Waarom moet water vloeistof worden genoemd?  Wat veroorzaakte de stofbak?
Wat veroorzaakte de stofbak?
Hoofdlijnen
- Welk eiwit is onoplosbaar in water?
- Wat is over reproductie?
- Welke soorten organische moleculen vormen een celmembraan?
- In de meeste meercellige organismen worden cellen georganiseerd volgens hun?
- Wat is het gebruik van computers in de biologie?
- Wetenschappers ontdekken dat darmbacteriën in bijen antibioticaresistente genen naar elkaar verspreiden
- Is de weide knoflookbloem multi-cellulair of eencellulair?
- Zijn er een wetenschappelijk woord dat begint met G?
- Welke wezen heeft twee seksorganen?
- Geuren langer laten duren

- Nieuwe deuren openen:eerste synthetisch mechanisch gevoelig kaliumkanaal

- Organische polymere scintillatoren prikkelen de röntgengemeenschap

- Microscopisch vibrerend circulair dichroïsme maakt supramoleculaire chiraliteitsmapping mogelijk
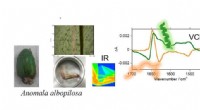
- Een grote stap voorwaarts in organische elektronica

 Hoe katalysatoren worden gebruikt in de landbouw van de indydry of de behandeling van besmet bodemafvalwater?
Hoe katalysatoren worden gebruikt in de landbouw van de indydry of de behandeling van besmet bodemafvalwater?  Heeft Jupiter dag en nacht?
Heeft Jupiter dag en nacht?  Vervuiling van Heathrow gedetecteerd in het centrum van Londen
Vervuiling van Heathrow gedetecteerd in het centrum van Londen Afbeelding:Amazonebranden
Afbeelding:Amazonebranden Welke chemische stof vormt calciumoxide als het aan water wordt toegevoegd?
Welke chemische stof vormt calciumoxide als het aan water wordt toegevoegd?  Hoe elektronen springen van de ene schaal naar de andere in aanwezigheid van verboden zone een atoom?
Hoe elektronen springen van de ene schaal naar de andere in aanwezigheid van verboden zone een atoom?  Een milieu-CGE-model van de Chinese economie:modellering van keuzes en toepassing
Een milieu-CGE-model van de Chinese economie:modellering van keuzes en toepassing  Pandemie drijft kinderen weer aan het werk, winsten in gevaar brengen
Pandemie drijft kinderen weer aan het werk, winsten in gevaar brengen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

