
Wetenschap
Wat hebben natriumhydroxide en kalium met elkaar gemeen?
Er zijn echter ook enkele belangrijke verschillen tussen natriumhydroxide en kalium. Natriumhydroxide is een zeer oplosbare verbinding, wat betekent dat het gemakkelijk in water oplost. Kalium is daarentegen een matig oplosbaar metaal dat slechts gedeeltelijk in water oplost. Dit verschil in oplosbaarheid beïnvloedt de reactiviteit van deze stoffen. Natriumhydroxide is reactiever dan kalium in water, omdat de ionen ervan gemakkelijker beschikbaar zijn om deel te nemen aan chemische reacties.
Bovendien is natriumhydroxide een sterkere base dan kalium. Dit betekent dat het een grotere neiging heeft om elektronen of hydroxide-ionen (OH-) aan water te doneren, wat resulteert in een hoger pH-niveau. Kalium daarentegen is een zwakkere base en heeft een lagere neiging om elektronen te doneren, wat leidt tot een lager pH-niveau.
Over het algemeen zijn natriumhydroxide en kalium beide zeer reactieve elementen die hydrolyse ondergaan wanneer ze in contact komen met water, waarbij warmte vrijkomt en een base wordt gevormd. Hun verschillen in oplosbaarheid en basiciteit resulteren echter in variaties in hun reactiviteit en de sterkte van de resulterende basen.
 China rolt groene loper uit voor Californië over klimaat
China rolt groene loper uit voor Californië over klimaat Is uw drinkwater veilig?
Is uw drinkwater veilig? Wat voor soort leefomgeving leeft een cheeta?
Wat voor soort leefomgeving leeft een cheeta?  Wetenschappers geven eerste gedetailleerde schattingen van hoeveel sediment vanuit het rifsysteem naar koraaleilanden wordt aangevoerd
Wetenschappers geven eerste gedetailleerde schattingen van hoeveel sediment vanuit het rifsysteem naar koraaleilanden wordt aangevoerd  Luchtvervuiling sluit alle scholen in Teheran
Luchtvervuiling sluit alle scholen in Teheran
Hoofdlijnen
- Mysterie opgelost? Biologen vinden een unieke versie van filamentvormend eiwit in menselijke cellen die insecten niet hebben
- De vogelgriep veroorzaakt duizenden zeehondensterfte. Wetenschappers weten niet zeker hoe ze dit kunnen vertragen
- De terugkeer van wolven naar Oregon brengt conflicten en kansen
- Hoe hotspots van genetische variatie zich ontwikkelden in menselijk DNA
- Wanneer wordt het inwendige van de cel als isotoon met de omringende vloeistof beschouwd?
- Hoe kunnen uitstervingen de evolutie beïnvloeden van organismen die een gebeurtenis overleven?
- Uit de kleine teelballen van vliegen ontstaat nieuw inzicht in hoe genen ontstaan
- Genetische modificatie: definitie, soorten, proces, voorbeelden
- Hoe bacteriën spuiten maken:wetenschappers reconstrueren het bacteriële transportkanaal in reageerbuisjes
- Aan het oppervlak blootgestelde nanodendrieten met hoge index als ORR-elektrokatalysator

- De juiste formule voor het opschalen van de productie van veelbelovend materiaal om water te decontamineren

- Nieuw materiaal kan de productie van plastic energiezuiniger maken
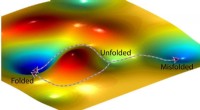
- Verborgen symmetrie gevonden in chemische kinetische vergelijkingen
- Duurzame biosynthetische transparante films ontwikkeld voor plasticvervanger

 Technicus A zegt dat UHSS is ontworpen om botsingsenergie te absorberen. B zacht staal overdracht Wie gelijk?
Technicus A zegt dat UHSS is ontworpen om botsingsenergie te absorberen. B zacht staal overdracht Wie gelijk?  Waarom zijn chloor en jodium in verschillende toestanden op kamertemperatuur?
Waarom zijn chloor en jodium in verschillende toestanden op kamertemperatuur?  Nieuw inzicht in hoe bijen zien
Nieuw inzicht in hoe bijen zien  Hoe gasdruk te converteren naar BTU
Hoe gasdruk te converteren naar BTU  Afbeelding:Ries-krater, Duitsland
Afbeelding:Ries-krater, Duitsland Eierontkookmachine neemt visolie over
Eierontkookmachine neemt visolie over Mijnbouw vermindert overvloed, rijkdom van het waterleven
Mijnbouw vermindert overvloed, rijkdom van het waterleven Industrie 4.0 implementeren in het MKB door te focussen op de klant
Industrie 4.0 implementeren in het MKB door te focussen op de klant
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

