
Wetenschap
Wat is de empirische formule van een verbinding die 40 procent zwavel en 60 zuurstof per gewicht?
1. Ga uit van een 100 g monster:
* Dit maakt berekeningen gemakkelijker, omdat percentages zich direct vertalen naar grams.
* Je hebt 40 g zwavel (s) en 60 g zuurstof (O).
2. Converteer grams naar mollen:
* Verdeel de massa van elk element door zijn molaire massa:
* Mol S =40 g / 32.06 g / mol =1,25 mol
* Mol O =60 g / 16,00 g / mol =3,75 mol
3. Zoek de eenvoudigste ratio van het hele nummer:
* Verdeel elke molwaarde door de kleinste molwaarde (in dit geval 1,25 mol):
* S:1,25 mol / 1,25 mol =1
* O:3,75 mol / 1,25 mol =3
4. Schrijf de empirische formule:
* De verhouding van zwavel tot zuurstof is 1:3.
* De empirische formule is So₃ .
 Als het goed is gegroeid, palmolie kan duurzaam zijn
Als het goed is gegroeid, palmolie kan duurzaam zijn Geofysicus blijft ondanks enorm gat optimistisch over Arctische ozonlaag
Geofysicus blijft ondanks enorm gat optimistisch over Arctische ozonlaag School is uit:hoe klimaatverandering het onderwijs bedreigt
School is uit:hoe klimaatverandering het onderwijs bedreigt  Studie daagt zorgen rond geïmporteerde gekweekte garnalen uit
Studie daagt zorgen rond geïmporteerde gekweekte garnalen uit Vroeg waarschuwingssysteem voor aardbevingen breidt zich uit naar Oregon, Washington
Vroeg waarschuwingssysteem voor aardbevingen breidt zich uit naar Oregon, Washington
Hoofdlijnen
- Wat is de naam van de studiebacteriën en -virussen?
- Wat is een organisme dat vanzelf beweegt en voedsel eet?
- (Her)verwerven van het potentieel om alles te worden
- Kunnen je hersenen een verkeersopstopping hebben?
- Hoe zou u de definitie van biologie in uw eigen woorden schrijven?
- Wat zijn de klieren in wangen?
- Wetenschappers vinden potentiële wapens voor de strijd tegen antibioticaresistentie
- Genetisch onderzoek streeft een ongrijpbaar doel na:hoeveel bultruggen bestonden er vóór de walvisvangst?
- Welke eukaryoten die geen lid zijn van de Kingdoms Plantae Animalia of Fungi overwogen?
- Video:Hoe werkt airconditioning?

- Coronavirus-testkits worden ontwikkeld met behulp van nieuwe RNA-beeldvormingstechnologie

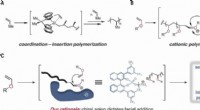
- Een organokatalysator gebruiken om de polymerisatie te stereocontroleren
- Video:Waarom plastic flessen worden gerecycled tot kleding

- Kwantumchemie lost het mysterie van de 20 aminozuren in de genetische code op

 Permafrost-koolstofverlies vermindert de microbiële stabiliteit
Permafrost-koolstofverlies vermindert de microbiële stabiliteit Kunnen we zware kernen modelleren vanuit de eerste principes?
Kunnen we zware kernen modelleren vanuit de eerste principes?  800 ft is gelijk aan hoeveel meter?
800 ft is gelijk aan hoeveel meter?  Welk eiwit wordt gebruikt in het exoskelet?
Welk eiwit wordt gebruikt in het exoskelet?  Hoe beschrijven we de kenmerken van een spore -lagerplanten?
Hoe beschrijven we de kenmerken van een spore -lagerplanten?  Is een batterij een voorbeeld van geleider?
Is een batterij een voorbeeld van geleider?  Hoe kan energie worden omgezet van warmte naar nucleair?
Hoe kan energie worden omgezet van warmte naar nucleair?  Hoe ontstaat een covalente binding tussen twee atomen?
Hoe ontstaat een covalente binding tussen twee atomen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

