
Wetenschap
Hoeveel gram ijzer II -sulfide moet reageren met zoutzuur genereren 12 g waterstofsulfide?
1. Schrijf de gebalanceerde chemische vergelijking:
FES (s) + 2 HCl (aq) → fecl₂ (aq) + h₂s (g)
2. Bereken de molaire massa van waterstofsulfide (H₂s):
* H:1,01 g/mol (x2 =2.02 g/mol)
* S:32.07 g/mol
* Totaal:34.09 g/mol
3. Bereken de mol waterstofsulfide:
* Mol =massa / molaire massa
* Mol H₂s =12 g / 34.09 g / mol =0,352 mol
4. Gebruik de molverhouding van de gebalanceerde vergelijking om de mol ijzer II sulfide (FES) te vinden:
* De vergelijking toont een 1:1 molverhouding tussen FES en H₂s.
* Daarom zijn 0,352 mol FES nodig.
5. Bereken de massa van ijzer II sulfide:
* Molaire massa FES:
* Fe:55.85 g/mol
* S:32.07 g/mol
* Totaal:87,92 g/mol
* Massa =mollen x molaire massa
* Massa van FES =0,352 mol x 87,92 g/mol =30,9 g
Daarom zijn ongeveer 30,9 gram ijzer II sulfide nodig om te reageren met zoutzuur om 12 gram waterstofsulfide te genereren.
 Een virtuele seismoloog maken
Een virtuele seismoloog maken Studie onderzoekt hoe Spaans extreemrechts traditionele perspectieven als ‘liefde’ omschrijft
Studie onderzoekt hoe Spaans extreemrechts traditionele perspectieven als ‘liefde’ omschrijft  Welke dieren tonen commensalisme in het regenwoud?
Welke dieren tonen commensalisme in het regenwoud?  Hoe onderscheid je een bullsnake van een ratelslang
Hoe onderscheid je een bullsnake van een ratelslang Nieuwe kolencentrales in China riskeren klimaatdoelstelling voor 2060:onderzoekers
Nieuwe kolencentrales in China riskeren klimaatdoelstelling voor 2060:onderzoekers
Hoofdlijnen
- Voorbeelden van sensorische adaptatie
- Wat is de studie van menselijke cellen van bemesting tot geboorte die wordt genoemd?
- Agressiede-escalatiegen geïdentificeerd in fruitvliegjes
- Wat is het beste bewijs om de evolutie te weerleggen?
- Genetisch gemodificeerd voedsel, wie moet het vertellen?
- Nieuw AI-systeem kan het gedrag van fruitvliegjes decoderen:waarom dat cruciaal is voor toekomstig onderzoek naar de menselijke genetica
- Gevangen in levende cellen:hoe bacteriën hun genen reguleren om zichzelf te verdedigen
- Onderzoekers ontwikkelen vergelijkingen om kantelpunten van de meest bedreigde ecosystemen van onze aardbol te voorspellen en te vergelijken
- Sommige soorten verdragen de klimaatverandering mogelijk beter dan verwacht
- Nieuwe methode voor het genereren van krachtige, specifieke bindende eiwitten voor nieuwe medicijnen
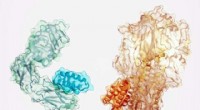
- Microschaal thermoforese om hits van high-throughput screening te karakteriseren

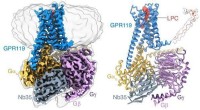
- Onderzoek onthult ligandherkenningsmechanisme van weesreceptor GPR119
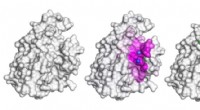
- Neurale netwerk detecteert eiwit-peptide bindingsplaatsen om de ontdekking van peptidegeneesmiddelen op gang te brengen
- Spinazie gebruikt in neutronenstudies zou het geheim kunnen ontrafelen voor een sterkere plantengroei

 Caraïben worden slim om orkanen het hoofd te bieden
Caraïben worden slim om orkanen het hoofd te bieden Luchtvaartvracht Hoe werkt het
Luchtvaartvracht Hoe werkt het  Hoe microgrids de veerkracht in New Orleans kunnen vergroten
Hoe microgrids de veerkracht in New Orleans kunnen vergroten Kleine apparaten beloven een nieuwe horizon voor veiligheidsonderzoek en medische beeldvorming
Kleine apparaten beloven een nieuwe horizon voor veiligheidsonderzoek en medische beeldvorming Hoe verhoudt de kracht van een wetenschappelijke theorie zich tot hypothese?
Hoe verhoudt de kracht van een wetenschappelijke theorie zich tot hypothese?  Afbeelding:Lancering van de Galileo-missie
Afbeelding:Lancering van de Galileo-missie Zijn dit geregistreerde verschillende personen die elkaar waarderen, ongeacht talenten of jaren van de huid?
Zijn dit geregistreerde verschillende personen die elkaar waarderen, ongeacht talenten of jaren van de huid?  Wat worden dingen die te klein zijn voor een lichte microscoop, bekeken?
Wat worden dingen die te klein zijn voor een lichte microscoop, bekeken?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

