
Wetenschap
Is het kookpunt van chloor lager dan het water?
Ja, het kookpunt van chloor is lager dan het kookpunt van water.
Dit is waarom:
* chloor (Cl₂) is een niet -polair molecuul: Chloormoleculen worden bij elkaar gehouden door zwakke dispersiekrachten in Londen. Deze krachten zijn relatief zwak in vergelijking met de waterstofbinding die aanwezig is in water.
* Water (H₂o) is een polair molecuul: Watermoleculen vormen sterke waterstofbruggen met elkaar, waardoor meer energie nodig is om deze bindingen te overwinnen en het kookpunt te bereiken.
kookpunten:
* chloor: -34.04 ° C (-29,47 ° F)
* Water: 100 ° C (212 ° F)
 Wat is een methode die wordt gebruikt om het nummer en de locatie van elektronen voor bepaalde atomen te identificeren?
Wat is een methode die wordt gebruikt om het nummer en de locatie van elektronen voor bepaalde atomen te identificeren?  Een harig forensisch probleem oplossen
Een harig forensisch probleem oplossen Een uitgebreide kijk op koemelk
Een uitgebreide kijk op koemelk Wat ontbreekt de stof in een vacuüm?
Wat ontbreekt de stof in een vacuüm?  Zijn de fysische en chemische eigenschappen van een verbinding noodzakelijkerwijs vergelijkbaar met die elementen waaruit deze is samengesteld?
Zijn de fysische en chemische eigenschappen van een verbinding noodzakelijkerwijs vergelijkbaar met die elementen waaruit deze is samengesteld?
 Nieuw perspectief op veranderende reisomstandigheden in Arctische gemeenschappen
Nieuw perspectief op veranderende reisomstandigheden in Arctische gemeenschappen Is het gemiddelde vrije pad afhankelijk van de temperatuur?
Is het gemiddelde vrije pad afhankelijk van de temperatuur?  Cry me a river:lage waterstanden zorgen voor chaos in Duitsland
Cry me a river:lage waterstanden zorgen voor chaos in Duitsland Het gebied van de aardewetenschap dat onderzoekt de fysieke en biologische veranderingen die in het verleden hebben plaatsgevonden, wordt aangeroepen?
Het gebied van de aardewetenschap dat onderzoekt de fysieke en biologische veranderingen die in het verleden hebben plaatsgevonden, wordt aangeroepen?  Percentage stikstof in de lucht
Percentage stikstof in de lucht
Hoofdlijnen
- Een gevolg van genetische drift is?
- Wie bezit en regelt genetische informatie?
- Onderzoekers onderzoeken de complexe interacties tussen hout, houtkap en bosolifanten
- Ontdekking van oud glasvezelfossiel uit Glasgow onthult nieuwe soorten
- Wat is gesorteerd in een vulkaanplantencel?
- Wat is de venatie van atis?
- G1-fase: wat gebeurt er tijdens deze fase van de celcyclus?
- Wat zijn de ziekteverwekker die borstkanker veroorzaakt?
- Waarom krijgen demonen de schuld van slaapverlamming?
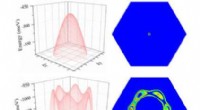
- Kan een nieuw 2D-materiaal ervoor zorgen dat halfgeleiders steeds kleiner worden, sterker, beter en sneller?
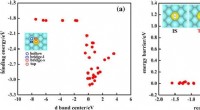
- AI zocht naar single-atom-alloy katalysatoren, 200 veelbelovende kandidaten gevonden
- Onderzoekers rapporteren nieuwe techniek voor het ontdooien van oppervlakken

- Wetenschappers suggereren titaniumnitride in plaats van goud in opto-elektronica

- Ionen in gesmolten zouten kunnen tegen de stroom in gaan

 Nieuwe wiskundige oplossingen voor een oud probleem in de astronomie
Nieuwe wiskundige oplossingen voor een oud probleem in de astronomie Hoe een hoek te vinden in de trigonometrie
Hoe een hoek te vinden in de trigonometrie Wanneer komt de maan over de berg geschapen?
Wanneer komt de maan over de berg geschapen?  Dolfijnen vormen grootste alliantienetwerk buiten mensen, studie vondsten
Dolfijnen vormen grootste alliantienetwerk buiten mensen, studie vondsten Nieuwe macrolacton-database kan helpen bij het ontdekken van medicijnen, Onderzoek
Nieuwe macrolacton-database kan helpen bij het ontdekken van medicijnen, Onderzoek Hoe zou u het epicentrum van een aardbeving vinden die ooit afstand van elke drie seismografische stations hebben vastgesteld?
Hoe zou u het epicentrum van een aardbeving vinden die ooit afstand van elke drie seismografische stations hebben vastgesteld?  Wat veroorzaakt de dagelijkse beweging van sterren?
Wat veroorzaakt de dagelijkse beweging van sterren?  Vier manieren om de koolstof in je voedselmand te verminderen
Vier manieren om de koolstof in je voedselmand te verminderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

