
Wetenschap
Wat voor soort ionen worden een natriumatoom en chloor wanneer valentie -elektron van de ene naar de andere wordt overgebracht?
Dit is hoe natrium- en chloorvorm ionen:
* natrium (na) heeft één valentie -elektron in zijn buitenste schaal. Het wil dit elektron verliezen om een stabiel octet (8 elektronen) in zijn buitenste schaal te bereiken. Wanneer het dit elektron verliest, wordt het een positief geladen ion genaamd een natriumkation (Na+) .
* chloor (Cl) heeft zeven valentie -elektronen in zijn buitenste schaal. Het wil één elektron winnen om een stabiel octet te bereiken. Wanneer het een elektron wint, wordt het een negatief geladen ion genaamd een chloride-anion (Cl-) .
Samenvattend:
* Natriumatoom (NA) -> Natriumkation (Na+)
* chlooratoom (CL)-> chloride anion (Cl-)
 Wat legt uit waarom geleiders en isolatorproducten?
Wat legt uit waarom geleiders en isolatorproducten?  Zijn wolken gemaakt van vloeistoffen een gas?
Zijn wolken gemaakt van vloeistoffen een gas?  Waarom reageren aluminium en titanium normaal niet?
Waarom reageren aluminium en titanium normaal niet?  Wat zijn twee manieren om een oplossing te scheiden die vloeistoffen bevat?
Wat zijn twee manieren om een oplossing te scheiden die vloeistoffen bevat?  Nieuwe nanodeeltjes ontwikkeld om kanker in beeld te brengen en te behandelen
Nieuwe nanodeeltjes ontwikkeld om kanker in beeld te brengen en te behandelen
 Hoe koud was de ijstijd? Onderzoekers weten het nu
Hoe koud was de ijstijd? Onderzoekers weten het nu  Aanvaarding van elektrische voertuigen verbetert de luchtkwaliteit en klimaatvooruitzichten
Aanvaarding van elektrische voertuigen verbetert de luchtkwaliteit en klimaatvooruitzichten Heeft het bamboe -bladverliezende bos een voedselweb?
Heeft het bamboe -bladverliezende bos een voedselweb?  Hoe vervuiling buitenshuis de luchtkwaliteit binnenshuis beïnvloedt
Hoe vervuiling buitenshuis de luchtkwaliteit binnenshuis beïnvloedt  Giftig, langdurige verontreinigingen gedetecteerd bij mensen die in het noorden van Canada wonen
Giftig, langdurige verontreinigingen gedetecteerd bij mensen die in het noorden van Canada wonen
Hoofdlijnen
- Hoe zorgwekkend is het dat vogelgriep overspringt naar melkkoeien? Dit is wat experts zeggen
- Wat ontgift de cel?
- Door wetenschap ondersteunde manieren om een nieuwe studie te starten
- Wat vier decennia zalm in blik onthullen over de voedselketens in de zee
- Het orgaan in het lichaam absorbeert meer water is groot Instestine?
- Onderzoeksthema's in de biotechnologie
- Indonesië's selfiesnagende aap uitgeroepen tot Persoon van het Jaar
- Wat zijn de twee basismanieren waarop stoffen een cel binnenkomen of verlaten?
- Wat zijn de eerste vijf dieren op intelligentieschaal?
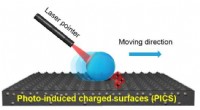
- Nieuw slim materiaal maakt hoogwaardige en betrouwbare lichtregeling van druppels mogelijk
- Wetenschappers ontdekken bij toeval zeldzame clusterverbinding

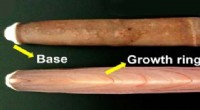
- Zee-egelstekels kunnen botten repareren
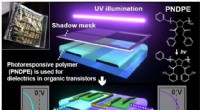
- Flexibele circuits afstemmen met licht
- Nieuwe studie onthult ladingsoverdracht op het grensvlak van spineloxide en ceria tijdens oxidatie van koolmonoxide

 Wat is de moleculaire formule van pepton?
Wat is de moleculaire formule van pepton?  Is virtual reality liefdadigheidsfondsenwerving armoedetoerisme in vermomming?
Is virtual reality liefdadigheidsfondsenwerving armoedetoerisme in vermomming? Wat zijn enkele beperkingen van het gebruik van verwarming om te bepalen of de stof een element of een verbinding is?
Wat zijn enkele beperkingen van het gebruik van verwarming om te bepalen of de stof een element of een verbinding is?  Waarom reist Comet door ons zonnestelsel?
Waarom reist Comet door ons zonnestelsel?  Ramanujan-machine genereert automatisch vermoedens voor fundamentele constanten
Ramanujan-machine genereert automatisch vermoedens voor fundamentele constanten 5 voorbeelden van stoffen en voorbeeldmengsels?
5 voorbeelden van stoffen en voorbeeldmengsels?  Hoeveel energie wordt verwijderd wanneer 10,0 g water is gekoeld van stoom bij 133,0 ° C tot vloeistof 53,0 ° C?
Hoeveel energie wordt verwijderd wanneer 10,0 g water is gekoeld van stoom bij 133,0 ° C tot vloeistof 53,0 ° C?  Waarom zijn er geen moderne buitenwijken gebouwd op een beloopbaar raster?
Waarom zijn er geen moderne buitenwijken gebouwd op een beloopbaar raster?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

