
Wetenschap
Is het waar dat stikstof een meer reactief element is dan zuurstof?
* elektronegativiteit: Zuurstof heeft een hogere elektronegativiteit dan stikstof. Dit betekent dat het een sterkere aantrekkingskracht heeft op elektronen, waardoor het waarschijnlijker is om bindingen te vormen en deel te nemen aan chemische reacties.
* bindingssterkte: De stikstof-nitrogene drievoudige binding (N≡N) is erg sterk, waardoor het moeilijk is om te breken. Zuurstof daarentegen vormt dubbele bindingen (o =O) die zwakker en gemakkelijker te breken zijn.
* Oxidatietoestand: Zuurstof accepteert gemakkelijk elektronen en vormt vaak een -2 oxidatietoestand. Stikstof kan verschillende oxidatietoestanden hebben, maar het is minder vatbaar voor het accepteren van elektronen in vergelijking met zuurstof.
Voorbeelden van reactiviteit:
* verbranding: Zuurstof is essentieel voor verbranding, omdat het gemakkelijk reageert met brandstoffen zoals hout en koolwaterstoffen om energie vrij te maken. Stikstof daarentegen is relatief inert in verbrandingsreacties.
* Atmosferische samenstelling: De atmosfeer is ongeveer 78% stikstof en 21% zuurstof. Dit komt omdat de lage reactiviteit van stikstof het stabiel maakt in de atmosfeer, terwijl de reactiviteit van zuurstof het doet deelnemen aan verschillende processen zoals ademhaling en oxidatie.
Uitzonderingen:
Hoewel zuurstof over het algemeen reactiever is, zijn er enkele uitzonderingen waar stikstof reactiever kan zijn. Dit gebeurt vaak onder specifieke omstandigheden, zoals hoge temperaturen of met zeer reactieve verbindingen.
Samenvattend: De hoge elektronegativiteit van zuurstof, de zwakkere bindingssterkte en de neiging om elektronen te verkrijgen, maken het een reactiever element dan stikstof onder typische omstandigheden.
 Kunnen mineralen elementen vormen die opgelost zijn in een oplossing?
Kunnen mineralen elementen vormen die opgelost zijn in een oplossing?  Wat is de moleculaire vorm van een watermolecuul en waarom?
Wat is de moleculaire vorm van een watermolecuul en waarom?  Onderzoekers lossen 60 jaar oude puzzel op over superhard materiaal
Onderzoekers lossen 60 jaar oude puzzel op over superhard materiaal Koolstof vertoont kwantumeffecten
Koolstof vertoont kwantumeffecten Slechts een klein stukje papier kan het waterverbruik veiliger maken
Slechts een klein stukje papier kan het waterverbruik veiliger maken
 Fruitvliegjes:zomerplaag of wetenschappelijk wonder?
Fruitvliegjes:zomerplaag of wetenschappelijk wonder?  Hoe de walvisvangst werkt
Hoe de walvisvangst werkt  Onderzoekers ontdekken dat wegen het aardoppervlak verbrijzelen in 600, 000 fragmenten
Onderzoekers ontdekken dat wegen het aardoppervlak verbrijzelen in 600, 000 fragmenten Op welke manieren is de houding ten opzichte van de natuur anders dan die van een wetenschapper?
Op welke manieren is de houding ten opzichte van de natuur anders dan die van een wetenschapper?  Een oproep om veel meer land en zee te beschermen tegen menselijke aantasting
Een oproep om veel meer land en zee te beschermen tegen menselijke aantasting
Hoofdlijnen
- Wat is het verschil tussen cytoplasma en protoplasma?
- Waarom zijn er zoveel hondenrassen, maar slechts een paar kattenrassen?
- Een geval van chimpansees of een grote uitbraak? Syndromale surveillance kan van cruciaal belang zijn
- Man of vrouw? Bij vliegen kunnen sommige cellen het niet zien
- Wat is celvergroting en verdeling?
- Wat doet de biosfeer met mensen?
- Gekapte tropische regenwouden ondersteunen nog steeds de biodiversiteit, zelfs als de hitte aan staat
- Waar worden mesenchymale stamcellen voor gebruikt?
- Wat zijn de verschillende vormen van wetenschappelijke kennis?
- Doorbraak verbetert de prestaties van natrium-zwavelbatterijen

- Nieuw polymeercomposiet voor elektromagnetische afschermingstoepassingen

- Recente vooruitgang in driedimensionale poreuze koolstofmaterialen voor absorptie van elektromagnetische golven
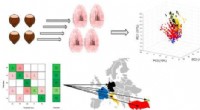
- Authenticatie van de geografische oorsprong van hazelnoten
- Verbetering van methoden voor het afleveren van genen

 Bij het ontdooien van permafrost komt mogelijk meer CO2 vrij dan eerder werd gedacht, studie suggereert:
Bij het ontdooien van permafrost komt mogelijk meer CO2 vrij dan eerder werd gedacht, studie suggereert: Hoe gloeiende Watts te converteren naar LED Watts
Hoe gloeiende Watts te converteren naar LED Watts Een sprong in het continuüm
Een sprong in het continuüm Onderzoekers ontwikkelen biohernieuwbare, biologisch afbreekbare kunststoffen
Onderzoekers ontwikkelen biohernieuwbare, biologisch afbreekbare kunststoffen Bali vulkaan gevaar tekent onverminderd week na hoge alertheid
Bali vulkaan gevaar tekent onverminderd week na hoge alertheid Vredesopbouw in conflictgebieden vereist een mensgerichte benadering
Vredesopbouw in conflictgebieden vereist een mensgerichte benadering Beeldvorming met hoog contrast voor kankertherapie met protonen
Beeldvorming met hoog contrast voor kankertherapie met protonen Orkaanrisico's begrijpen - 5 essentiële reads
Orkaanrisico's begrijpen - 5 essentiële reads
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

