
Wetenschap
Wat is molaire massa in de chemie?
Molaire massa in chemie:de massa van één mol
Molaire massa is een fundamenteel concept in de chemie die de massa van één mol van een stof definieert .
Hier is een uitsplitsing:
* mol (mol): Een meeteenheid die een specifiek aantal deeltjes vertegenwoordigt (atomen, moleculen, ionen, enz.). Eén mol bevat 6.022 x 10^23 deeltjes , ook bekend als het nummer van Avogadro .
* molaire massa (g/mol): De massa van één mol van een stof tot expressie gebracht in gram per mol (g/mol).
Hoe molaire massa te bepalen:
Je kunt de molaire massa van een element vinden door te kijken naar de Atomic Mass Atomic op het periodiek systeem. Deze waarde vertegenwoordigt de gemiddelde massa van een atoom van dat element in atomaire massa -eenheden (AMU). Omdat 1 AMU ongeveer gelijk is aan 1 g/mol, is de atoommassa numeriek gelijk aan de molaire massa van het element.
Voor verbindingen , u moet de molaire massa's van alle aanwezige elementen toevoegen, rekening houdend met het aantal van elk element in de formule van de verbinding.
Voorbeelden:
* waterstof (h): Molaire massa =1,008 g/mol (uit de periodiek systeem)
* water (h₂o): Molaire massa =(2 x 1,008 g/mol) + 15,999 g/mol =18,015 g/mol
* Natriumchloride (NaCl): Molaire massa =22.990 g/mol + 35.453 g/mol =58,443 g/mol
Waarom is molaire massa belangrijk?
Molaire massa is cruciaal in de chemie omdat het ons in staat stelt:
* converteren tussen massa en mol: Dit is essentieel voor veel berekeningen, zoals het bepalen van de hoeveelheid reactanten die nodig zijn voor een specifieke chemische reactie.
* Bereken de concentratie van oplossingen: Met behulp van molaire massa kunnen we de concentratie van een oplossing in eenheden van molariteit (mol per liter) uitdrukken.
* Begrijp de stoichiometrie van reacties: Chemische vergelijkingen tonen de verhouding van mol reactanten en producten die bij een reactie betrokken zijn. Melaire massa stelt ons in staat om deze verhoudingen om te zetten in gram, waardoor het gemakkelijker wordt om met real-world hoeveelheden te werken.
In wezen fungeert molaire massa als een brug tussen de microscopische wereld van atomen en moleculen en de macroscopische wereld die we ervaren. Het helpt ons de hoeveelheden die betrokken zijn bij chemische reacties en processen te begrijpen, waardoor het een essentieel hulpmiddel is voor chemici.
 Een elektronensnelweg op weg naar methanol
Een elektronensnelweg op weg naar methanol Is het onmogelijk voor een element om atomen van anothesen in een compound te vervangen?
Is het onmogelijk voor een element om atomen van anothesen in een compound te vervangen?  Wat is de oplosbaarheid van carbonaatzouten?
Wat is de oplosbaarheid van carbonaatzouten?  Wat zijn niet -voorbeelden van het Coriolis -effect?
Wat zijn niet -voorbeelden van het Coriolis -effect?  Hoeveel mol gas bezetten 1,3 L bij een druk 3,89 atmosferen en temperatuur 323 K?
Hoeveel mol gas bezetten 1,3 L bij een druk 3,89 atmosferen en temperatuur 323 K?
 Droogte, zondvloed veranderde stabiele aardverschuiving in een ramp
Droogte, zondvloed veranderde stabiele aardverschuiving in een ramp Zijn depressies in de Canadese prairies de sleutel tot het aanvullen van grondwater?
Zijn depressies in de Canadese prairies de sleutel tot het aanvullen van grondwater? Verkeersdichtheid, wind- en luchtstratificatie beïnvloeden concentraties luchtverontreinigende stof stikstofdioxide
Verkeersdichtheid, wind- en luchtstratificatie beïnvloeden concentraties luchtverontreinigende stof stikstofdioxide NASA vindt een piekerige, door de wind geschoren tropische depressie 06W
NASA vindt een piekerige, door de wind geschoren tropische depressie 06W Noord-Atlantisch klimaat veel voorspelbaarder na grote wetenschappelijke doorbraak
Noord-Atlantisch klimaat veel voorspelbaarder na grote wetenschappelijke doorbraak
Hoofdlijnen
- Is menselijke groei een fysieke of chemische verandering?
- Veel microscopische organismen die moeilijk te classificeren waren geplaatst in het koninkrijk?
- Hoe bloedzuigende insecten donkergecoat vee in het donker vinden
- Hoe neemt een forel zuurstof in?
- Welke cel kan een benige matrix opbouwen?
- Ondergewaardeerde microben krijgen nu de eer voor het behouden van twee banen in de bodem
- Het eerste genetische materiaal was waarschijnlijk?
- Hoe wordt DNA gebruikt om organismen te helpen classificeren?
- DNA kraakt een eeuwenoud mysterie over de enige uitgestorven zoetwatervis van Nieuw-Zeeland
- DNA-origami vol krachtige antikankermiddelen
- Nieuwe methode om uranium in zeewater te verrijken

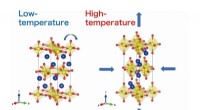
- Studie onderzoekt opmerkelijke negatieve thermische uitzetting gezien in gelaagde ruthenaten
- Team gebruikt 3D-printen om doorstroomelektroden voor elektrochemische reactoren te optimaliseren

- Miniatuurdruppels kunnen een raadsel over de oorsprong van het leven oplossen

 Hoe ver is Mars verwijderd van de aarde en de zon?
Hoe ver is Mars verwijderd van de aarde en de zon?  Overheidsregimes leren mogelijk nieuwe Twitter-tactieken om afwijkende meningen de kop in te drukken
Overheidsregimes leren mogelijk nieuwe Twitter-tactieken om afwijkende meningen de kop in te drukken Wat doet bakpoeder bij DNA -extractie?
Wat doet bakpoeder bij DNA -extractie?  Actieve levering van Cas9-sgRNA-complex in de cel met behulp van ultrageluid aangedreven nanomotoren
Actieve levering van Cas9-sgRNA-complex in de cel met behulp van ultrageluid aangedreven nanomotoren Wat zijn 5 landen met een polaire zone?
Wat zijn 5 landen met een polaire zone?  Wat zijn twee dingen gemaakt van broom?
Wat zijn twee dingen gemaakt van broom?  Archeologen gebruiken tandglazuur-eiwit om geslacht van menselijke resten aan te tonen
Archeologen gebruiken tandglazuur-eiwit om geslacht van menselijke resten aan te tonen Onderzoekers volgen de milieu-impact van steenovens in Zuid-Azië
Onderzoekers volgen de milieu-impact van steenovens in Zuid-Azië
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

