
Wetenschap
Is het onmogelijk voor een element om atomen van anothesen in een compound te vervangen?
Dit is waarom het complex is:
* chemische bindingen: Atomen in een verbinding worden bij elkaar gehouden door chemische bindingen. Om een atoom te vervangen, moet u deze obligaties doorbreken en nieuwe vormen. Dit vereist energie -input.
* Reactiviteit: Verschillende elementen hebben verschillende reactiviteiten. Sommige elementen zullen eerder deelnemen aan reacties dan andere. Een meer reactief element kan een minder reactief element in een verbinding verplaatsen.
* chemische eigenschappen: De eigenschappen van de verbinding kunnen de kans beïnvloeden dat een element wordt vervangen. De oplosbaarheid van de verbinding in een bepaald oplosmiddel kan bijvoorbeeld een rol spelen.
Hier zijn enkele voorbeelden van hoe elementen atomen in verbindingen kunnen vervangen:
* Enkele verplaatsingsreacties: In deze reacties verplaatst een meer reactief element een minder reactief element van een verbinding. Bijvoorbeeld:
* Zink reageert met koper (ii) sulfaat: Zn (S) + Cuso₄ (aq) → Cu (s) + ZnSo₄ (aq)
* Redox -reacties: In deze reacties worden elektronen overgebracht tussen atomen. Dit kan leiden tot de vervanging van atomen in een verbinding. Bijvoorbeeld:
* Natrium reageert met water: 2na (s) + 2H₂O (l) → 2naOH (aq) + h₂ (g)
* verbrandingsreacties: In verbranding reageert een stof met zuurstof om nieuwe verbindingen te vormen. Dit kan de vervanging van atomen in de oorspronkelijke verbinding met zich meebrengen. Bijvoorbeeld:
* brandend methaan: Ch₄ (g) + 2o₂ (g) → co₂ (g) + 2h₂o (g)
Het is belangrijk op te merken dat deze reacties vaak specifieke omstandigheden vereisen, zoals warmte, katalysatoren of specifieke oplosmiddelen, optreden.
Hoewel het niet onmogelijk is voor een element om atomen in een verbinding te vervangen, is het geen eenvoudig proces en vereist het zorgvuldig overweging van de chemische eigenschappen van de betrokken elementen.
 Nieuwe technologie verandert een zonnige dag in veilig water
Nieuwe technologie verandert een zonnige dag in veilig water  Hoe beleidsmakers gegevens uit nieuwe onderzoeken kunnen gebruiken om klimaatdoelen te halen
Hoe beleidsmakers gegevens uit nieuwe onderzoeken kunnen gebruiken om klimaatdoelen te halen Wetenschappers ontdekken relatie tussen trillingen, water aan de rand van Cascadia
Wetenschappers ontdekken relatie tussen trillingen, water aan de rand van Cascadia Korstbeweging en vervormingssnelheden in de zuidelijke provincie Basin and Range
Korstbeweging en vervormingssnelheden in de zuidelijke provincie Basin and Range Stedelijke eekhoorns, hoeveel storen we je?
Stedelijke eekhoorns, hoeveel storen we je?
Hoofdlijnen
- Wat moet Finny Train Gene doen?
- Wat zijn de overeenkomsten tussen bacteriën en virus van een diercelplant?
- Wat is rodehond?
- Van koralen tot gewassen:hoe het leven de plannen voor zijn cellulaire energiecentrales beschermt
- Welke eigenschap kan een menselijk nageslacht erven?
- Wat is een wetenschappelijk model en hoe het nuttig is voor wetenschappers?
- Wat is de zuurstofroute als we inademen?
- Wat worden de secties van DNA genoemd tijdens replicatie?
- Wiskundigen en biologen leggen uit waarom de darmen van gewervelde dieren zo voorspelbaar krom zijn
- Detectie van kankermarkers in één molecuul brengt vloeibare biopsie dichter bij de kliniek

- Chemici ontdekken hoe blauw licht blindheid versnelt

- De groeiende mogelijkheden van biobased polymeren

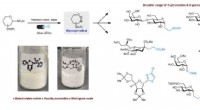
- Activering met zichtbaar licht maakt transformatie van stabiele sulfonen naar waardevolle glycosiden mogelijk
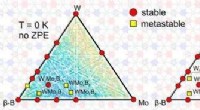
- Wetenschappers voorspellen nieuwe, moeilijk, en superharde ternaire verbindingen
 Nepals laagland voedselmand kwetsbaar voor klimaatverandering
Nepals laagland voedselmand kwetsbaar voor klimaatverandering Zonnewaterstof:fotoanodes beloven hoge efficiëntie
Zonnewaterstof:fotoanodes beloven hoge efficiëntie Geef de leraar niet de schuld:de resultaten van studenten zijn (meestal) uit hun handen
Geef de leraar niet de schuld:de resultaten van studenten zijn (meestal) uit hun handen Wat is de veiligste manier om zon te bekijken?
Wat is de veiligste manier om zon te bekijken?  Enzymonderzoek onthult waarom sommige kankermedicijnen ernstige bijwerkingen veroorzaken
Enzymonderzoek onthult waarom sommige kankermedicijnen ernstige bijwerkingen veroorzaken  Wat maakt een Hill Mountain?
Wat maakt een Hill Mountain?  Welk antwoord is niet een van de drie theorieën Moon Formation?
Welk antwoord is niet een van de drie theorieën Moon Formation?  Wat zijn rotsen gemaakt van grotere stukken sediment genoemd?
Wat zijn rotsen gemaakt van grotere stukken sediment genoemd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

