
Wetenschap
Gebruik VSEPR -theorie om de vorm van koolstoftetraiodide -molecuul CI4 te voorspellen?
1. Lewis -structuur:
* Koolstof (C) heeft 4 valentie -elektronen.
* Jodium (I) heeft 7 valentie -elektronen.
Om een stabiel octet te bereiken, vormt koolstof vier enkele bindingen met vier jodiumatomen. De Lewis -structuur ziet er zo uit:
I
|
I - c - i
|
I
2. Elektronedomeingeometrie:
* centraal atoom: Koolstof
* Aantal elektronendomeinen rond centraal atoom: 4 (elke enkele binding vertegenwoordigt één elektronendomein)
Volgens de VSEPR -theorie leiden 4 elektronendomeinen rond een centraal atoom naar een tetrahedral Elektronedomeingeometrie.
3. Moleculaire geometrie:
* Aangezien alle vier elektronendomeinen bindparen (enkele bindingen) zijn, is de moleculaire geometrie hetzelfde als de geometrie van de elektronomein: tetraëdral .
Daarom is de vorm van koolstoftetraiodide (CI₄) tetraëdrisch.
 Hoe wordt chloroform gebruikt?
Hoe wordt chloroform gebruikt?  Zou een stof met een pH-waarde van 2 erg zuur of basisch zijn?
Zou een stof met een pH-waarde van 2 erg zuur of basisch zijn?  Welke van de volgende wordt onderzocht om fusiereacties op aarde te bevatten?
Welke van de volgende wordt onderzocht om fusiereacties op aarde te bevatten?  Bestaat er zoiets als niet-giftige stof?
Bestaat er zoiets als niet-giftige stof?  Op weg naar de selectieve en energie-efficiënte synthese van ethyleen via koolstofdioxidereductie
Op weg naar de selectieve en energie-efficiënte synthese van ethyleen via koolstofdioxidereductie
 Stedelijke hitte en sterfte:wie zijn het meest kwetsbaar?
Stedelijke hitte en sterfte:wie zijn het meest kwetsbaar? Drugsvervuiling tegen kanker is een groeiend mondiaal probleem
Drugsvervuiling tegen kanker is een groeiend mondiaal probleem  Hoe beïnvloedt ruimte -exploratie de omgeving?
Hoe beïnvloedt ruimte -exploratie de omgeving?  Welke planten en dieren leven er in de bamboebossen?
Welke planten en dieren leven er in de bamboebossen?  NASA publiceert nieuwe hoogwaardige, bijna realtime gegevens over de luchtkwaliteit
NASA publiceert nieuwe hoogwaardige, bijna realtime gegevens over de luchtkwaliteit
Hoofdlijnen
- Welke biologische moleculen worden gebruikt om energie op te slaan in levende organismen, variëren in structuur en vormen het grootste deel van het celmembraan?
- Waar kwamen hersenen vandaan?
- Wat betekent in de wetenschap?
- Hebben rode bloedcellen van kippen kern?
- Waarom en hoe voert u een strengtest?
- Cowpea beschermd tegen een verwoestende plaag, gratis voor kleine Afrikaanse boeren
- Krijgen enzymen hulp van cofactoren?
- Hoe ontstaan vliegen?
- Hoe verschillen de verschillende soorten RNA?
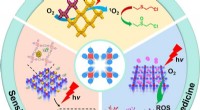
- Recente vorderingen in de ontwikkeling van foto- en elektroactieve waterstofgebonden organische raamwerken
- Chemici gebruiken supercomputers om oplosmiddelen te begrijpen

- Zonnepanelen met dunne schil bedrukt met inkjet

- Actief leren versnelt het ontdekken van redox-flow-batterijen

- Versterking van passieve bemonstering van niet-polaire chemicaliën

 Antilichamen zijn eiwitmoleculen die zich hechten aan?
Antilichamen zijn eiwitmoleculen die zich hechten aan?  Aanwijzingen uit verzuurde melk onthullen hoe goudaders ontstaan
Aanwijzingen uit verzuurde melk onthullen hoe goudaders ontstaan  Hoe scheiden de aarde in landen?
Hoe scheiden de aarde in landen?  Synthese van een koolstof nanobelt met mogelijke toepassingen in nanotechnologie
Synthese van een koolstof nanobelt met mogelijke toepassingen in nanotechnologie Twee fouten die proberen het goed te maken:make-upgesprekken zijn gebruikelijk voor MLB-umpires, financiële analisten en waarschijnlijk ook voor jou
Twee fouten die proberen het goed te maken:make-upgesprekken zijn gebruikelijk voor MLB-umpires, financiële analisten en waarschijnlijk ook voor jou  Wetenschappers ontdekken belangrijke bijdrage van diepe microben aan de koolstofcyclus van de aarde
Wetenschappers ontdekken belangrijke bijdrage van diepe microben aan de koolstofcyclus van de aarde Een nieuwe benadering van een oude vraag:hoe werken we eigenlijk samen?
Een nieuwe benadering van een oude vraag:hoe werken we eigenlijk samen? Is de maan helderder dan sterren?
Is de maan helderder dan sterren?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

