
Wetenschap
Waarom is Ferric Ion stabieler dan ijzerraad?
* Elektronische configuratie: Ferro -ion heeft een stabiele 3D⁶ -configuratie, terwijl Ferric Ion een 3D⁵ -configuratie heeft. Het halfgevulde D orbitaal in ijzerionen biedt enige stabiliteit, maar het is niet zo belangrijk als het volledig gevulde d orbitaal in ferrous-ion.
* Hydratatie -energie: Ferro -ionen hebben een hogere hydratatie -energie dan ijzerionen. Hydratatie -energie is de energie die vrijkomt wanneer ionen worden omgeven door watermoleculen. De hogere ladingsdichtheid van ijzerionen leidt tot sterkere interacties met watermoleculen, maar het resulteert ook in een grotere elektrostatische afstoting tussen de watermoleculen en het ion, waardoor de totale hydratatie -energie lager wordt.
* Redox -potentieel: Ferro -ionen worden gemakkelijker geoxideerd tot ijzerionen dan de omgekeerde reactie. Dit suggereert dat ijzerionen minder stabiel zijn dan ferro -ionen.
Er zijn echter enkele situaties waarin ferrische ion stabieler kan zijn:
* In aanwezigheid van sterke oxiderende middelen: In aanwezigheid van sterke oxiderende middelen kunnen ijzerionen worden gestabiliseerd vanwege de vorming van stabiele complexen. Ferrisch ion kan bijvoorbeeld stabiele complexen vormen met cyanide -ionen (Fe (CN) ₆³⁻) die stabieler zijn dan de overeenkomstige ferreu -complexen.
* In aanwezigheid van specifieke liganden: Bepaalde liganden kunnen bij voorkeur binden aan ijzerionen en stabiliseren ze.
Samenvattend, terwijl ijzerionen over het algemeen stabieler zijn dan ijzerionen in oplossing, kan de stabiliteit van beide ionen worden beïnvloed door factoren zoals de aanwezigheid van oxidatiemiddelen, liganden en pH.
 China belooft zich te houden aan klimaatakkoord Parijs
China belooft zich te houden aan klimaatakkoord Parijs Dag van de Aarde:Hoe een idee van de senator meer dan vijftig jaar geleden ervoor zorgde dat mensen voor hun planeet gingen vechten
Dag van de Aarde:Hoe een idee van de senator meer dan vijftig jaar geleden ervoor zorgde dat mensen voor hun planeet gingen vechten  Klimaatadaptatie op toekomstige veranderingen in de regenvalintensiteiten in het VK
Klimaatadaptatie op toekomstige veranderingen in de regenvalintensiteiten in het VK UITLEG:Was een tornado-uitbraak gerelateerd aan klimaatverandering?
UITLEG:Was een tornado-uitbraak gerelateerd aan klimaatverandering? Is een rozenstruik en object in beweging?
Is een rozenstruik en object in beweging?
Hoofdlijnen
- Welke lagen van de opperhuid verdelen cel?
- Oorlog tegen onkruid eist zijn tol van nuttige bacteriën in de bodem
- Wat zijn de bouwstenen voor eiwitten?
- Wat is het proces waarbij stoffen de cellen binnenkomen en verlaten en binnen de cellen worden verdeeld?
- Het reuzenschaap dat Tadzjikistan helpt de klimaatverandering te doorstaan
- Wat is een mogelijke bron van cellulase-enzymen op hoge temperatuur?
- Wat zijn de vier meest voorkomende elementen in het menselijk lichaam, sommige van moleculen die ze helpen vormen en waarom deze belangrijke termen hun biologische functies?
- Wat zijn de vier steriele sites in het menselijk lichaam?
- Verschillen tussen codering en sjabloonstrengen
- Het beste van twee werelden:hoge entropie ontmoet lage dimensies, opent oneindige mogelijkheden

- Nieuw materiaal kan de productie van plastic energiezuiniger maken
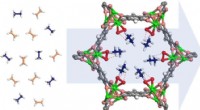
- Een regelbaar membraan om koolstofdioxide uit uitlaatstromen te halen

- Alles in orde:een omkeerbare moleculaire zweefmolen
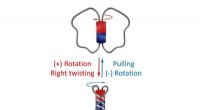
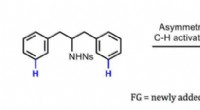
- Chemici bereiken belangrijke mijlpaal van synthese:chirale inductie op afstand
 Ideeën voor een Shoebox Animal Habitat Project
Ideeën voor een Shoebox Animal Habitat Project  Welke krachten veroorzaken verwering en erosie?
Welke krachten veroorzaken verwering en erosie?  Nog een reden om de uit-schakelaar om te zetten:lichtvervuiling
Nog een reden om de uit-schakelaar om te zetten:lichtvervuiling Augmented reality ‘sandbox’ laat zien hoe zwaartekracht werkt
Augmented reality ‘sandbox’ laat zien hoe zwaartekracht werkt  Gap-geometrie begrepen:nieuw algoritme kan helpen de structuur van vloeistoffen te begrijpen, en hoe ze door poreuze media stromen
Gap-geometrie begrepen:nieuw algoritme kan helpen de structuur van vloeistoffen te begrijpen, en hoe ze door poreuze media stromen  1 metriek is gelijk aan hoeveel gram?
1 metriek is gelijk aan hoeveel gram?  Wilt u verantwoorde robotica? Begin met mensen
Wilt u verantwoorde robotica? Begin met mensen  Nefertiti was geen farao, zegt gerenommeerde egyptoloog
Nefertiti was geen farao, zegt gerenommeerde egyptoloog
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

