
Wetenschap
Wat is de algemene elektronische grondtoestand elektronelektronenconfiguratie voor neutrale alkalische aardmetalen?
Dit is waarom:
* alkalische aardmetalen bevinden zich in groep 2 van het periodiek systeem.
* valentie -elektronen zijn de elektronen in de buitenste schaal van een atoom, die betrokken zijn bij chemische binding.
* grondtoestand elektronenconfiguratie verwijst naar de opstelling van elektronen in een atoom wanneer het zich in de laagste energietoestand bevindt.
Bijvoorbeeld:
* beryllium (BE): 1S² 2S² (valentie -elektronen:2s²)
* magnesium (mg): 1S² 2S² 2P⁶ 3S² (valentie -elektronen:3S²)
* calcium (CA): 1S² 2S² 2P⁶ 3S² 3P⁶ 4S² (Valentie -elektronen:4S²)
De ns² Configuratie betekent dat alkalische aardmetalen twee valentie -elektronen hebben in hun buitenste s -orbitale, die hun neiging verklaart om deze twee elektronen te verliezen om +2 kationen te vormen.
 Onderzoek onthult de gevaarlijke impact van stijgende temperaturen op kinderen
Onderzoek onthult de gevaarlijke impact van stijgende temperaturen op kinderen Uit onderzoek blijkt dat de omstandigheden op het landoppervlak van invloed kunnen zijn op convectieve systemen op mesoschaal terwijl ze in beweging zijn
Uit onderzoek blijkt dat de omstandigheden op het landoppervlak van invloed kunnen zijn op convectieve systemen op mesoschaal terwijl ze in beweging zijn Studie legt de haalbaarheid vast voor het terugdringen van broeikasgasemissies op het land door bossen, landbouw en consumentengedrag
Studie legt de haalbaarheid vast voor het terugdringen van broeikasgasemissies op het land door bossen, landbouw en consumentengedrag Atmosferische rivieren blijken meer wind te dragen dan gedacht
Atmosferische rivieren blijken meer wind te dragen dan gedacht Verdrag om blootstelling aan kwik te beteugelen treedt in werking
Verdrag om blootstelling aan kwik te beteugelen treedt in werking
Hoofdlijnen
- Naam voor een reeks DNA -basen die één eiwit coderen?
- Onnauwkeurigheden in de GPT in de landbouw kunnen leiden tot oogstverliezen en voedselcrises
- Nieuwe fossielen leveren bewijs voor een tijdperk van monotremes
- Discovery legt uit hoe de Leishmania-parasiet de infectie versterkt
- Waarom verspreiden bloeiende planten hun zaden?
- Waarom hebben bacteriën geen kern?
- Welke bijdrage heeft Carl Linnaeus geleverd aan de evolutie?
- Wat produceren organismen?
- Wat zijn de kenmerken die alle bacteriën gemeen hebben?
- Video:Sublieme geheimen van sushi

- Ionische zonnecel kan on-demand waterontzilting bieden;

- Een op ruthenium gebaseerde katalysator met zeer actieve, vlakke oppervlakken presteren beter dan op metaal gebaseerde concurrenten
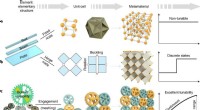
- Op tandwielen gebaseerde mechanische metamaterialen maken het mogelijk om configureerbare bladen te maken
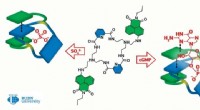
- Chemici maken een molecuul dat kan helpen bij de behandeling van hartaandoeningen en het opsporen van virussen
 De foutmarge berekenen
De foutmarge berekenen Huawei's AI-aangedreven smartphone bestuurt een Porsche
Huawei's AI-aangedreven smartphone bestuurt een Porsche Wat zijn de namen van twee MT Thera Interactie -platen?
Wat zijn de namen van twee MT Thera Interactie -platen?  Nieuwe COVID-19-test detecteert snel en nauwkeurig viraal DNA
Nieuwe COVID-19-test detecteert snel en nauwkeurig viraal DNA Crisis Hoe de macht in Californië werkt
Crisis Hoe de macht in Californië werkt  Hoeveel stikstofmoleculen zitten er in een ballon?
Hoeveel stikstofmoleculen zitten er in een ballon?  Is magnesiumchloride een goede geleider?
Is magnesiumchloride een goede geleider?  Hoe het volume van een cilinder in gallons te berekenen
Hoe het volume van een cilinder in gallons te berekenen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

