
Wetenschap
Waarom hebben atomen met een zwakke elektronegativiteit zoals lithium een aantrekkelijke kracht voor elektronen?
Hier is de uitsplitsing:
* elektronegativiteit: Dit is een maat voor het vermogen van een atoom om elektronen naar zichzelf aan te trekken wanneer het deel uitmaakt van een chemische binding. A High Elektronegativiteit betekent een sterke aantrekkingskracht voor elektronen, terwijl laag Elektronegativiteit betekent een zwakkere aantrekkingskracht.
* lithium (li): Lithium heeft een zeer lage elektronegativiteit, wat betekent dat het geen elektronen erg sterk aantrekt.
* Waarom verliest lithium elektronen? Lithium, ondanks zijn zwakke elektronegativiteit, verliest * gemakkelijk * zijn buitenste elektron om een positief geladen ion te worden (li⁺). Dit gebeurt omdat:
* het enige buitenste elektron is verre van de kern: Dit maakt het gemakkelijker om te verwijderen.
* Het wil een stabiele elektronenconfiguratie bereiken: Door het buitenste elektron te verliezen, bereikt lithium dezelfde elektronenconfiguratie als het edelgashelium, dat extreem stabiel is.
Samenvattend: Hoewel lithium een zwakke elektronegativiteit heeft, is het waarschijnlijker om te verliezen elektronen dan om ze te winnen. Dit verlies van elektronen is te wijten aan de wens om een stabiele elektronenconfiguratie te bereiken, niet omdat het een sterke aantrekkingskracht heeft op elektronen.
Hoofdlijnen
- Wat gebeurt er met een enzym als het zijn functie vervult? Wat betekent dit voor moleculen?
- Veren hebben hun eigen geuren, en roofdieren weten het
- Hoe DHX9-stresskorrels dochtercellen beschermen tegen UV-geïnduceerde RNA-schade
- Het foerageren van wild voedsel is goed voor bijna 250.000 kubieke meter producten die jaarlijks in Zambia worden geconsumeerd
- Wie is de grootste wetenschapper aller tijden?
- Anti-insuline-eiwit gekoppeld aan levensduur en voortplanting bij mieren
- Wat is de functie van mannose?
- Acht nieuwe soorten kleine gekko's tuimelen uit de regenwouden van Madagaskar
- Organismen die het lichaam binnenkomen en je ziek maken, worden ziek?
- Kleine sensoren ontwikkeld om de geheimen van hersenchemie te bestuderen

- Tweefasig materiaal met verrassende eigenschappen

- De uitdaging om koolstof op te vangen

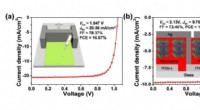
- Organische gaten-transporterende lagen met kleine moleculen naar efficiënte p-i-n perovskiet-zonnecellen
- Studie innoveert in glutenvrije formuleringen, smakelijker en voedzamer brood creëren

 Strikte Amazon-bescherming maakte Braziliaanse boeren productiever, nieuw onderzoek toont aan
Strikte Amazon-bescherming maakte Braziliaanse boeren productiever, nieuw onderzoek toont aan Wetenschappers kweken optische chips in petrischaal
Wetenschappers kweken optische chips in petrischaal Ontdekken hoe rivierwater in de zee wordt gemengd, kan helpen bij het in kaart brengen van de klimaatverandering
Ontdekken hoe rivierwater in de zee wordt gemengd, kan helpen bij het in kaart brengen van de klimaatverandering  Storing treft Facebook, Instagram-gebruikers wereldwijd
Storing treft Facebook, Instagram-gebruikers wereldwijd Waarom zijn de maan en de zon groter bij Horizon?
Waarom zijn de maan en de zon groter bij Horizon?  Wat is de pH van mierenzuur?
Wat is de pH van mierenzuur?  Hoe DNA duizenden jaren lang in archeologische sedimenten wordt bewaard
Hoe DNA duizenden jaren lang in archeologische sedimenten wordt bewaard  Nieuwe opties voor gezondheid, milieumonitoring met waterbestendige gassensor
Nieuwe opties voor gezondheid, milieumonitoring met waterbestendige gassensor
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


