
Wetenschap
In de grondtoestand heeft een atoom van elke elementen in groep 2 een ander?
Dit is waarom:
* Groep 2 elementen Ze hebben allemaal twee valentie -elektronen (elektronen in hun buitenste schaal).
* elektronenschalen vertegenwoordigen energieniveaus waar elektronen zich bevinden. Terwijl u een groep (kolom) op het periodiek systeem naar beneden verplaatst, neemt het aantal elektronenschalen toe.
Voorbeeld:
* beryllium (BE): Heeft 2 elektronen in de eerste schaal (1S²)
* magnesium (mg): Heeft 2 elektronen in de tweede schaal (2s²)
* calcium (CA): Heeft 2 elektronen in de derde schaal (3S²)
* strontium (SR): Heeft 2 elektronen in de vierde schaal (4S²)
Daarom is het aantal elektronenschalen, dat overeenkomt met het periodienummer op het periodieke tabel, het belangrijkste verschil in grondtoestandsatomen van groep 2 -elementen.
 Klimaatmodellen kunnen recente luchtdrukveranderingen boven Groenland niet simuleren
Klimaatmodellen kunnen recente luchtdrukveranderingen boven Groenland niet simuleren Klimaatverandering als gevolg van rook van nucleaire oorlogen kan de wereldwijde voedselvoorziening bedreigen, menselijke gezondheid
Klimaatverandering als gevolg van rook van nucleaire oorlogen kan de wereldwijde voedselvoorziening bedreigen, menselijke gezondheid Beter dan geld? Betalingen in natura stimuleren boeren om agrobiodiversiteit te behouden
Beter dan geld? Betalingen in natura stimuleren boeren om agrobiodiversiteit te behouden Soldaten ingezet om bosbranden in Engeland te bestrijden
Soldaten ingezet om bosbranden in Engeland te bestrijden Hoe PlayPump werkt
Hoe PlayPump werkt
Hoofdlijnen
- Hoe mycorrhiza-typen de effecten van biodiversiteit op de productiviteit beheersen
- Welke structuren in een cel met een specifieke functie?
- Wat bepaalt de sterkte van een arrheniusbasis?
- Wetenschappers hebben fundamentele ontdekkingen gedaan over de manier waarop eigenschappen van embryonale stamcellen worden gecontroleerd
- Epigenetische erfenis:een 'zilveren kogel' tegen klimaatverandering?
- Wat is de betekenis van boerderijdierenaandoeningen?
- Adenosine trifosfaat (ATP): definitie, structuur en functie
- Plasmamembraan: definitie, structuur en functie (met diagram)
- Wat is het verschil tussen cytokinese in dierlijke cellen en een plantencel?
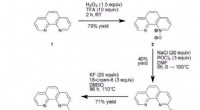
- Nieuwe methode voor het produceren van PET-radiotracers met hogere radiochemische opbrengsten
- Nieuwe studie analyseert levensvatbaarheid van duurzame brandstoffen ontwikkeld via nieuw proces

- Ontwikkeling van elektrodemateriaal dat de efficiëntie van zoutgehaltegradiëntenergie verbetert

- Het volgen van pileups op de oplaadroute van de batterij om de prestaties te verbeteren

- Een ademtest voor Parkinson in een vroeg stadium
 Waarom worden sterrenbeelden gezien in de zomerhemel anders dan Winter Sky?
Waarom worden sterrenbeelden gezien in de zomerhemel anders dan Winter Sky?  Welk nationaal park in de VS heeft de hoogste bomen?
Welk nationaal park in de VS heeft de hoogste bomen?  Wat is de wetenschappelijke naam voor North Star?
Wat is de wetenschappelijke naam voor North Star?  Krachten van spinnengif onderzocht in VR-game
Krachten van spinnengif onderzocht in VR-game Feiten over terugkeer in de atmosfeer van de aarde
Feiten over terugkeer in de atmosfeer van de aarde  Experimenten combineren, modellen stimuleren onderzoek naar sociaal gedrag
Experimenten combineren, modellen stimuleren onderzoek naar sociaal gedrag Wat leidde tot de vorming van het zonnestelsel?
Wat leidde tot de vorming van het zonnestelsel?  Is het mogelijk om te overleven als je van de Grand Canyon valt?
Is het mogelijk om te overleven als je van de Grand Canyon valt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

